Калиев оксид: формула, взаимодействие
В неорганичната химия има три основни класа съединения. Това са киселини, основи и оксиди. Киселината се състои от катион на водород и анион на киселинен остатък. Алкалът е от метален катион и хидроксилна група. По-долу ще разгледаме по-подробно оксидите.
Какво е оксид?
Това съединение се състои от два различни химически елемента, единият от които е кислород. Вторият може да бъде метален или неметален. Броят на кислородните атоми зависи от валентността на втория химичен елемент, който е част от съединението. Например, валентността на калия е равна на единица, следователно калиевият оксид ще съдържа един кислороден атом и два калиеви атома. Валентността на калция е две, така че нейният оксид ще се състои от един кислороден атом и един калциев атом. Валентността на фосфора е пет, така че нейният оксид се състои от два фосфорни атома и пет кислородни атома.
Ad
В тази статия ще говорим повече за калиевия оксид. А именно - за неговите физични и химични свойства, за приложението му в различни индустрии. 
Калиев оксид: Формула
Тъй като валентността на този метал е една, а валентността на кислорода е две, това химично съединение ще се състои от два метални атома и един кислороден атом. Така че, калиев оксид: формула - K 2 O. 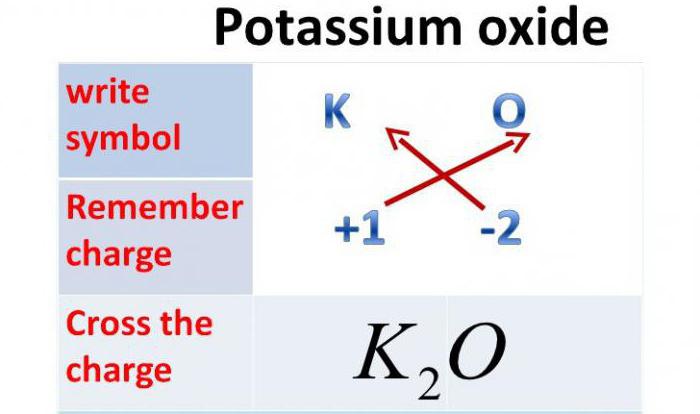
Физични свойства
Разглежданият оксид има бледожълт цвят. Понякога може да бъде безцветен. При стайна температура тя има агрегирано твърдо състояние.
Точката на топене на това вещество е 740 градуса по Целзий.
Плътността е 2.32 g / cm3.
Термичното разлагане на този оксид произвежда пероксид от същия метал и чист калий.
Разтворим в органични разтворители.
Не се разтваря във вода, а реагира с него.
Той е силно хигроскопичен.
Химични свойства на К2О
Това вещество има химични свойства, типични за всички основни оксиди. Помислете за химичните реакции на този оксид с различни вещества.
Реакция с вода
На първо място, той е в състояние да реагира с водата с образуването на хидроксида на метала.
Уравнението за тази реакция е както следва:
- К2О + Н20 = 2КОН
Знаейки моларната маса на всяко от веществата, може да се направи следното заключение от уравнението: 112 грама калиев хидроксид могат да бъдат получени от 94 грама от въпросния оксид и 18 грама вода.
С други оксиди
В допълнение, разглежданият оксид може да реагира с въглероден диоксид. (въглероден диоксид). Това образува сол - калиев карбонат. 
Уравнението за реакцията на калиев оксид и въглероден оксид може да бъде записано по следния начин:
- K 2 O + CO 2 = K 2 CO 3
Така може да се заключи, че от 94 грама от въпросния оксид и 44 грама въглероден диоксид, се получават 138 грама. калиев карбонат.
Също така, разглежданият оксид може да реагира със сулфорен оксид. Това образува друга сол - калиев сулфат.
Взаимодействието на калиев оксид със серен оксид може да се изрази със следното уравнение:
- K2O + SO3 = K2S04
Това показва, че като се вземат 94 грама от въпросния оксид и 80 грама оксид от сяра, могат да се получат 174 грама калиев сулфат.
По същия начин, К2О може да реагира с други оксиди.
Друг вид взаимодействие е реакцията не с кисела, а с амфотерни оксиди. В този случай това не е киселина, а сол, която се образува Пример за такъв химичен процес е взаимодействието на въпросния оксид с цинковия оксид.
Ad
Тази реакция може да бъде изразена чрез следното уравнение:
- K 2 O + ZnO = K 2 ZnO 2
Това показва, че при взаимодействието на въпросния оксид и цинковия оксид се образува сол, наречена калиев цинкат. Ако знаете моларната маса на всички вещества, може да се изчисли, че от 94 грама K 2 O и 81 грама цинков оксид, можете да получите 175 грама калиев цинкат.
Също така, K2O може да взаимодейства с азотен оксид. Това образува смес от две соли: нитрат и калиев нитрит. Уравнението за тази реакция изглежда така:
- K 2 O + 2NO 2 = KNO 3 + KNO 2
Ако знаете моларните маси на веществата, можем да кажем, че от 94 грама от въпросния оксид и 92 грама азотен оксид могат да се получат 101 грама нитрати и 85 грама нитрити. 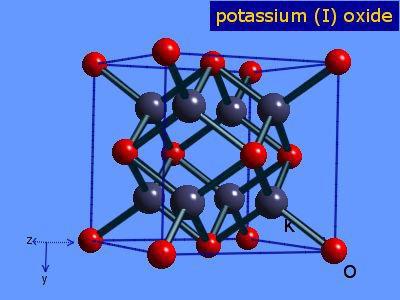
Взаимодействие с киселини
Най-често срещаният случай е калиев оксид + сярна киселина = калиев сулфат + вода. Уравнението на реакцията изглежда така:
- K2O + H2SO4 = K2S04 + H20
От уравнението може да се заключи, че за да се получат 174 грама калиев сулфат и 18 грама вода, трябва да се вземат 94 грама от въпросния оксид и 98 грама сярна киселина.
По същия начин, химичното взаимодействие протича между въпросния оксид и азотната киселина. Това образува калиев нитрат и вода. Уравнението за тази реакция може да бъде записано както следва:
Ad
- 2К 2 О + 4ННО 3 = 4KNO 3 + 2Н 2 О
Така от 188 грама от въпросния оксид и 252 грама азотна киселина могат да се получат 404 грама калиев нитрат и 36 грама вода.
По същия принцип, разглежданият оксид може да реагира с други киселини. При това ще се образуват други соли и вода. Така например, при реакцията на този оксид с фосфорна киселина се получават фосфат и вода, хлоридна киселина и вода, с хлорид и т.н. 
K2O и халогени
Разглежданото химическо съединение може също да реагира с вещества от тази група. Халогените включват прости съединения, състоящи се от няколко атома от един и същ химичен елемент. Това, например, хлор, бром, йод и някои други.
Ad
Така че, хлор и калиев оксид: уравнение:
- К 2 О + СІ 2 = КСІ + КСІО
В резултат на това взаимодействие се образуват две соли: калиев хлорид и хипохлорит. От 94 грама от въпросния оксид и 70 грама хлор се получават 74 грама калиев хлорид и 90 грама калиев хипохлорит.
Амонячна реакция
K 2 O може да реагира с това вещество. В резултат на това химично взаимодействие се образуват калиев хидроксид и амид. Уравнението за тази реакция е както следва:
- К2О + NH3 = KOH + KNH2
Познавайки моларните маси на всички вещества, можем да изчислим пропорциите на реактивите и реакционните продукти. От 94 грама от въпросния оксид и 17 грама амоняк могат да се получат 56 грама калиев хидроксид и 55 грама калиев амид.
Взаимодействие с органични вещества
От органични химикали калиевият оксид взаимодейства с етери и алкохоли. Тези реакции обаче са бавни и изискват специални условия.
Получаване на K 2 За
Този химикал може да се получи по няколко начина. Ето най-често срещаните:
- От калиев нитрат и метален калий. Тези два реагента се нагряват, което води до образуването на К2О и азот. Уравнението на реакцията е както следва: 2KNO 3 + 10K = N2 + 6K2O.
- Вторият метод се осъществява на два етапа. Първо, реакцията между калий и кислород се получава, което води до образуването на калиев пероксид. Уравнението на реакцията изглежда така: 2K + O 2 = K 2 O 2 . Освен това, пероксидът е обогатен с калий, в резултат на което се получава калиев оксид. Уравнението на реакцията може да бъде записано както следва: K 2 O 2 + 2 K = 2 K 2 O.

Използване на K 2 O в промишлеността
Най-често считаното вещество се използва в селскостопанския отрасъл. Този оксид е един от компонентите на минералните торове. Калият е много важен за растенията, тъй като увеличава тяхната устойчивост към различни заболявания. Разглежданото вещество се използва и в строителството, тъй като може да присъства в състава на някои видове цимент. В допълнение, той се използва в химическата промишленост за производство на други калиеви съединения.