Сярна киселина и нейните химични свойства
Киселините са химични съединения, състоящи се от водородни атоми и киселинни остатъци, например SO4, SO3, PO4 и др. Те са неорганични и органични. Първата включва солна, фосфорна, сулфидна, азотна, сярна киселина. Към втория - оцетна, палмитинова, мравчена, стеаринова и др.
Какво е сярна киселина
Тази киселина се състои от два водородни атома и киселинен остатък SO4. Той има формула H2SO4. 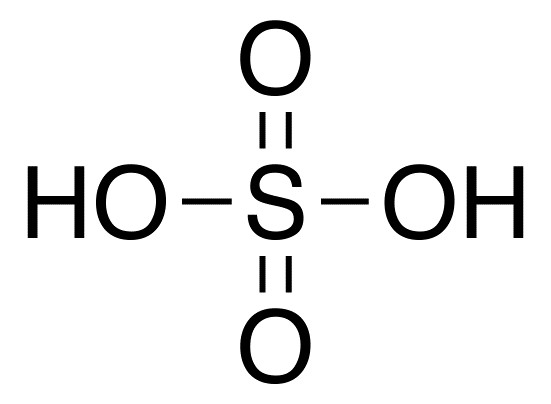 Сярна киселина или, както се нарича също, сулфат, се отнася до неорганични кислородсъдържащи двуосновни киселини. Това вещество се счита за едно от най-агресивните и химически активни. При повечето химични реакции той действа като окислител. Тази киселина може да се използва в концентрирана или разредена форма, като в тези два случая има леко различни химични свойства.
Сярна киселина или, както се нарича също, сулфат, се отнася до неорганични кислородсъдържащи двуосновни киселини. Това вещество се счита за едно от най-агресивните и химически активни. При повечето химични реакции той действа като окислител. Тази киселина може да се използва в концентрирана или разредена форма, като в тези два случая има леко различни химични свойства.
Физични свойства
Сярна киселина в нормални условия има течно състояние, нейната точка на кипене е около 279.6 градуса по Целзий, точката на замръзване, когато тя се превръща в твърди кристали, е около -10 градуса за сто процента и около -20 за 95 процента.  Чистата 100% сулфатна киселина е мазна, без мирис и безцветна течна субстанция, която има почти два пъти по-голяма плътност от водата - 1840 кг / м3.
Чистата 100% сулфатна киселина е мазна, без мирис и безцветна течна субстанция, която има почти два пъти по-голяма плътност от водата - 1840 кг / м3.
Химични свойства на сулфатната киселина
Сярна киселина реагира с метали, техните оксиди, хидроксиди и соли. Разреден с вода в различни пропорции, той може да се държи по различен начин, следователно, ние разглеждаме по-подробно свойствата на концентриран и слаб разтвор на сярна киселина поотделно.
Ad
Концентриран разтвор на сярна киселина
Концентриран е разтвор, който съдържа 90% сулфатна киселина. Такъв разтвор на сярна киселина може да реагира дори с ниско активни метали, както и с неметали, хидроксиди, оксиди, соли. Свойствата на този разтвор на сулфатна киселина са подобни на тези на концентрирана азотна киселина. 
Взаимодействие с метали
При химична реакция на концентриран разтвор на сулфатна киселина с метали, разположени отдясно на водород в електрохимичната серия от метални напрежения (т.е. с не най-активни), се образуват такива вещества: сулфатът на метала, с който се осъществява взаимодействието, вода и серен диоксид. Мед (меден), живак, бисмут, сребро (argentum), платина и злато (aurum) са метали, които са резултат от взаимодействия, с които се образуват изброените вещества.
Ad

Взаимодействие с неактивни метали
С метали, които са от лявата страна на водорода в поредица от напрежения, концентрираната сярна киселина се държи малко по-различно. В резултат на такава химична реакция се образуват следните вещества: специфичен метален сулфат, сероводород или чиста сяра и вода. Желязо (ferum), магнезий, манган, берилий, литий, барий, калций и всички останали в серия от напрежения отляво на водорода, с изключение на алуминий, хром, никел и титан - също са концентрирани с метали; сулфатна киселина не реагира.
Взаимодействие с неметали
Това вещество е силно окислително средство, поради което е способно да участва в окислително-редукционни химични реакции с неметали, като например въглерод (въглерод) и сяра. В резултат на такива реакции водата непременно се освобождава. Добавянето на това вещество към въглерода също освобождава въглероден диоксид и серен диоксид. И ако добавите киселина към сяра, получаваме само серен диоксид и вода. При такава химична реакция сулфатната киселина играе ролята на окислител.
Ad
Взаимодействие с органични вещества
Сред реакциите на сярна киселина с органична материя може да се разграничи овъгляването. Такъв процес се случва, когато дадено вещество се сблъсква с хартия, захар, влакна, дърво и т.н. Във всеки случай въглеродът се освобождава. Въглеродът, който се образува по време на реакцията, може частично да взаимодейства със сярна киселина, когато е в излишък. Снимката показва реакцията на захар с разтвор на сулфатна киселина със средна концентрация.

Реакции със соли
Концентрираният разтвор на H2SO4 също реагира със сухи соли. В този случай протича стандартна обменна реакция, при която се образува метален сулфат, който присъства в структурата на солта, и киселината с остатъка, който е в състава на солта. Въпреки това, със солни разтвори, концентрираната сярна киселина не реагира.
Взаимодействие с други вещества
Също така това вещество може да реагира с метални оксиди и техните хидроксиди, в тези случаи настъпват обменни реакции, в първия случай се освобождават метален сулфат и вода, във втория - същото.
Ad
Химични свойства на слаб разтвор на сулфатна киселина
Разредената сярна киселина реагира с много вещества и има същите свойства като всички киселини. Той, за разлика от концентрираните, взаимодейства само с активни метали, т.е. тези, които са отляво на водорода в поредица от напрежения. В този случай, същата заместителна реакция се случва както при всяка киселина. Това освобождава водород. Също така, такъв киселинен разтвор взаимодейства със солеви разтвори, в резултат на което възниква обменна реакция, която вече беше обсъдена по-горе, с оксиди - както и концентрирани, с хидроксиди - също по същия начин. Освен обикновените сулфати, съществуват и хидросулфати, които са продукт на взаимодействието на хидроксид и сярна киселина.

Как да знаем, че разтворът съдържа сярна киселина или сулфати
За да се определи дали тези вещества присъстват в разтвора, специално отговор на качеството до сулфатни йони, което ви позволява да знаете. Състои се в добавяне на барий или неговите съединения към разтвора. В резултат на това може да падне бяла утайка. (бариев сулфат), което показва наличието на сулфати или сярна киселина.
Как да извлечем сярна киселина
Най-разпространеният метод за промишлено производство на това вещество е да се извлече от железен пирит. Този процес се осъществява в три етапа, на всеки от които протича специфична химична реакция. Помислете за тях. Първо се добавя кислород към пирита, което води до образуването на железен оксид и серен диоксид, който се използва за по-нататъшни реакции. Това взаимодействие се осъществява при високи температури. Това е последвано от етапа, в който серен триоксид се получава чрез добавяне на кислород в присъствието на катализатор, който е ванадиев оксид. Сега в последния етап към полученото вещество се добавя вода и се получават сулфатни киселини. Това е най-често срещаният процес за търговско производство на сулфатна киселина, той се използва най-често, защото пиритът е най-лесно достъпният суров материал, подходящ за синтеза на веществото, описано в тази статия. Получената с този процес сярна киселина се използва в различни индустрии, както химически, така и много други, например рафиниране на нефт обогатяване на руди и т.н. Също така често се използва в технологията за производство на набор от синтетични влакна.