Законът за запазване на масата в химията. Откриване на закона
Законът за запазване на масата е основа за изчисляване на физическите процеси във всички сфери на човешката дейност. Неговата справедливост не се оспорва от физици, химици или представители на други науки. Този закон, като строг счетоводител, следи за спазването на точната маса на веществото преди и след взаимодействието му с други вещества. Честта на откриването на този закон принадлежи на руския учен М. В. Ломоносов.
Първоначално разбиране на състава на веществата
Структурата на материята от векове остава загадка за всеки човек. Различни хипотези вълнуваха умовете на учените и мотивираха мъдреците да водят дълги и безсмислени спорове. Един от тях твърди, че всичко се състои от огън, а другият - с напълно различна гледна точка. В масата на теориите проблясваха и теорията на древния гръцки мъдрец Демокрит, че всички вещества се състоят от малки, малки частици материя, които са невидими за окото, е несправедливо забравена. Демокрит ги нарича "атоми", което означава "неделимо". За съжаление, за цели 23 века неговото предположение беше забравено.
Ad
алхимия
Повечето от научните данни от Средновековието се основават на предразсъдъци и различни спекулации. Алхимията възниква и е широко разпространена, която е колекция от скромни практически познания, тясно ароматизирани с най-фантастичните теории. Например, добре познатите умове на онова време се опитаха да превърнат оловото в злато и да намерят камък на непознат философ, изцелявайки всички болести. В процеса на търсене постепенно се натрупва научен опит, състоящ се от много необясними реакции на химични елементи. Например, установено е, че много вещества, впоследствие наречени прости, не се разпадат. Така се възражда древната теория за неделимите частици на материята. За да се превърне този запас от информация в кохерентна и логическа теория, трябваше страхотен ум. 
Теория на Ломоносов
Точният количествен метод на изследователската химия е задължителен за руския учен М. В. Ломоносов. Заради блестящите си способности и упорита работа, той получава титлата професор по химия и става член на Руската академия на науките. Под него се организира първата модерна химическа лаборатория в страната, в която е открит известният закон за опазване на масата на веществата. 
В процеса на изучаване на потока химични реакции Ломоносов претегли оригиналните химикали и продукти, които се появиха след реакцията. В същото време той открива и формулира закона за запазване на масата на материята. През 17-ти век понятието за маса често се бърка с термина „тегло”. Следователно, масите на веществата често се наричат "тежести". Ломоносов определя, че структурата на материята е пряко зависима от частиците, от които е построена. Ако съдържа частици от един и същи вид, ученият нарича такова вещество просто. При хетерогенния състав на корпускулите се получава комплексно вещество. Тези теоретични данни позволиха на Ломоносов да формулира закона за масовото съхранение.
Ad
Определение на правото
След многобройни експерименти, М. В. Ломоносов създава закон, чиято същност е следната: теглото на веществата, които влизат в реакцията, е равно на теглото на веществата, които са получени в резултат на реакцията. 
В руската наука този постулат се нарича “Законът за опазване на масата на Ломоносовите вещества”.
Този закон е формулиран през 1748 г. и най-точните експерименти с реакцията на изгаряне на метали в запечатани съдове са извършени през 1756 година.
Експерименти с Лавуазие
Европейската наука откри закона за запазване на масата след публикуването на описанието на творбите на великия френски химик Антоан Лавуазие.  Този учен смело прилага теоретичните идеи и физическите методи на времето в своите експерименти, което му позволява да разработи химическа номенклатура и да създаде регистър на всички известни по това време химикали.
Този учен смело прилага теоретичните идеи и физическите методи на времето в своите експерименти, което му позволява да разработи химическа номенклатура и да създаде регистър на всички известни по това време химикали.
Чрез своите експерименти Лавоазие доказа, че в хода на всяка химична реакция се наблюдава законът за запазване на масата на веществата, влизащи в съединението. В допълнение, той разшири разпределението на закона за запазване на масата на всеки от елементите, които са участвали в реакцията като част от сложни вещества.
Ad
Така на въпроса кой е открил закона за запазване на масата на веществата, може да се отговори по два начина. М. В. Ломоносов е първият, който провежда експерименти, които ясно демонстрират закона на консервацията и го довеждат до теоретична основа. А. Лавуазие, през 1789 г., независимо от руския учен, самостоятелно открива закона за масовото съхранение и разширява принципа си до всички елементи, участващи в химическа реакция.
Маса и енергия
През 1905 г. великият А. Айнщайн показа връзката между масата на материята и нейната енергия. Тя беше изразена по формулата:
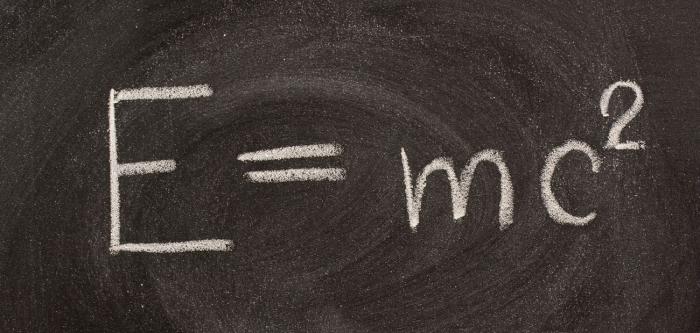
Уравнението на Айнщайн потвърждава закона за запазване на масата и енергията. Тази теория твърди, че всяка енергия има маса и промяната в тази енергия е промяна в телесната маса. Потенциална енергия всяко тяло е много голямо и може да се освободи само при специални условия.
Законът за запазване на масата е валиден за всички органи на микро- и макрокосмоса. Всяка химическа реакция е включена в превръщането вътрешна енергия вещества. Следователно, когато се изчислява масата на веществата, участващи в химични реакции, е необходимо да се вземе предвид увеличаването или намаляването на масата, причинена от освобождаването или абсорбцията на енергия в дадена реакция. Всъщност в макрокосмоса този ефект е толкова незначителен, че тези промени могат да бъдат пренебрегнати.