Азотен оксид: формула, свойства, приложение
Оксидите се наричат бинарни съединения на химични елементи с кислороден атом, в който степента на окисление е 2-. Азотът, който има по-ниска електронегативна стойност, образува различни комбинации с кислород. Тези съединения принадлежат към различни класове вещества. Азотният оксид съдържа кислород в количество, което определя валенцията на елемента N. Тя варира от 1 до 5.
Какви са оксидите
Има около дузина азотни съединения, съдържащи О-елемент. От тях петте най-често срещани са: моновалентен оксид, двувалентен оксид, тривалентен оксид, четиривалентен оксид и пентавалентен оксид. 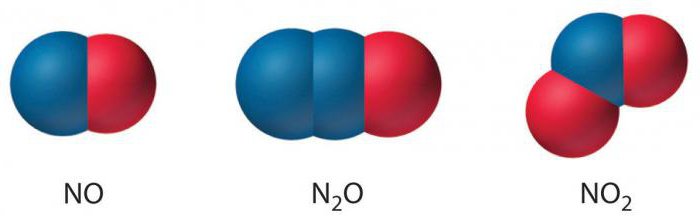
Останалите съединения се считат за по-рядко срещани. Те включват тетравалентен азотен оксид под формата на димер, нестабилни молекули на нитрилазид, нитрозил азид, тринитрамид и нитратен радикал.
Формули за азотни оксиди
По-долу са представени символите на най-важните съединения на елемента N.
Това е предимно азотен оксид, формулата на който се състои от два химически знака - N и O. След тях се поставят показатели, в зависимост от окислителни състояния атома.
- Моновалентният азотен оксид има формулата N2O. В него N атомът се зарежда +1.
- Азотният оксид има формула NO. В него N атомът е зареден +2.
- Азотният железен оксид има формулата N2O3. В него N атомът се зарежда +3.
- Тетравалентният азотен оксид, чиято формула е NO 2 , има заряд от N + 4 атом.
- Пентавалентно кислородно съединение се обозначава като N205. В него N атомът се зарежда +5.
Описание на моновалентния азотен оксид
Той се нарича също диазо, азотен оксид и газ за смях. Последното име произлиза от действието, свързано с интоксикация. 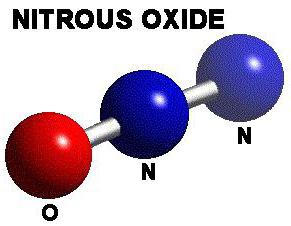
Азотният оксид с валентност I при нормални температурни условия съществува под формата на незапалим газ, без цвят, който показва приятен сладникав вкус и мирис. Въздухът е по-лек от това съединение. Оксидът е разтворим във водна среда, етанол, етери и сярна киселина.
Водните, алкалните и киселинните разтвори не могат да реагират с него, не образуват сол. Не подлежи на запалване, но е в състояние да поддържа процеса на горене.
Амониевият азотен оксид се превръща в азид (N3NH4).
Когато се комбинира с молекули етери, хлороетан и циклопропан, се образува експлозивна смес.
Нормалните условия допринасят за неговата инерция. Под действието на нагряването веществото се възстановява.
Описание на оксида на двувалентен азот
Нарича се още монооксиден, оксиден или нитрозилов радикал. При нормални температурни условия той е безцветен, незапалим газ, слабо разтворим във водна среда. Въздухът се окислява, оказва се NO 2. Неговата течна и твърда форма става синя. 
Азотният оксид може да бъде редуктор в реакциите на взаимодействие с халогени. Продуктът от тяхното добавяне е нитрозилхалогенид, който има формула NOBr.
Серен диоксид и други силни редуциращи агенти окисляват NO до образуване на N2 молекули.
Описание на железен оксид
Те се наричат азотен анхидрид. В нормално състояние може да бъде течност със син цвят, а стандартните параметри на средата превръщат оксида във вид на газ, който няма цвят. Притежава стабилност само при ниски температури.
N2O3 молекули се дисоциират по време на нагряване с освобождаването на моно- и двувалентен оксид.
Като анхидрид, той добавя вода за производството на азотиста киселина, а с алкали образува соли под формата на нитрити.
Описание на оксида с четиривалентен азот
По друг начин се нарича диоксид. Има кафяво-червен газ, който има остър мирис и може да бъде и жълтеникава течност. 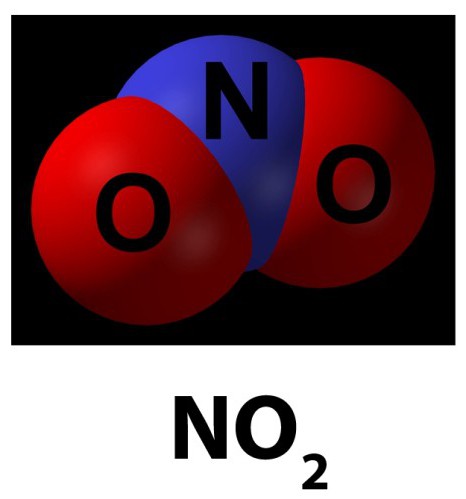
Отнася се за кисели оксиди, които имат добре развита химическа активност.
Нейните молекули окисляват неметалите с образуването на кислородсъдържащи съединения и свободен азот.
Диоксидът реагира с четиривалентен и шестивалентен серен оксид. Оказва се сярна киселина. Методът на неговия синтез се нарича азотен.
Азотният оксид може да се разтвори във водната среда. Азотна киселина е резултат от тази реакция. Този процес се нарича диспропорциониране. Междинният компонент се счита за азотна киселина, която бързо се разлага.
Ако се разтварят азот четиривалентен оксид в алкални, след това образуването на разтвори на нитрати и нитрити. Можете да използвате неговата течна форма, за да взаимодействате с метала, след което получавате безводна сол.
Описание на пентавалентен азотен оксид
Нарича се също като диазотичен пентоксид, нитрониев нитрат, нитрилен нитрат или азотен анхидрид. 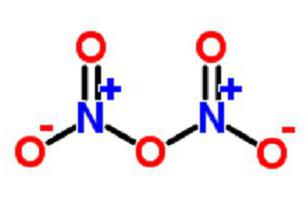
Той е под формата на безцветни кристали, които са летливи и нестабилни. Тяхната стабилност се наблюдава при ниски температури. Тази структура се формира от нитратни и нитритни йони.
В газообразна форма веществото е под формата на анхидрид NO 2 - O - NO 2 .
Пентавалентният азотен оксид има кисели свойства. Лесно се разлага с освобождаването на кислород.
Веществото реагира с вода, което води до азотна киселина.
Алкали разтварят анхидрида с освобождаването на соли на нитрати.
Как да получите азотни оксиди
N 2 O оксид се образува, когато се използва сух амониев нитрат в остро състояние, но този метод може да бъде придружен от експлозия.
Предпочитаният метод за получаване на моновалентен оксид е действието на азотна киселина в концентрирана форма върху сулфаминова киселина. Основното условие е отоплението.
Нитрозил, или NO, е специален азотен оксид, който се получава чрез взаимодействие на молекули N 2 и О2. Важно условие за този процес е силното нагряване над 1000 ° С.
Естественият метод за получаване, свързан с гръмоотводи в атмосферния въздух. Такъв оксид бързо се съчетава с кислородни молекули и се образува диоксид.
Лабораторният метод за синтез на NO е свързан с реакцията на метали и неконцентрирана азотна киселина. Пример за такава реакция е взаимодействието на мед с HNO3.
Друг метод за образуване на азотен монооксид е реакцията на железен хлорид с натриев нитрит и солна киселина. Резултатът от процеса е железното и натриевите хлориди, водата и самия оксид.
В промишлен мащаб, той се произвежда чрез окисляване на амонячни молекули по време на нагряване и под високо налягане. Ускорителят на процеса е платина или хром тривалентен оксид. 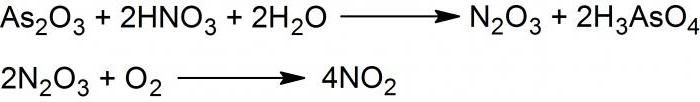
Диоксид или NO2 се получава чрез взаимодействие на арсена с тривалентен оксид с 50% азотна киселина, която се нанася на капки на повърхността на твърд реактив. Образува се смес от оксиди на двувалентен и четиривалентен азот.
Ако се охлади до температура от -30 ° С, тогава се синтезира азотен анхидрид или N2O3.
В прахообразна форма се получава при преминаване на електрически ток през неговата газообразна форма.
Ако на нишестения прах се действа с азотна киселина с концентрация 50%, оксидът на двувалентен и четиривалентен азот, газ въглероден диоксид и вода се освобождават. След това, от първите две получени съединения, се образува молекулата на N2O3.
В резултат на термичния разпад на съединението с нитроводно вещество, азотен диоксид, свободен кислород и оловен оксид.
Анхидрид, или N 2 O 5, се образува поради елиминирането на водната молекула от киселина чрез азотно действие фосфорен оксид петвалентен.
Друг начин за синтезиране е преминаването на сух хлор чрез безводен сребърен нитрат.
Ако азотният диоксид се въздейства от озоновите молекули, се образува N 2 O 5 .