Йони са заредени атоми и атомни групи. Концепцията за йонни реакции и зареждане на йони
За първи път терминът "йон" е въведен през 1834 г., в който заслугата на Майкъл Фарадей. След проучване на влиянието на електрическия ток върху разтворите на соли, основи и киселини, той стига до заключението, че те съдържат частици, които имат определен заряд. Фарадееви катиони, наречени йони, които в електрическо поле се движат към катода, който има отрицателен заряд. Аниони са отрицателно заредени неелементарни йонни частици, които в електрическо поле се движат към плюс-анод.
Тази терминология се използва сега и частиците се изучават по-нататък, което ни позволява да разгледаме химическа реакция в резултат на електростатично взаимодействие. Много реакции протичат съгласно този принцип, което прави възможно да се разбере техния курс и да се изберат катализатори и инхибитори, за да се ускори протичането им и да се инхибира синтеза. Също така стана известно, че много вещества, особено в разтвори, винаги са под формата на йони.
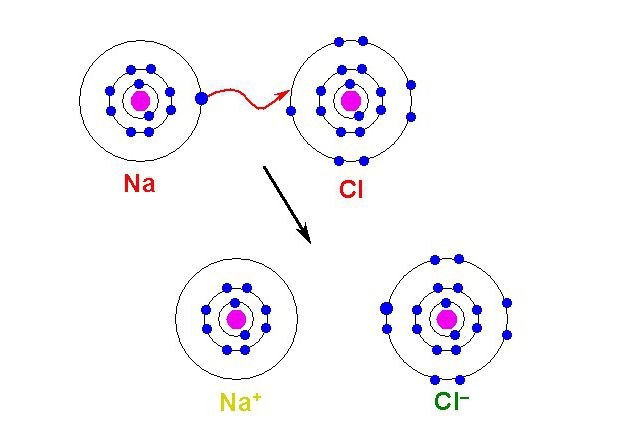
Номенклатура и класификация на йони
Йони са заредени атоми или група от атоми, които са загубили или придобили електрони по време на химическа реакция. Те съставляват външните слоеве на атома и могат да бъдат загубени поради ниската сила на гравитацията на ядрото. Тогава резултатът от отделянето на електрона е положителен йон. Също така, ако един атом има силен ядрен заряд и тясна електронна обвивка, ядрото е акцептор на допълнителни електрони. В резултат се образува отрицателна йонна частица.
Самите йони не са само атоми с излишък или недостатъчна електронна обвивка. Тя може да бъде група от атоми. В природата най-често има точно групирани йони, които присъстват в разтвори, биологични течности на организми и в морска вода. Има огромен брой видове йони, чиито имена са доста традиционни. Катионите са йонни частици, които са положително заредени, а отрицателно заредените йони са аниони. В зависимост от състава те се наричат различно. Например, натриев катион, цезиев катион и други. Анионите се наричат по различен начин, тъй като най-често се състоят от много атоми: сулфатен анион, ортофосфатен анион и други.
Механизъм за образуване на йони
Химичните елементи в съединенията рядко са електрически неутрални. Това означава, че те почти никога не са в състояние на атоми. В образованието ковалентна връзка, които се считат за най-често срещаните, атомите също имат определен заряд, а електронната плътност се измества по протежение на връзките вътре в молекулата. Тук обаче не се образува йонният заряд, тъй като енергията на ковалентната връзка е по-малка от енергията на йонизация. Следователно, въпреки различната електронегативност, някои атоми не могат напълно да привлекат електрони от външния слой на другите.
В йонните реакции, където разликата в електронегативността между атомите е достатъчно голяма, един атом може да вземе електроните на външния слой от друг атом. Тогава създадената връзка е силно поляризирана и счупена. Енергията, изразходвана за това, която създава йонно зареждане, се нарича йонизационна енергия. За всеки атом той е различен и е посочен в стандартните таблици.
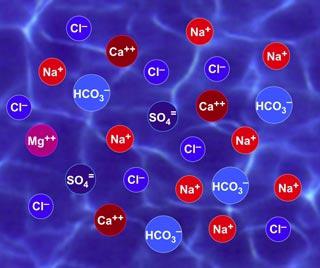
Йонизацията е възможна само в случаите, когато атом или група атоми са способни или да дарят електрони, или да ги приемат. Най-често това се наблюдава в разтвора и кристалите на солта. Кристалната решетка съдържа почти неподвижни заредени частици, лишени от кинетична енергия. И тъй като няма възможност за движение в кристала, реакцията на йони се среща най-често в разтвори.
Йони по физика и химия
Физиците и химиците активно изучават йони по няколко причини. Първо, тези частици присъстват във всички известни агрегатни състояния на материята. Второ, енергията на разделяне на електроните от атома може да бъде измерена, за да се използва в практическите дейности. Трето, в кристалите и разтворите йони се държат по различен начин. И четвърто, йони позволяват да се провежда електрически ток, а физикохимичните свойства на разтворите варират в зависимост от концентрациите на йони.
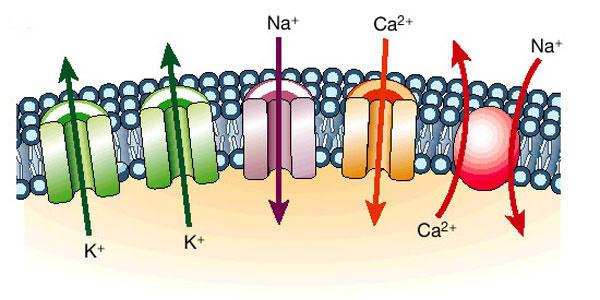
Йонни реакции в разтвор
Самите решения и кристали трябва да се разглеждат по-подробно. В кристалите на соли има отделно разположени положителни йони, например натриеви катиони и отрицателни хлорни аниони. Кристалната структура е невероятна: благодарение на силите на електростатично привличане и отблъскване, йоните са ориентирани по специален начин. В случай на натриев хлорид те образуват така наречената кристална решетка от диамант. Тук всеки натриев катион е заобиколен от 6 хлоридни аниона. От своя страна всеки хлориден анион обгражда 6 хлорни аниони. Поради това е просто сол а в студена и топла вода се разтваря почти със същата скорост.

В разтвора също така няма твърда молекула натриев хлорид. Всяка от йените тук е заобиколена от диполи вода и хаотично се движи в дебелината си. Наличието на заряди и електростатични взаимодействия води до факта, че солните водни разтвори се замразяват при температура, малко по-малка от нула, и се вари при температура над 100 градуса. Освен това, ако има други вещества в разтвора, които могат да влязат в химическа връзка, тогава реакцията не се проявява с участието на молекули, а на йони. Това създаде доктрината за организирането на химическа реакция.
Тези продукти, които са получени в края, не се образуват веднага по време на взаимодействието, а постепенно се синтезират от междинни продукти. Изследването на йони направи възможно да се разбере, че реакцията протича точно съгласно принципите на електростатичните взаимодействия. Резултатът им е синтез на йони, които електростатично взаимодействат с други йони, създавайки крайния равновесен реакционен продукт.
резюме
Такава частица като йон е електрически зареден атом или група от атоми, която се получава по време на загубата или придобиването на електрони. Най-простият йон е водород: ако загуби един електрон, той е само ядро с такса +1. Той причинява киселата среда на разтвори и среди, която е важна за функционирането на биологичните системи и организми.
Йони могат да имат както положителни, така и отрицателни заряди. Поради това, в разтворите всяка частица влиза в електростатично взаимодействие с диполите на водата, което също създава условия за живот и предаване на сигнала от клетките. Освен това, в йонната технология се развива по-нататък. Например, създадени са йонни двигатели, които вече са оборудвали 7 космически мисии на НАСА.