Химични свойства на алкалоземните метали. Списък на алкалоземните метали
Втората група на периодичната система на Д. И. Менделеев съдържа група от елементи, които са много сходни по своите свойства алкални метали те обаче са по-нисши в дейността си. Съдържа берилий и магнезий, както и калций, стронций, барий и радий. Те са известни под общото наименование - алкалоземни елементи. В нашата статия ще се запознаем с тяхното разпределение в природата и приложението в индустрията, а също така ще проучим основните химични свойства на алкалоземните метали.

Общи характеристики
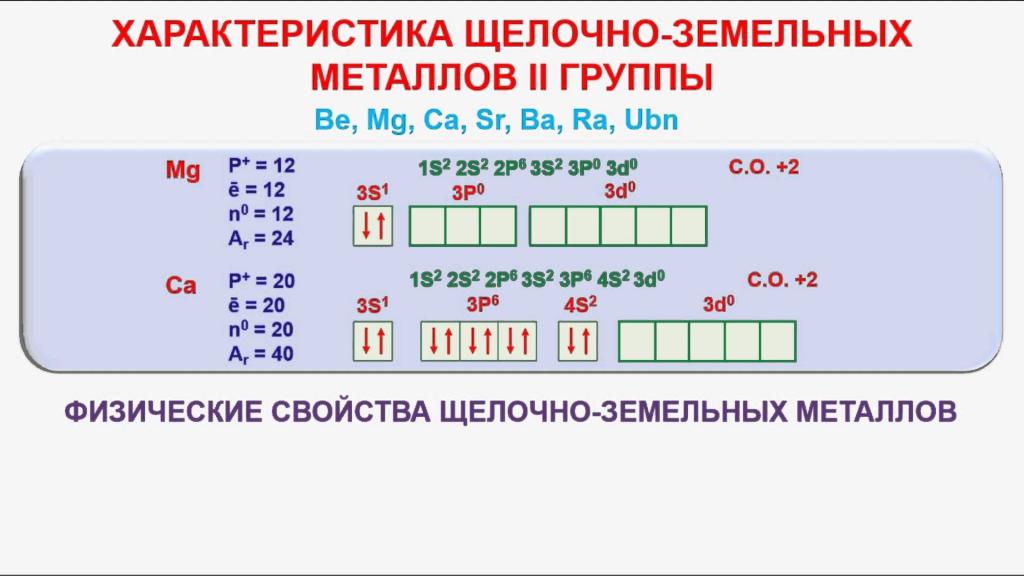
Всички атоми над изброените елементи съдържат два електрона във външния енергиен слой. Взаимодействайки с други вещества, те винаги се отказват от отрицателните си частици, преминавайки в състояние на катиони с такса от 2+. При редокс реакциите, елементите се държат като силни редуциращи агенти. С увеличаването на ядрения заряд се повишават химичните свойства на алкалоземните метали и тяхната активност. Те бързо се окисляват във въздуха, образувайки оксиден филм на повърхността им. Общата формула за всички оксиди е RO. Те съответстват на хидроксиди с формула R (OH) 2 . Техните основни свойства и разтворимост във вода също се увеличават с увеличаване на серийния номер на елемента.
Специални свойства на берилий и магнезий
В някои от техните свойства първите двама представители на основната подгрупа на втората група се различават донякъде от другите алкалоземни елементи. Това се проявява по-специално по време на взаимодействието им с вода. Например, химичните свойства на берилия са такива, че той изобщо не реагира с Н2О. Магнезият взаимодейства с вода само при нагряване. Но всички алкалоземни елементи лесно реагират с нея при обикновена температура. Какви вещества се образуват едновременно?

Основи на алкалоземни метали
Калций, барий и други членове на групата бързо заместват водород от вода, което води до получаването на хидроксиди. Взаимодействието на алкалоземни метали с вода протича бързо, с отделяне на топлина. Разтвори на основи на калций, барий, стронций, успокояващи при допир, когато влязат в контакт с кожата и лигавицата на очите, причиняват тежки изгаряния. Първата помощ в такива случаи ще бъде третирането на раната на повърхността със слаб разтвор на оцетна киселина. Неутрализира алкалите и намалява риска от некроза на увредените тъкани.
Химични свойства на алкалоземните метали
Взаимодействието с кислород, вода и неметали е основният списък на свойствата на металите, включени във втората група на периодичната система от химични елементи. Например, калций дори при нормални условия реагира с халогени: флуор, хлор, бром и йод. При нагряване се комбинира със сяра, въглерод и азот. Твърдата оксидация - изгаряне, завършва с образуването калциев оксид: 2Ca + O2 = 2 CaO. Взаимодействието на метали с водород води до появата на хидриди. Те са бели огнеупорни вещества с йонни кристални решетки. Важните химични свойства на алкалоземните метали включват тяхното взаимодействие с вода. Както беше споменато по-рано, продуктът от тази заместваща реакция е метален хидроксид. Имайте предвид също, че в основната подгрупа на втората група калций заема най-значимото място. Ето защо, ние се спираме на неговите характеристики по-подробно.
Калций и неговите съединения
Съдържанието на елемента в земната кора е до 3,5%, което показва широкото му разпространение в състава на такива минерали като варовик, креда, мрамор и калцит. Съставът на естествения калций включва шест вида изотопи. Намира се и в естествени водоизточници. Съединенията на алкални метали се изучават подробно в хода на неорганичната химия. Например, в клас 9, учениците ще научат, че калцийът е лек, но силен сребристо-бял метал. Неговите точки на топене и кипене са по-високи от тези на алкалните елементи. Основният метод за получаване - електролизата на смес от разтопени соли на хлорид и калциев флуорид. Основните химични свойства са неговите реакции с кислород, вода и неметали. От съединенията на алкалните метали, оксид и калций са най-важни за промишлеността. Първото съединение се получава от креда или варовик чрез изгарянето им.

Освен това, калциев хидроксид се образува от калциев оксид и вода. Неговата смес с пясък и вода се нарича строителен разтвор. Продължава да се използва като мазилка и за свързване на тухли при полагане на стени. Разтвор на калциев хидроксид, наречен вода от вар, се използва като реагент за откриване на въглероден диоксид. При преминаване на въглероден диоксид през бистър воден разтвор на Са (ОН) 2 , неговата мътност се наблюдава поради образуването на неразтворима утайка. калциев карбонат.
Магнезий и неговите характеристики
Химията на алкалоземните метали изследва свойствата на магнезий, като се фокусира върху някои от неговите характеристики. Това е много лек, сребрист бял метал. Магнезият, разтопен в атмосфера с висока влажност, активно поглъща водородни молекули от водни пари. Охлаждайки се, металът почти напълно ги освобождава обратно във въздуха. Той реагира много бавно с вода, поради образуването на слабо разтворимо съединение, магнезиев хидроксид. Алкалите изобщо не действат на магнезий. Металът не реагира с някои киселини: концентриран сулфат и флуороводородна, поради пасивацията и образуването на защитен филм на повърхността. Повечето минерални киселини разтварят метала, който е съпроводен с бързо освобождаване на водород. Магнезият е силен редуциращ агент, който замества много метали от техните оксиди или соли:
BeO + Mg = MgO + Be.
Металът заедно с берилий, манган, алуминий се използва като легиращ агент за стомана. Особено ценни свойства са магнезиеви сплави - електрони. Използват се в авиационното и автомобилното производство, както и в детайлите на оптичните технологии.
Ролята на елементите в жизнената активност на организмите
Да дадем примери за алкалоземни метали, съединенията от които са обичайни в дивата природа. Магнезият е централен атом в молекулите на хлорофила в растенията. Той участва в процеса на фотосинтеза и е част от активните центрове на зеления пигмент. Магнезиевите атоми фиксират светлинната енергия, превръщайки я в енергия от химически връзки на органични съединения: глюкоза, аминокиселини, глицерин и мастни киселини. Важна роля играе елементът като необходим компонент на ензимите, които регулират метаболизма в човешкото тяло. Калцият е макроелемент, който осигурява ефективно преминаване на електрически импулси през нервната тъкан. Наличието на неговите фосфатни соли в състава на костите и зъбния емайл им придава твърдост и здравина.
Берилий и неговите свойства
Алкалоземните метали също включват берилий, барий и стронций. Помислете за берилий. Елементът не е широко разпространен в природата, основно се намира в състава на минералите, например, берил. Неговите разновидности, съдържащи многоцветни примеси, образуват скъпоценни камъни: изумруди и аквамарини. Особеност на физическите свойства е крехкостта и високата твърдост. Отличителна черта на един атом на елемент е наличието на второ външно енергийно ниво не осем, както при всички други алкалоземни метали, а само два електрона.

Следователно радиусът на атома и йона е непропорционално малък, йонизационната енергия е голяма. Това води до висока якост. кристална решетка метал. Химичните свойства на берилия също го отличават от другите елементи от втората група. Реагира не само с киселини, но и с алкални разтвори, като измества водород и образува хидроксиберилати:
Be + 2NaOH + 2H2O = Na2 [Be (OH) 4 ] + H2.
Металът има редица уникални характеристики. Благодарение на възможността за пропускане на рентгенови лъчи, той се използва за производството на прозорци с рентгенови тръби. В ядрената промишленост елементът се счита за най-добрия модератор и рефлектор на неутроните. В металургията се използва като ценна легираща добавка, която повишава антикорозионните свойства на сплавите.
Стронций и барий
Елементите са доста често срещани в природата и, точно като магнезий от алкалоземни метали, са част от минералите. Нека ги наречем: барит, селестин, стронций. Барият има вид на пластмасов метал със сребристо-бял цвят. Подобно на калция, той е представен от няколко изотопа. Във въздуха тя активно взаимодейства със своите компоненти - кислород и азот - за да образува бариев оксид и нитрид. Поради тази причина металът се съхранява под слой от парафин или минерално масло, избягвайки контакта му с въздуха. И двата метала образуват пероксиди при нагряване до 500 ° С.

От тях бариевият пероксид, използван като тъканно белина, има практическо приложение. Химичните свойства на алкалоземните метали, бария и стронция са подобни на свойствата на калция. Въпреки това, тяхното взаимодействие с водата е много по-активно и получените бази са по-силни от калциевия хидроксид. Барийът се използва като добавка към охлаждащи течности за течни метали, като намалява корозията в оптиката при производството на вакуумни електронни устройства. Стронций се търси в производството на фотоволтаични клетки и фосфори.
Качествени реакции като се използват йони на алкалоземни метали
Бариевите и стронциевите съединения са примери за алкалоземни метали, които се използват широко в пиротехниката поради тяхното ярко оцветяване на пламъка с йони. По този начин, стронциевият сулфат или карбонат дава карминово-червен блясък на пламъка, а съответните бариеви съединения дават жълто-зелено. За откриване на калциеви йони в лабораторията върху пламъка на горелката се изливат няколко пелети от калциев хлорид, пламъкът се оцветява в тухлено-червен цвят.

Разтвор на бариев хлорид се използва в аналитичната химия за откриване на киселинния остатък на сулфатната киселина в разтвора. Ако при изсипването на разтворите се образува бяла утайка от бариев сулфат, това означава, че в него има SO 2 2- частици.
В нашата статия изследвахме свойствата на алкалоземните метали и дадохме примери за тяхното приложение в различни индустрии.