Видове химични реакции. Класификация на химичните реакции
Концепцията за това какви видове химични реакции са неразривно свързани с основните познания по предмета, които задължително се преподават в училище. За разлика от физическата метаморфоза, в химията има трансформация на вещество от едно или няколко към друго или няколко други. Почти всички видове химични реакции се основават на това.
Химични реакционни фактори
До момента са идентифицирани достатъчно голям брой реакции, които по един или друг начин принадлежат към областта на химията и физиката. Класификацията на химичните реакции обаче е такава, че те могат да бъдат преценени по някои основни характеристики. Най-често това са признаци на визуален характер.

Например, най-лесният начин да се определи дали е извършена химическа реакция или не, е промяната в цвета на вещество или разтвор, утаяване, отделяне на газ и др. Всичко това не е трудно да се забележи, както се казва, дори и с око. В някои случаи този метод не работи. По-специално, това се отнася за течни реагенти като киселини и основи, когато се разтварят във вода. Въпреки че този процес е свързан изцяло с физически процеси, въпреки това хидратирането или хидролизата се разглеждат именно от гледна точка на науката като химията. Химични реакции определя се чрез допълнителни средства. Например, ако определите рН на разтвора, тук няма да видите нищо визуално. За обозначаване се използват решения лакмусова хартия който е боядисан в определен цвят в зависимост от киселинността на средата.

Определението обаче не се ограничава само до визуални ефекти. Това може да бъде потвърдено от други не по-малко забележими фактори, които се появяват по време на курса или края на процеса. И много от тях.
Също толкова интересна особеност е повишаване на температурата или пожар в фугата. Достатъчно е да си припомните училищните преживявания, когато парче калий се изхвърля във водата, след което се освобождава водород. Ако вземете достатъчно голямо парче от този метал и правилното количество вода, можете дори да постигнете факта, че просто ще се случи експлозия от невероятна сила. Имайте предвид, че такива случаи в историята, за съжаление, не са уникални.

Основни видове химични реакции
Що се отнася до това кои видове химични реакции могат да бъдат разграничени на настоящия етап от развитието на химията, тук може да се спомене за начало, че процесите могат първоначално и условно да бъдат разделени на хомогенни и хетерогенни. Хомогенните процеси протичат в една и съща фаза (например течна), а хетерогенните реакции използват няколко състояния на вещество (течност, твърдо вещество, газ и др.) Като основни реагенти.
Но такова разделение на видовете химични процеси далеч не е уникално, тъй като тук е необходимо да се вземе предвид точно преобразуването на веществата, участващи в реакцията, от едно към друго.
Същите алхимици се опитаха веднъж да получат злато от олово. Всъщност този процес може да се отдаде на химията по-скоро косвено.

Всъщност, превръщането на един елемент в друг принадлежи по-скоро на областта на ядрената физика. Днес е възможно да се произведе такъв процес, но полученото по този начин злато става много силно радиоактивно, изключително скъпо и просто е неподходящо за употреба.
Въпреки това, в основното разбиране на разделението на класове на химични реакции е да се разграничат най-често срещаните видове. В основата са взети четири основни класа: реакция на съединението, разлагане, заместване и йонен обмен. Има и пети тип, който по своята същност не се вписва в нито един от изброените по-горе класове. Това са окислително-редукционни реакции, при които, като правило, калиев перманганат (KMnO 4 ) действа като основен реагент, който, заедно с киселините, се счита за един от най-мощните окислителни агенти, известни на човечеството.

Реакции на съединението
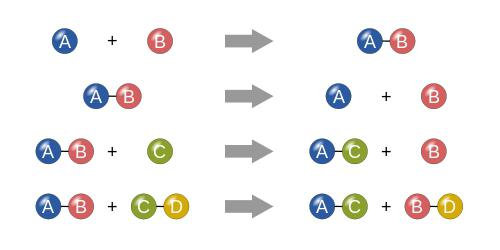
Ако говорим за условията на този вид химични реакции, условно самият процес може да бъде представен като вид математически израз. Да предположим, че имаме две вещества. Обикновено ги обозначаваме като “А” и “В”. В този случай реакцията ще има следната формула:
A + B = AB
Както вече е ясно, има просто сливане на двата компонента (независимо дали става въпрос за прости или сложни вещества, които са съединения).
Най-простият пример е образуването на оксиди. Например:
S + O2 = S02
Реакции на разлагане
Всъщност класификацията на химичните реакции е невъзможна без разбиране на процесите на разлагане. Въз основа на горния пример, самият процес може да бъде представен като формула:
X = AB - A - B ,
където АВ е първоначалното вещество, а А и В са съставките, в които ще се разложи. Съответно, X е резултатът, представляващ два компонента А и В, които в края на реакцията не реагират един с друг.
Реакции на заместване
Условията на химичните реакции със заместването също имат свои характеристики. На базата на проста математика, този тип процес може да бъде описан със следния пример:
Да предположим, че имаме определено съединение под формата на два компонента “AB” и определено вещество “C”. В тази връзка реакцията на заместване ще бъде:
AB + C = AC + B или AB + C = BC + A.
С други думи, възниква обичайното заместване на един или няколко компонента за друг.
Реакции за обмен на йони
Скоростта на химичната реакция най-добре се илюстрира от примера на реакциите на йонообмен, когато реагентите се обменят с йони (заредени частици). В този случай тя може да бъде максимална, тъй като превръщането на едно вещество в друго се случва на молекулярно ниво. В математическия израз тази формула има формата:
AB + CD = AD + CB (или в други варианти).
По същество реакциите на йонообмен са донякъде подобни на реакциите на заместване, въпреки че принадлежат към отделен клас.
Редокс реакции
Що се отнася до реакциите от този тип, те са сред всички известни най-сложни (да не говорим за реакциите на синтез). Факт е, че дори правенето на обикновено химическо уравнение, включващо калиев перманганат без специални познания, просто няма да работи. Тук е необходимо да се вземе предвид не само валентността на всеки начален компонент, но и валентността, която компонентите придобиват след края на процеса. В повечето случаи валентността може да варира в доста широки граници, а резултатът от реакцията на двата първоначални компонента може да бъде образуването на три или четири съединения.
Фактори, влияещи върху скоростта на химичните реакции
Самата скорост на химическата реакция зависи от способността на реагентите да влязат в процеса, както и от някои допълнителни условия, като температура. Най-простият пример е използването на катализатор - вещество, способно да ускори химическа реакция. Например, за да се забави в някои случаи, могат да се използват вещества като инхибитори, адсорбенти, абсорбенти и т.н. Всяко такова вещество може да има значително въздействие върху целия химичен процес и неговата скорост на потока.
Сред веществата от този тип обикновен човек е запознат с активен въглен, който е в състояние да абсорбира киселини или основи, в зависимост от средата, в която се намира.

заключение
Както виждате, видовете химически реакции, които един обикновен човек може да разбере, са доста прости. Най-важното в този въпрос е ясно да се изясни какво е процес. Забележете, в този случай, разглеждахме химически процеси, базирани на проста математика, без да навлизаме в подробности за химията. Изглежда, че този подход ще помогне да се обясни същността на основните химически процеси, така да се каже, “на пръстите”. Освен това, от гледна точка на математиката, всеки ще може да разбере какво представлява един конкретен процес.
В този случай не се разглеждат химични реакции и системи, в които взаимодействат повече от два реагента. За да ги разберете, трябва да имате определени знания. Само с тях ще бъде възможно да се направи същото уравнение, описващо този процес, да не говорим за органичната химия, където, за да се разбере какво е веществото, човек дори трябва да приложи структурни формули, например, базирани на бензеновия пръстен или свързаните радикали.
В този случай трябва да се отдръпнете от обичайните основи неорганична химия който описва повечето от процесите най-просто и сбито. Това е вярно, защото в зората на развитието на самата биологична наука никой не е имал представа, но резултатите от откритията и много изследвания просто учудват.