Структурната формула на нитробензола
Нитро съединенията са незаменими в синтеза на различни азо багрила, както и в производството на пиротехнически и експлозивни продукти. По-специално, нитробензенът, чиято формула е дадена по-долу, се използва като основен реагент в повечето подобни отрасли, тъй като характеристиките на неговата химична природа определят значението на използването на този прост представител на нитроарените.
Структура на връзката
В химията, нитробензоловата формула е изобразена като ароматен пръстен, към който е прикрепена нитрогрупа, която има изразени електро-акцепторни свойства. Нитрониевият йон NO2 + лишава съединението от способността за по-нататъшно електрофилно заместване. Този заместител разгражда електронната плътност на ароматния пръстен в структурната формула на нитробензола към себе си (пример 1), като по този начин го прави малко реактивен към подобни реакции, включително синтеза от Friedel-Crafts.
Ad
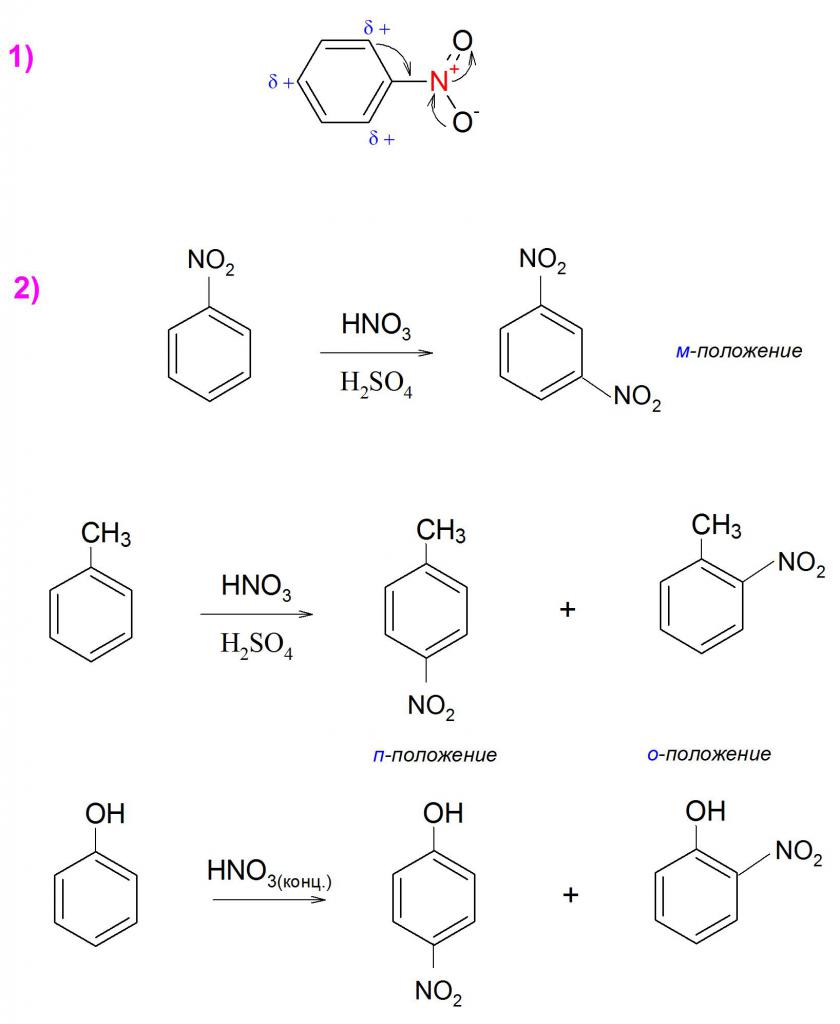
Тази особеност се изразява също така и в невъзможността за лесно полинизиране на такива съединения, поради което са необходими преки условия и допълнителни средства, като например високи температури или катализатори, за директното производство на динитро и тринитробензени. Обаче, присъствието на всякакви електронно-донорни заместители в молекулата, като метиловата или хидроксилна група, улеснява не само реакциите на прибавяне, но и улеснява по-простото нуклеофилно заместване. Тази функция обяснява същото ottyagirovanie плътност на пръстена, само в този случай, той се разпределя между ориентанти според силата на техните индуктивни и мезомерни ефекти.
Характеристики заместник
Тъй като -NO 2 е 2-ри вид ориентант, неговият дезактивиращ ефект върху ароматния пръстен води до дефиниране на заместители, главно в мета позиция. Но при получаване на нитро производни, например, толуен или фенол, -N02 става в орто- или пара-позиции, тъй като тези заместители определят мястото на нитрогрупата в съединението (пример 2) чрез добавяне на електронна плътност (мезомерен ефект). Казано по-просто, наличието на първокласни ориентанти регулира определянето на -N02 в химичната формула на нитробензола е по-силно от присъствието на групи от втори вид.
Ad
Получаване на нитробензен
Получаването на това вещество в промишлеността се извършва чрез директно нитриране на бензол със смес от сярна (H 2 SO 4 ) и азотна (HNO 3 ) киселина с добив от 96 до 99% (пример 3). Рядко в лабораторни условия формулата на нитробензола се синтезира чрез заместване или модифициране на съществуващи групи, тъй като добивът в такива реакции е много нисък и самият процес изисква специални условия.
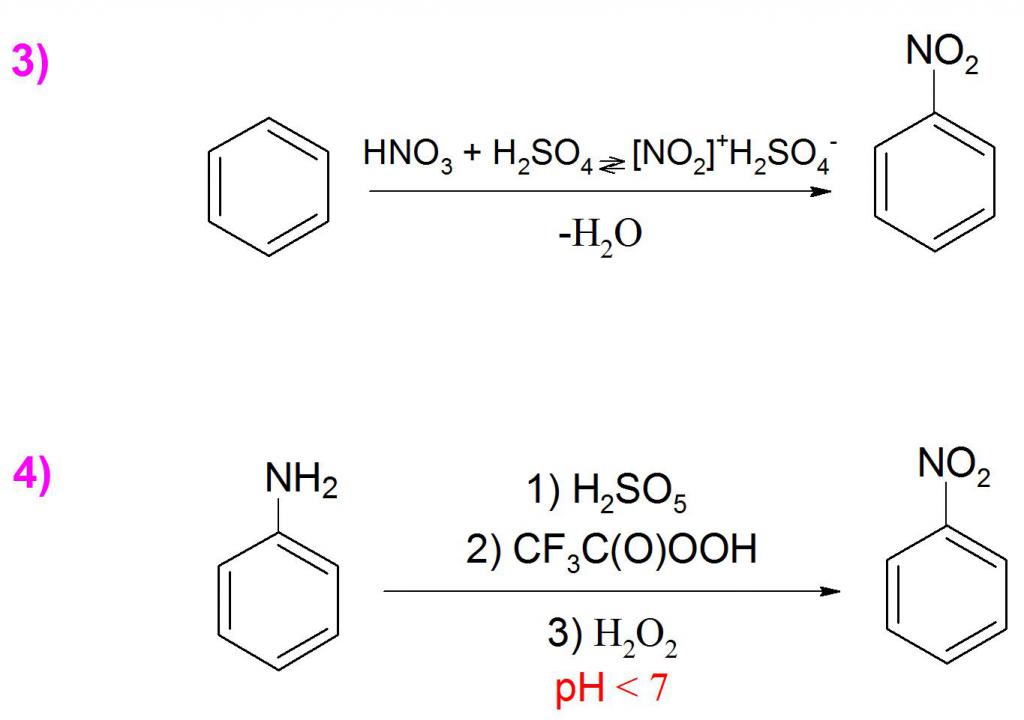
Друг метод за получаване е окисляването на анилин чрез перокси съединения, например, пероксисулфонова киселина (H2SO5) или перокситрифлуорооцетна киселина (CF3C (0) OOH), и също водороден пероксид (H202). Тази реакция изисква мониторинг на рН на средата, тъй като в алкалната среда се образува предимно азоксибензен (пример 4).
Физични свойства
Нитробензолът е мазна течност, неразтворима във вода, със специфичен мирис на горчиви бадеми и много токсичен за хората. Въпреки това, той е силно разтворим в органични разтворители като бензен и диетилов етер. В случай на директен препарат от бензен, той се отделя от нереагиралата смес чрез парна дестилация.
Ad
Взаимодействие с електрофилни реагенти
Както беше споменато по-горе, наличието на нитрогрупа в състава на нитробензеновата формула прави съединението по-малко реактивно към електрофилно заместване, но процесът на по-нататъшно нитриране може да продължи да се извършва под действието на силни киселини и високи температури.
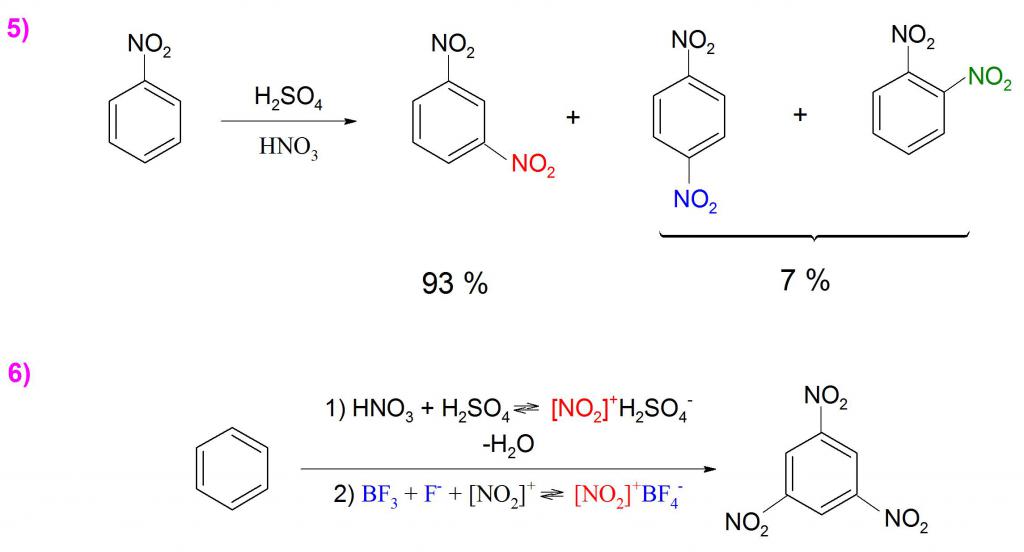
За да се получи динитробензен, в допълнение към използването на нитрираща смес (H2S04 + HNO3), се изисква значителен термичен ефект, но процесът е много труден и в резултат се получава смес от голямо количество мета-нитро съединение и незначителни фракции на орто и пара производни (Пример 5). ).
Тринитробензолът не се образува чрез директно нитриране, но като се използва борен трифлуорид (BF 3 ) и смеси от концентриран H 2 SO 4 и HNO 3 се получава с доста добър добив (пример 6).
Нуклеофилно заместване
Според формулата на нитробензола, може да се прецени, че само по себе си има слаби акцепторни свойства, следователно може да взаимодейства само с много силни електродонорни вещества. Най-често реагентите действат върху нитрогрупата, за да образуват азокси и азо съединения, но чрез избиране на правилните окислителни агенти може да се получи малък добив от фенолни производни. Пример за това е синтеза на нитрофенолови изомери чрез директно въвеждане на хидроксилна група в ароматен пръстен (Пример 7). Такива реакции протичат бавно и изискват много тежки условия.
Ad
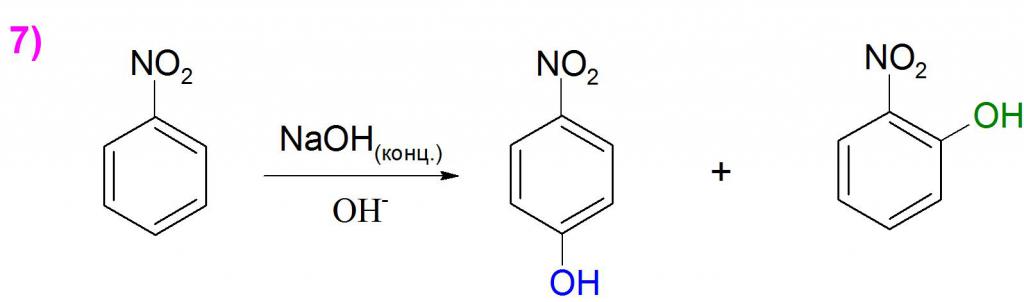
С увеличаването на броя на нитрогрупите тези съединения проявяват много по-силни акцепторни свойства, което улеснява реакцията със слаби нуклеофилни и основни реагенти.
Ролята на нитробензеновата структура в производството на първични амини
Нитро групата е заместител, който може да бъде редуциран до различни продукти в кисела, неутрална и алкална среда. Целият процес на възстановяване на структурната формула на нитробензола към първичния амин може да бъде представен като многостепенен процес.
На първо място, при добавянето на 2 водородни атома се образува нитрозобензен, който е трудно да се изолира в чиста форма (Фиг. 1А).
Следващият етап на възстановяване е да се получи арилхидроксиламин, който в кисела среда (рН <6) лесно се превръща в анилин (фиг. 1В). Възможно е също, че вторичното прегрупиране на това междинно съединение се среща в аминофеноли (Фиг. 1В). В чиста форма арилхидроксиламинът се получава чрез регулиране на стойностите на рН до неутрални стойности.
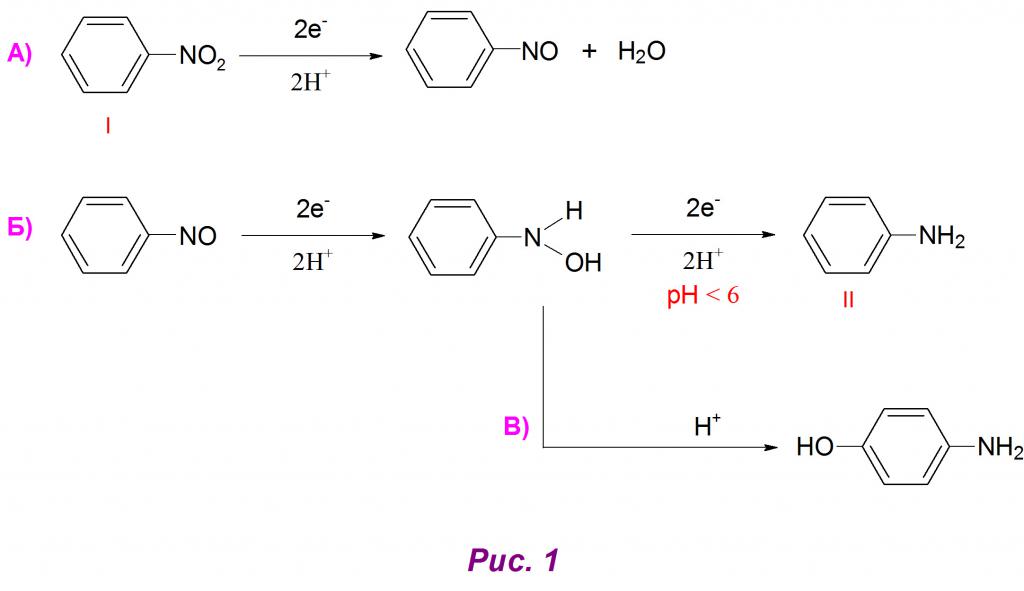
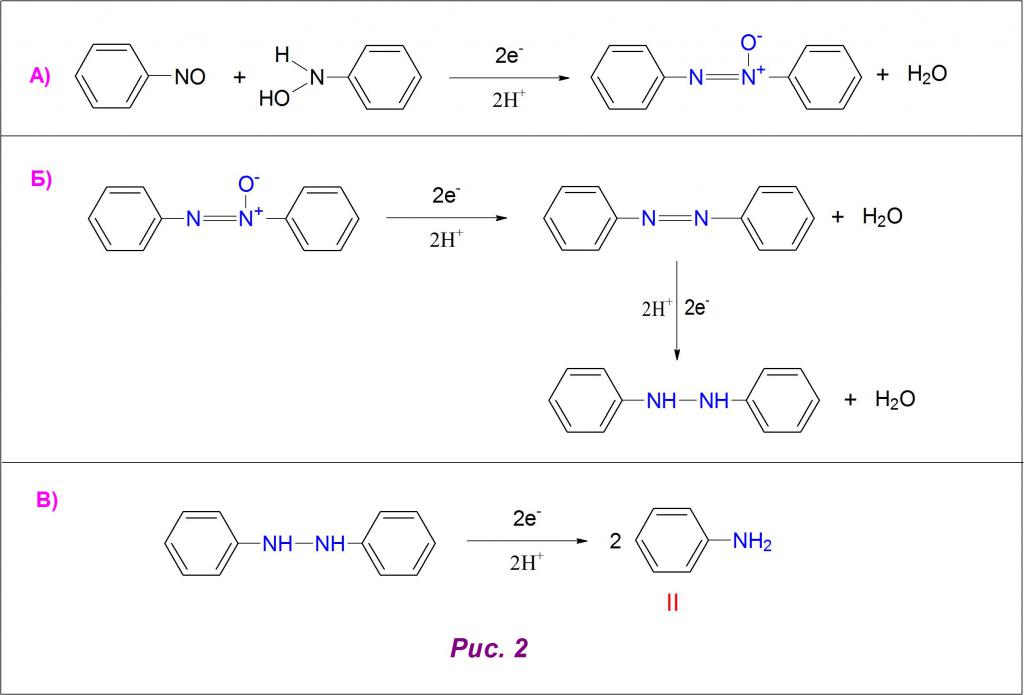
Алкалната среда (рН> 8) влияе върху хода на реакцията с образуването на азокси и азо съединения като кондензационни продукти на арилхидроксиламин и нитрособензен, като последната се възстановява много бавно при тези условия. Полученият азоксибензен при подкисляване дава азо-производно (Фиг. 2А) и то от своя страна реагира с водородни атоми за образуване на хидразо съединение (Фиг. 2В).
Когато последното се възстанови, се получава готов ариламин (фиг. 2В). Структурни формули нитробензен и анилин са представени под римски цифри I и II на фигури 1 и 2.
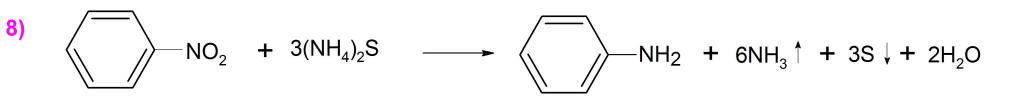
Zinin реакция
През 1842 г. руският учен Зинин Н.Н. синтезиран от нитробензен анилин формула чрез редукция на първия амониев сулфид ((NH4) 2S) (пример 8).
С течение на времето ученият потвърди възможността за използване на реакцията при приготвянето на ароматни амини от други нитросъединения, което позволи да се развие широкомащабно производство на синтетични багрила, експлозиви, както и специални фармацевтични препарати.