Концепцията, свойствата и заряда на електрона
Електронът е елементарна частица, която е една от основните единици в структурата на веществото. Зарядът на електрони е отрицателен. Най-точните измервания са направени в началото на ХХ век от Milliken и Ioffe.
Зарядът на електрона е минус 1.602176487 (40) * 10 -1 9 Cl.
Чрез тази стойност се измерва електрически заряд други малки частици.

Обща концепция за електрон
При физиката на елементарните частици се казва, че един електрон е неделим и неструктуриран. Участва в електромагнитни и гравитационни процеси, принадлежи към лептоновата група, както и към нейната античастица - позитрон. Сред другите лептони има най-лекото тегло. Ако електроните и позитроните се сблъскат, това води до тяхното унищожаване. Такава двойка може да възникне от гама-квантови частици.
Преди да бъдат измерени неутрино, именно електронът се счита за най-леката частица. В квантовата механика тя се нарича фермиони. Също така, електронът има магнитен момент. Ако позитронът също се позовава на него, то позитронът се разделя като положително заредена частица, а електронът се нарича негатрон, като частица с отрицателен заряд.
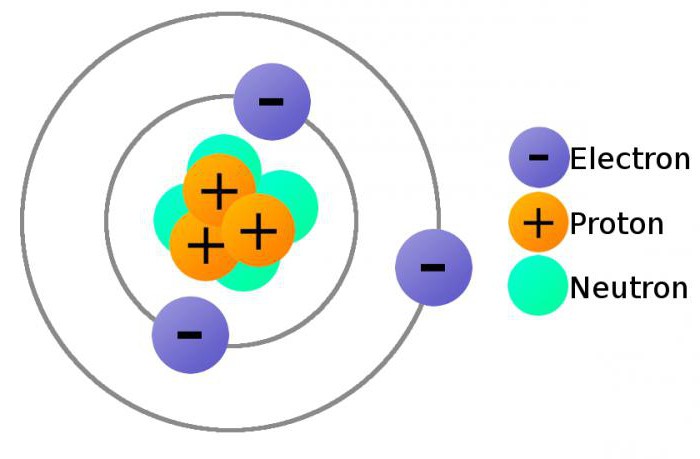
Отделни свойства на електроните
Електроните принадлежат към първото поколение лептони с свойствата на частиците и вълните. Всеки от тях е снабден с квантово състояние, което се определя чрез измерване на енергията, ориентацията на спина и други параметри. Принадлежността към фермиони в нея се разкрива чрез невъзможността да бъдеш в едно и също квантово състояние в същото време на два електрона (съгласно принципа на Паули).
То се изучава по същия начин като квазичастица в периодичен кристален потенциал, при която ефективната маса може да се различава значително от масата в покой.
Чрез движението на електрони се случва електрически ток магнетизъм и термо едс. Зареждането на електрона в движение образува магнитно поле. Външното магнитно поле обаче отклонява частицата от директната посока. По време на ускорението електронът придобива способността да абсорбира или излъчва енергия като фотон. Нейният комплект се състои от електронни атомни черупки, чийто брой и позиция определят химичните свойства.
Атомната маса се състои главно от ядрени протони и неутрони, докато електронна маса Той е от порядъка на 0,06% от общото атомно тегло. Електрическата сила на Кулон е една от основните сили, способни да задържат електрона в близост до ядрото. Но когато молекулите се създават от атоми и възникват химически връзки електрони се преразпределят в новосформираното пространство.
Появата на електроните включва нуклони и адрони. Изотопите с радиоактивни свойства могат да отделят електрони. В лабораторни условия тези частици могат да бъдат изследвани в специални устройства, например телескопите могат да откриват радиация от тях в плазмени облаци.
откритие
Електронът е открит от германските физици през деветнадесети век, когато изучава катодните свойства на лъчите. Тогава други учени започнаха да го изучават по-подробно, привеждайки го в ранг на единична частица. Изследвани са радиационни и други физични явления.
Например, групата, водена от Томсън, оценява заряда на електрона и масата на катодните лъчи, чиято връзка, както тя установи, не зависи от източника на материала.
Бекерел установява, че минералите сами излъчват радиация, а техните бета-лъчи могат да се отклоняват от действието на електрическото поле, а масата и заряда поддържат същото съотношение като катодните.
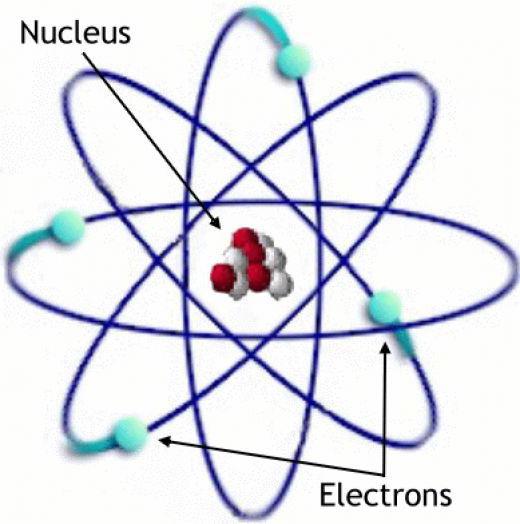
Атомна теория
Според тази теория един атом се състои от ядро и електрони около него, разположени в него като облак. Те са в определени квантовани енергийни състояния, промяната на които е съпроводена от процеса на абсорбция или излъчване на фотони.
Квантова механика
В началото на ХХ век е формулирана хипотеза, според която материалните частици имат свойствата както на самите частици, така и на вълните. Светлината може да се прояви и под формата на вълна (наричана е вълна на де Бройл) и частици (фотони).
В резултат на това беше формулирано известното уравнение на Шрьодингер, където беше описано разпространението на електронните вълни. Този подход се нарича квантова механика. Чрез него са изчислени електронните състояния на енергията в водородния атом.
Фундаментални и квантови свойства на електрона
Частицата проявява фундаментални и квантови свойства.
Основните от тях включват маса (9.109 * 10 -31 kg), елементарен електрически заряд (т.е. минималната част на зареждане). Според проведените досега измервания в електрона не се откриват елементи, които да разкриват неговата субструктура. Но някои учени са на мнение, че това е частично заредена частица. Както е посочено в началото на статията, електрическият заряд е -1,602 * 10 -19 Cl.
 Като частица, един електрон може едновременно да бъде вълна. Експериментът с два прореза потвърждава възможността за едновременното му преминаване през тях. Това е в конфликт със свойствата на частицата, където всеки път е възможно да се премине само през един слот.
Като частица, един електрон може едновременно да бъде вълна. Експериментът с два прореза потвърждава възможността за едновременното му преминаване през тях. Това е в конфликт със свойствата на частицата, където всеки път е възможно да се премине само през един слот.
Смята се, че електроните имат еднакви физични свойства. Следователно тяхната пермутация, от гледна точка на квантовата механика, не води до промяна в състоянието на системата. Вълновата функция на електроните е антисиметрична. Следователно нейните решения изчезват, когато същите електрони попадат в едно и също квантово състояние (принцип на Паули).