Периодичен закон за химичните елементи на Дмитрий Иванович Менделеев
Тук читателят ще намери информация за един от най-важните закони, открити някога от човека в научната област - периодичния закон на Менделеев Дмитрий Иванович. Ще се запознаете с неговата стойност и влияние върху химията, общите разпоредби, характеристиките и детайлите на периодичния закон, историята на откриването и основните разпоредби.
Какво е периодичен закон?
Периодичният закон е естествен закон с фундаментален характер, който за първи път е открит от Д. И. Менделеев през 1869 г., а самото откритие се дължи на сравнение на свойствата на определени химични елементи и на известните по това време атомни маси.

Менделеев твърди, че според неговия закон простите и сложни тела и различните съединения на елементи зависят от тяхната зависимост от периодичен тип и от теглото на техния атом.
Периодичният закон е уникален по свой собствен начин и това се дължи на факта, че той не се изразява чрез математически уравнения, за разлика от други основни закони на природата и вселената. Графично тя намира израз в периодичната таблица на химичните елементи.
История на откриването
Откриването на периодичния закон е станало през 1869 г., но опитите за систематизиране на всички познати елементи на Х започнали много преди това.
Първият опит да се създаде такава система е предприет от И. В. Деберайнер през 1829 г. Той класифицира всички химични елементи, които са му известни, в една триада, свързана една с друга чрез близостта на половината от сумата на атомните маси, принадлежащи към тази група от три компонента. След Деберайнер бе направен опит да се създаде уникална таблица на класификацията на елементите на A. de Chancourtois, наречена неговата система "земната спирала", а след нея беше съставена октавата на Newlands от John Newlands. През 1864, почти едновременно, Уилям Алдинг и Лотар Майер публикуват таблици, създадени независимо един от друг.

Периодичният закон беше представен на научната общност на 8 март 1869 г. и това се случи по време на среща на руското общество. Менделеев Дмитрий Иванович, за всички, обяви откритието си и през същата година беше издаден учебникът на Менделеев “Основи на химията”, където за пръв път беше показана създадената от него периодична таблица. Година по-късно, през 1870 г., той пише статия и я излага в RCW, където за първи път се използва концепцията за периодичния закон. През 1871 г. Менделеев дава изчерпателно описание на своето z-in в известната статия за периодичната легитимност на химическите елементи.

Неоценим принос за развитието на химията
Значението на периодичния закон е изключително голямо за научната общност на целия свят. Това се дължи на факта, че откритието му дава мощен тласък на развитието както на химията, така и на други естествени науки, например физика и биология. Взаимовръзката между елементи с техните качествени химически и физически характеристики е била отворена, тя също така дава възможност да се разбере същността на конструирането на всички елементи по един принцип и да даде основание за съвременната формулировка на понятията за химичните елементи, за да се уточни знанието за веществата от сложна и проста структура.
Използването на периодичен закон позволява да се реши проблемът с химичното прогнозиране, да се определи причината за поведението на известни химически елементи. Атомната физика, включително ядрената енергия, стана възможна благодарение на същия този закон. На свой ред данните от науката позволяват да се разширят хоризонтите на същността на този закон и да се задълбочи в неговото разбиране.
Химични свойства на елементите на периодичната система
По същество химичните елементи са свързани помежду си с характеристиките, присъщи на тях в свободното състояние както на атом, така и на йон, солватирани или хидратирани, в проста субстанция и форма, които могат да образуват многобройните им съединения. Характеристиките на рентгеновите лъчи обаче обикновено се състоят от две явления: свойства, характерни за един атом в свободно състояние, и просто вещество. Много видове имоти принадлежат към този вид имоти, но най-важните са:
- Атомна йонизация и нейната енергия, в зависимост от позицията на елемента в таблицата, нейния ред.
- Енергийната връзка между атома и електрона, която, подобно на атомната йонизация, зависи от местоположението на елемента в периодичната таблица.
- Електроотрицателността на атома, която не носи постоянна стойност, но може да се променя в зависимост от различни видове фактори.
- Радиусите на атоми и йони - тук, като правило, се използват емпирични данни, които са свързани с вълновата природа на електроните в състояние на движение.
- Атомизация на прости вещества - описание на реактивността на елемента.
- Степента на окисление е формална характеристика, но се явява една от най-важните характеристики на даден елемент.
- Окислителният потенциал на простите вещества е измерването и индикацията на потенциала на веществото за неговото действие във водни разтвори, както и нивото на проявление на свойствата на редокс природата.
Честотата на елементите на вътрешния и вторичния тип
Периодичният закон дава разбиране за друга важна съставна част от природата - вътрешната и вторичната периодичност. Горните области на изучаване на атомни свойства, всъщност, много по-трудно, отколкото може да си помислите. Това се дължи на факта, че елементите s, p, d на таблицата променят качествените си характеристики в зависимост от позицията в периода (периодичност на вътрешен характер) и групата (периодичността на вторичния характер). Например, вътрешният процес на преход на елемента s от първата група към осмата към p-елемента се придружава от точки на минимум и максимум на кривата на енергията на йонизирания атом. Това явление показва вътрешната непостоянство на периодичността на промените в свойствата на атома според неговото положение в периода.
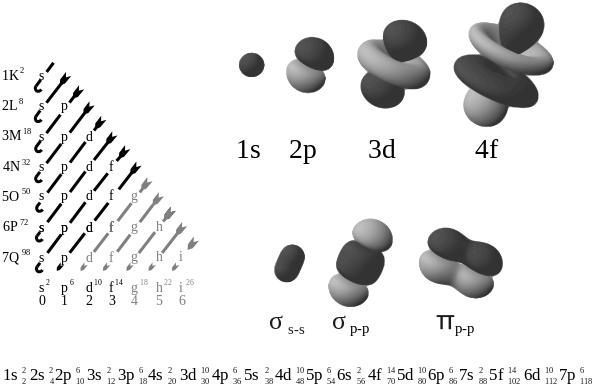
резултати
Сега читателят има ясно разбиране и дефиниция на това, което периодичният закон на Менделеев е, осъзнава неговото значение за човека и развитието на различни науки и има представа за сегашните си позиции и историята на откритието.