Азотна киселина: свойства, подготовка и употреба
въведение
 Вие се интересувате от цветарството и сте дошли в магазина, за да си купите тор за вашите цветя. Преразглеждайки различните имена и композиции, забелязахте бутилка с надписа "Азотен тор". Ние четем състава му: "Фосфор, калций, че-това ... Азотна киселина? И какво е това животно?!". Обикновено с азотна киселина се запознават в такава ситуация. И много от тях искат да знаят повече за него. Днес ще се опитам да задоволя любопитството ви.
Вие се интересувате от цветарството и сте дошли в магазина, за да си купите тор за вашите цветя. Преразглеждайки различните имена и композиции, забелязахте бутилка с надписа "Азотен тор". Ние четем състава му: "Фосфор, калций, че-това ... Азотна киселина? И какво е това животно?!". Обикновено с азотна киселина се запознават в такава ситуация. И много от тях искат да знаят повече за него. Днес ще се опитам да задоволя любопитството ви.
дефиниция
Азотната киселина (формула HNO 3 ) е силна едноосновна киселина. В неокислено състояние, тя изглежда като на снимка 1. При нормални условия, тя е течна, но може да бъде превърната в твърдо агрегатно състояние. И в нея тя прилича на кристали с моноклинна или ромбична решетка.
Химични свойства на азотната киселина
 Той има способността да се смесва добре с вода, където се получава почти пълна дисоциация на тази киселина в йони. Концентрираната азотна киселина има кафяв цвят (снимка). Осигурява се чрез разлагане на азотен диоксид, вода и кислород, което се дължи на слънчевата светлина, която пада върху нея. Ако се нагрее, ще се получи същото разлагане. Всички метали реагират с него, с изключение на тантал, злато и платиноиди (рутений, родий, паладий, иридий, осмий и платина). Въпреки това, връзката му с солна киселина може дори да разтвори някои от тях (това е така наречената "кралска водка"). Азотната киселина, която има някаква концентрация, може да се прояви като окислител. много органична материя при взаимодействие с него може спонтанно да се възпламени. И някои метали в тази киселина ще бъдат пасивирани. Когато са изложени на тях (както и при реакция с оксиди, карбонати и хидроксиди), азотната киселина образува нейните соли, наречени нитрати. Последните се разтварят добре във вода. Но нитратните йони в него не се хидролизират. Ако солите на дадена киселина се загреят, те ще бъдат необратимо разложени.
Той има способността да се смесва добре с вода, където се получава почти пълна дисоциация на тази киселина в йони. Концентрираната азотна киселина има кафяв цвят (снимка). Осигурява се чрез разлагане на азотен диоксид, вода и кислород, което се дължи на слънчевата светлина, която пада върху нея. Ако се нагрее, ще се получи същото разлагане. Всички метали реагират с него, с изключение на тантал, злато и платиноиди (рутений, родий, паладий, иридий, осмий и платина). Въпреки това, връзката му с солна киселина може дори да разтвори някои от тях (това е така наречената "кралска водка"). Азотната киселина, която има някаква концентрация, може да се прояви като окислител. много органична материя при взаимодействие с него може спонтанно да се възпламени. И някои метали в тази киселина ще бъдат пасивирани. Когато са изложени на тях (както и при реакция с оксиди, карбонати и хидроксиди), азотната киселина образува нейните соли, наречени нитрати. Последните се разтварят добре във вода. Но нитратните йони в него не се хидролизират. Ако солите на дадена киселина се загреят, те ще бъдат необратимо разложени.
приемане
За да се получи азотна киселина, синтетичният амоняк се окислява, като се използват платино-родиеви катализатори, докато се появи смес от азотни газове, които впоследствие се абсорбират от водата. Той също се образува при смесване и нагряване. калиев нитрат и железен витрий. 
приложение
С помощта на азотна киселина се произвеждат минерални торове, взривни вещества и някои токсични вещества. Тя е гравирана отпечатани форми (ецвани дъски, магнезиеви клишета и др.), Както и подкиселени тониращи разтвори за снимки. Бои и лекарства се произвеждат от азотна киселина и се използва също за определяне на наличието на злато в златни сплави.
Физиологично въздействие
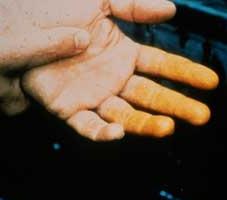
Като се има предвид степента на влияние на азотната киселина върху тялото, тя се отнася до третия клас на опасност (средно опасен). Вдишването на неговите пари води до дразнене на дихателните пътища. Когато се прилага върху кожата, азотната киселина оставя много дълготрайни язви. Зоните на кожата, където тя е станала, се превръщат в характерен жълт цвят (снимка). Научно казано, настъпва реакцията на ксантопротеин. Азотният диоксид, който се получава чрез нагряване на азотна киселина или разграждането му на светлина, е много токсичен и може да причини белодробен оток.
заключение
Азотната киселина облагодетелства едно лице както в разредено, така и в чисто състояние. Но най-често се среща в състава на веществата, много от които вероятно знаете (например нитроглицерин).