Литиев хидроксид. Примери за химични реакции, както и физичните свойства на алкалите и неговите характеристики
Какво е литиев хидроксид? Това съединение е едно от най-важните топлоустойчиви съединения, използвани при производството на различни литиеви соли. Ионите на този елемент имат редица характерни черти, които са намерили широко приложение в химическото производство.
Особености на структурата на литиевия атом
Литий (Li) е елемент от група I на основната подгрупа на втория период и принадлежи към групата алкални метали. Той често се нарича преход към алкалоземни елементи, тъй като има малко по-ниска активност от следните членове на тази група, например натрий (Na) или калий (К).
Литиевият атом има най-малък радиус сред всички алкални метали, което причинява неговата химична активност. Особена роля играе стабилната 1s 2 електронна обвивка от типа хелий, която предхожда 2s 1 валентния електрон, което създава висока поляризуемост на частицата.
Ad
Това свойство на литий характеризира появата на електромагнитни или диполни полета около атома, което ви позволява да създавате силни комплексни йони като [Li (NH3) n ] + . Трябва да се отбележи, че с такива свойства самият атом не е подложен на поляризация, което обяснява термичната нестабилност на някои от неговите соли, особено при сложните аниони.
Всички тези факти обясняват някои особености на физичните и химичните свойства на литиев хидроксид (LiOH).

Физични свойства
Чистият LiOH е много разяждащо вещество, което може да разруши стъкло и порцелан, така че се съхранява във восъчни съдове. В стопеното състояние може да се получи само в никелови или сребърни съдове, тъй като окислява повечето метали и сплави. Златото е едно от малкото вещества, устойчиви на въздействието на такова съединение.
Самата основа, в сравнение с оксида Li2O, е химически нестабилна и по-близо до 1000 ° С в атмосфера на водород, Н2 се разлага на съставките си (Пример 1).
Литиев оксид и литиев хидроксид в химически чисто състояние са твърди вещества, относително разтворими във вода, но по-малко (почти 5 пъти) от подобни съединения на следните членове на групата. Най-високата точка на разтваряне при описаната база е при 100 ° С - 17.5 g / 100 g разтворител, докато например натриев хидроксид (NaOH) е 337 g / 100 g и продължава да нараства с повишаване на температурата. В същото време разтворимостта на литиев хидроксид е почти 100 пъти по-голяма от разтворимостта на гасената вар (Ca (OH) 2 ), при която тази способност намалява с повишаване на температурата.
Ad
Интересно е, че е експериментално възможно да се получи газообразен LiOH в присъствието на водна пара. Получава се чрез нагряване на лиоксида до 2000 ° С, когато след етапа от 1000 ° С, налягането на парите на това съединение се увеличава поради образуването на стабилна родителска основа (пример 2).
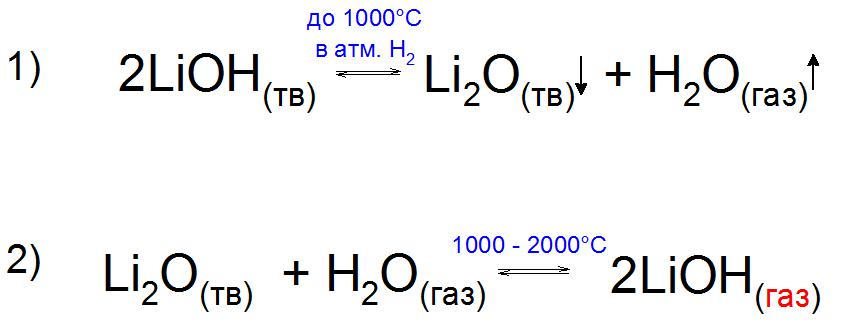
Химични свойства
Литиевият хидроксид не се счита за киселина, тъй като не е амфотен елемент и не показва способността да се разлага според типа МеОН - MeO - + H + (където, Ме е всеки метал от група I или II на основната подгрупа), както и другите представители на алкалните метали. За такива съединения се казва, че са много силни бази, тъй като тяхната дисоциационна константа съгласно принципа на МеОН-Ме + ОН е много висока (Kb , LiOH = 6.75 · 10 -1 ).
Тъй като такова съединение проявява силни основни свойства, то може да влезе реакции на неутрализация с киселини киселинни оксиди и размяна с различни соли (пример 3).
Типична реакция е взаимодействието на студени и горещи концентрирани разтвори на литиев хидроксид с хлорен газ за образуване на хипохлорити и литиев хлорат (пример 4).
Характеристика на тази основа е взаимодействието с горещ разтвор на водороден пероксид Н 2 О 2 с образуването на кристален хидрат на литиев пероксид Li 2 O 2 в етанол, разделен във вакуум (Пример 5).
Ad
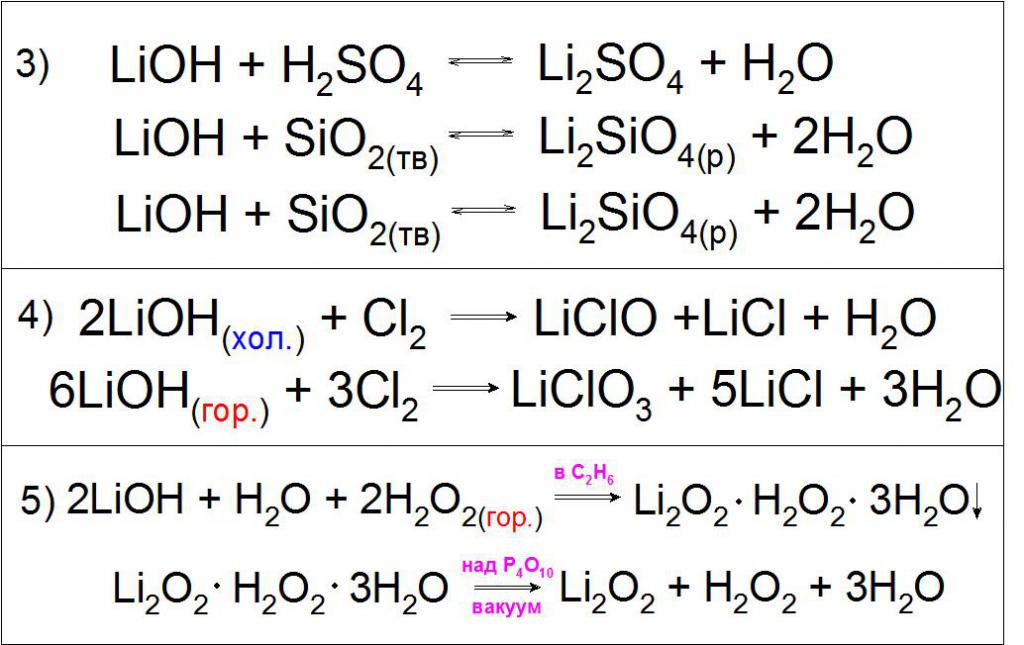
приемане
LiOH се получава по различни начини, едно от които е директното взаимодействие на метал или негов оксид с вода съгласно схемата литиев → литиев оксид → литиев хидроксид.

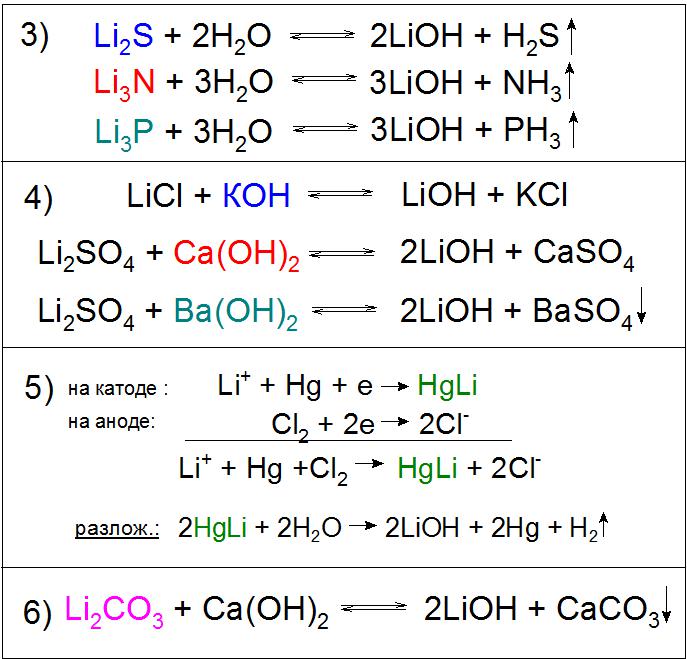
Използва се също хидролиза на сулфид, нитрид, фосфиди и други съединения (пример 3).
Реакциите обменни разтвори на литиеви соли са възможни с почти всяка причина, например калиев хидроксид (KOH), калций (Ca (OH) 2 ) и барий (Ba (OH) 2 ), и с последния реагент химическото взаимодействие преминава почти напълно с Li сулфат. В първия и втория случай реакцията ще бъде оправдана поради лошата разтворимост на получените соли в разтвор на LiOH (пример 4), а в третия - към това ще се добави водонеразтворим BaSO 4 (пример 4). Следва да се отбележи, че последният вариант не се използва в производството по икономически причини.
Ad
Друг забележителен метод за получаване на това съединение е електролизата на разтвор на литиев хлорид LiCl на живачен катод. Това произвежда амалгама HgLi, интересна, защото нейната точка на топене е много по-висока (609 ° C) от която и да е от неговите компоненти. В процеса на разлагане с вода на полученото съединение се получава необходимата база (Пример 5).
От особено индустриално значение е реакцията на разлагане на литиев карбонат с гасена вар, по време на която химическо равновесие изкуствено изместен към дясната страна за по-висок добив на основния продукт (пример 6).
приложение
Литиевият хидроксид се използва при приготвянето на стеарати от този метал за производството на водонепроницаеми замръзващи и топлоустойчиви смазки. Използва се и като катализатор при производството на полимерни материали и като компонент на електролита в различни батерии.

В пожарната и военната практика литиевият хидроксид се използва като абсорбер на въглероден двуокис (СО 2 ) в газовите маски.