Закон на Далтон за смес от газове: примери за решаване на проблеми
Газови смеси, в които компонентите не взаимодействат помежду си, могат да бъдат описани, използвайки закона на Dalton. Той свързва парциалните налягания на компонентите и техните молни фракции в едно равенство. Нека разгледаме този закон по-подробно и да покажем как може да се използва с конкретни примери.
Идеални газове

Законът на Далтон във физиката се оказва валиден само за идеални газове. Чрез такива разбираеми газове съставните частици, от които (атоми, молекули) не взаимодействат помежду си. За идеален газ с непроменен брой молекули (атоми) в него (n = const) е вярно следното равенство, свързващо три макроскопични параметъра (налягане Р, обем V и температура Т):
P * V = n * R * T, R = 8.314 J / (K * mol) е постоянна стойност.
Всички реални газове при налягания от няколко атмосфери и температури от около помещение и нагоре могат да се считат за идеални с добра точност, т.е. даденото равенство е валидно за тях.
Частично налягане на компонента
За да се разбере същността на закона на Далтън, е необходимо да се разбере понятието "парциално налягане".
Тъй като молекулите на различни газове не се чувстват взаимно, за всеки химичен компонент i в газовата смес, следващото равенство ще бъде вярно:
Pi * V = ni * R * T.
Това означава, че всеки компонент може да се счита за независим от останалите. Тъй като молекулите му заемат целия обем V и имат температура Т, характерна за цялата смес, това е мястото, където следва писменото изразяване.
Ad
Налягането P i се нарича частично за i-тия компонент. С други думи, парциалното налягане е налягането, което само i-тият компонент създава върху стените на съда. Тя се нарича частична, защото е част от общото налягане или нейната част.
Формулировката на закона на Далтън

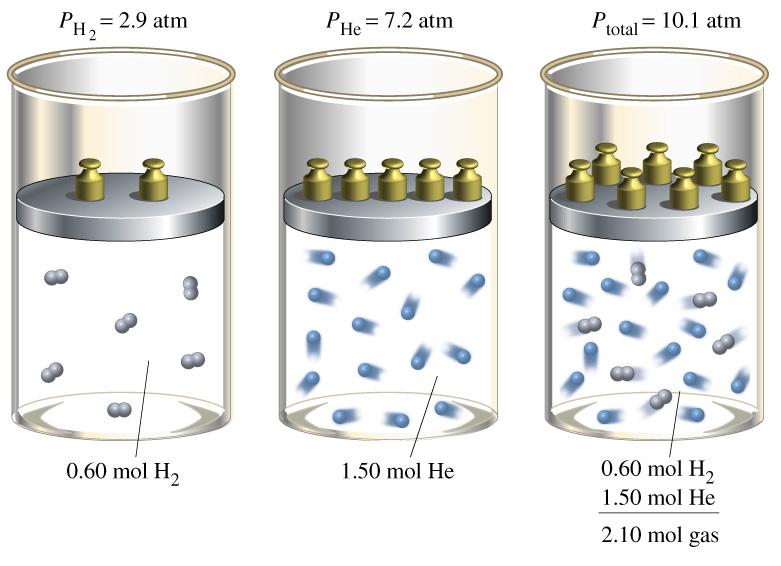
В ранните години на XIX век, изучавайки поведението на различни газови смеси, британският учен Джон Далтън установява следното: ако сумирате всички парциални налягания на компонентите на газова смес, получавате общо налягане, което може да бъде измерено с барометър, манометър или друг инструмент. Това е законът на Далтън. Пишем го под формата на математическо равенство:
P tot = ∑ i (P i ).
За да разберем защо това равенство е вярно, можем, ако си припомним, че компонентите на сместа създават налягане независимо един от друг.
Като се има предвид, че парциалното налягане P i е право пропорционално на количеството вещество n i компонент i, което винаги е вярно, когато T = const и V = const, тогава стигаме до друго равенство:
P i / P tot = n i / n = x i .
Стойността на x i се нарича молекулна фракция. С атомния процент a i на компонента, той е свързан с проста връзка:
a i = x i * 100.
Изразът, който позволява да се определи моларната фракция на компонента чрез неговото парциално налягане и обратно, също се нарича закон на Далтон.
Трябва да се помни, че разглежданият закон е валиден не само в случай на идеални газове, но и в отсъствието на химични реакции в тях. Последните водят до промени в компонента и моларния състав, което нарушава закона за налягането на газовата смес.
Примери за решаване на проблеми
В този параграф ще разгледаме примери за прилагането на закона на Далтон за решаване на практически проблеми.
Задача 1. Необходимо е да се определи парциалното налягане на трите основни компонента в сух въздух.
От литературата може да се установи, че тъй като въздухът е сух, основните му компоненти ще бъдат азот (около 78%), кислород (около 21%) и аргон от благороден газ (около 1%). Като се има предвид, че общото налягане на въздуха на морското равнище е 1 атмосфера, и превръщането на атомния процент в молни фракции, получаваме стойностите за парциално налягане за всеки компонент:
Ad
P i = P tot * x i
PN2 = 1 * 0.78 = 0.78 атм.
PO2 = 1 * 0.21 = 0.21 atm.
P Ar = 1 * 0.01 = 0.01 atm.
Задача 2. Има два цилиндъра с чисти газове. Първият цилиндър съдържа азот с температура 300 K, обем 10 литра и налягане 2 атмосфери. Вторият цилиндър съдържа кислород с температура 300 K, но с обем 15 литра и налягане 1,5 атмосфери. И двата цилиндъра са свързани помежду си. Необходимо е да се изчисли парциалното налягане на всеки компонент в получената смес.
Ще започнем да решаваме този проблем чрез изчисляване на количеството вещество за азот и кислород. Използвайки уравнението за идеален газ, получаваме:
P N2 * V N2 = n N2 * R * T =>
nN2 = PN2 * VN2 / R * T = 2 * 101325 * 10 -2 / (8.314 * 300) = 0.812 mol;
n O2 = РО2 * VO2 / R * T = 1.5 * 101325 * 1.5 * 10 -2 / (8.314 * 300) = 0.914 mol.
Когато са свързани два цилиндъра, газовете ще бъдат смесени така, че всеки компонент да заема целия обем на двата цилиндъра. Общото налягане, което ще бъде в системата, може да се изчисли с помощта на уравнението на състоянието на идеален газ:
V tot = V N2 + V O2 = 2.5 * 10 -2 m 3 ;
n = n N2 + nO2 = 0.812 + 0.914 = 1.726 mol.
P tot = n * R * T / V tot = 1,726 * 8,314 * 300 / (2,5 * 10 -2 ) = 172199,568 Pa или 1,7 atm.
Сега можем да приложим формулите на закона на Далтон за изчисляване на парциалните налягания на кислород и азот:
P N2 = P tot * n N2 / n = 1.7 * 0.812 / 1.726 = 0.8 atm;
P O2 = P tot - P N2 = 1.7 - 0.8 = 0.9 atm.
Съотношението на полученото парциално налягане на газовете е равно на съотношението между количествата на веществото за тях.