Колоидни разтвори: методи за приготвяне и употреба
Много хора, които не се занимават с химия, чувайки фразата "колоидни разтвори", представляват нещо като гел, вискозна смес. Факт е, че първоначално това име произхожда от гръцката дума, преведена като „лепкава“. Когато балансиращата система не е балансирана, золите се утаяват, наподобявайки желе.
Като правило, колоидните разтвори са абсолютно прозрачна течност. В зависимост от състава, той може да бъде безцветен или оцветен. На пръв поглед солите не се различават от истинските решения. Изследването на този вид субстанция се занимава с цяла секция - колоидна химия.

Общи характеристики
Всяко решение е еднофазна система, съдържаща два или повече компонента. Обратно, суспензията или емулсията са по-малко стабилни. В течни разтвори по време на съхранение може да се утаи, ако например те се поставят в несвързано затворен контейнер и се получава изпаряване на течността. В други случаи това е инертна система, в която компонентите не реагират помежду си и затова може да остане непроменена дълго време.
Ad
Свойства на колоидни разтвори

Молекулите на веществото са равномерно разпределени в разтворителя, но те непрекъснато правят броуновско (осцилаторно) движение. В резултат на това се получава пълно смесване на компонентите на системата. Свойствата на колоидните разтвори в този процес са малко по-различни. Частиците на такава система се наричат мицели. Те се разпространяват от един слой течност в друг по-бавно (100 пъти). Причината за ниската скорост е по-голям обем мицели в сравнение с молекулите на истинските разтвори.
В зависимост от размера на частиците, техните количества, колоидните разтвори се различават по вискозитет. Често съществуват системи, които преминават в състояние на гел с понижаване на температурата. Наличието на твърде големи мицели и превишаването на границата на разтворимост води до мътност.
Ad
Колоидните частици, за разлика от молекулите, имат по-големи размери и следователно могат да разсейват светлината. По този начин е възможно да се разграничат тези решения от истинските. При преминаване през такава система ще бъде видим лъч светлина.
Мицеловата структура
Получаването на колоидни разтвори се основава на образуването на мицели, които трябва да останат за запазване на свойствата на системата в стабилно състояние. Частицата има сложна структура, състояща се от ядро, образувано от слабо разтворима субстанция. Около него се разпределя слой от потенциално определящи йони. Обикновено те са същите като в слабо разтворимата субстанция, разположена в центъра на мицела (правило Панет - фаянс). Такива йони определят заряда на ядрото.
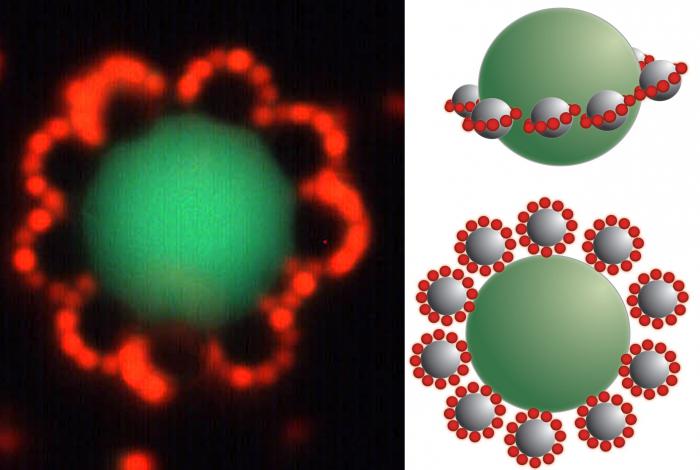
Например, при взаимодействието на калиев йодид и сребърен нитрат образуват се мицели. Ядрото на такива частици е сребърен йодид (AgI). Ако вторият компонент преобладава, тогава потенциално-определящите йони ще бъдат Ag + , ако първият е I - . Следващият слой е противойоните на веществото, което е взето в излишък. Те образуват две зони. Първият е разположен близо до повърхността на ядрото, е част от адсорбирания слой. Вторият е част от дифузионния слой, който се състои от свободно движещи се йони на повърхността.
Ad
Колоидната частица е ядро с адсорбиран слой, което включва потенциално-определящи йони и контра-йони. Тази формация има такса. Мицелът включва колоидална частица и дифузионен слой от противо-йони и е неутрален.
Как се образува мицела
Всички методи за получаване на колоидни разтвори се основават на взаимодействието на слабо разтворими съединения с електролит. Например, AgNO 3 (сребърен нитрат) с KI (калиев йодид). В резултат на реакцията се получават AgI и KNO3 (калиев нитрат). Структурата на мицела може да бъде представена схематично. Има 2 варианта за образуване на колоидни частици от горните съединения:
- С излишък от AgNO 3 - {n (AgI) mAg + (mx) NO 3 ¯} xNO 3 ¯.
- С излишък от KI - {n (AgI) mpi (mx) K + } xK + .
Първо се посочва ядрото, след това потенциално-определящите йони и противойоните на адсорбирания и дифузионния слой. Електрокинетичният потенциал, който определя заряда на колоидна частица, се обозначава с буквата "x". Тя възниква поради разликата в повърхностната енергия на ядрото на частица с потенциално-определящи йони.
стабилност

Колоидните разтвори са способни да останат непроменени за дълго време. Стабилността на такива системи е следствие от мицеловите заряди със същото име, което води до тяхното отблъскване един от друг. Въпреки това, с твърде големи размери и висока концентрация, частиците могат да се сблъскат и сливат. Стабилността на колоидните разтвори е относително понятие. Те могат да се съхраняват непроменени достатъчно дълго.
Ad
Коагулацията на колоидните разтвори е процесът на залепване на мицели един към друг. При стабилно състояние на системата, това явление се случва бавно, което му позволява да се задържи дълго време (до 100 години) в еднофазно състояние. Това явление се нарича агрегатна нестабилност.
Коагулация
Скоростта на агрегиране на частиците и, в резултат, разделяне на фазите, зависи от много фактори, включително размера и концентрацията на мицелите, температурата на съхранение. Ускоряването на процеса на коагулация е резултат от добавянето на електролит. Това явление се наблюдава в хидрофилни системи. Известни методи за забавяне на процеса на агрегиране на частиците. Например, смесване на липофилен колоид с хидрофилен. Загубата на стабилност на золите може да бъде повлияна от нагряване или охлаждане, механично напрежение.
Коагулиране на колоидни разтвори при използване на електролити
Има определени модели на влияние на електролити върху колоиден разтвор. Така че, за да започнете процеса, се нуждаете от определена концентрация на последното, а не под определено ниво - прага на коагулация. Електролитът е вещество, което може да провежда електрически ток в резултат на дисоциация в разтвор или стопяване в йони. Състоянието на колоиден разтвор се влияе от йон, чийто заряд е противоположен на този на мицела. Действието се засилва със степента на зареждане (правило на Шулце-Гарди).
Друг фактор, който определя степента на йонно влияние е тяхната хидравличност. Частиците със същия заряд имат различно ниво на действие върху процеса на коагулация. При отделянето на колоиден разтвор коагулационните йони присъстват в утайката. При добавяне на смес от електролити, нейните компоненти могат да отслабят ефекта един от друг (антагонизъм) или, обратно, да подобрят (синергизъм). Рядко се наблюдава независим (адитивен) ефект.
Ad
Начини за получаване

Методите за получаване на колоидни разтвори са намалени до две. Една от възможностите е диспергирането (смилането) на големи частици до размери, съответстващи на колоидалните. Такъв процес може да се осъществи например чрез използване на ултразвукови устройства (механично смилане). Различни дисперсни методи са образуването на колоидни частици в резултат на добавянето на електролити, които се адсорбират на повърхността на колоидните ядра и прехвърлят частиците в разтворено състояние.
Обратното на дисперсионния метод е кондензационният метод, който се състои в агрегиране на малки частици в по-големи. Това явление възниква, например, при смяна на разтворителя. Как може да се постигне този ефект? Налице е рязък спад на разтворимостта поради промени в околната среда. Освен това, веществото образува колоидна частица. В неговата формация участват молекули на разтворители, с които се смесва по-добре. Този ефект, например, се постига чрез постепенно добавяне на колофон, разтворен в етанол във вода.
Различни реакции на кондензация, включително тези, описани по-горе, също се прилагат за методите на агрегиране. Други примери могат да бъдат хидролиза на сол метали, по-специално железен хлорид (FeCl3), реакция на неутрализация, получена от взаимодействието на бариев хидроксид (Ba (OH) 2 ) със сярна киселина (H2S04).
разтварящ
Стойността на колоидните разтвори в човешкия живот е голяма поради способността на повърхностноактивните вещества да увеличат разтварянето на хидрофобни съединения във вода. Това явление се нарича "разтваряне". В основата си този процес представлява разтварянето на съединенията в мицели. Поради това явление праховете могат да отстранят замърсяването от тъканите, което води до стабилни емулсии на въглеводороди и багрила във вода.
Разтварянето може да се извърши по различни начини. Така, неполярните въглеводороди проникват в ядрото на мицелите, докато съединения с хидрофилни и хидрофобни части (амини, алкохоли) са вградени така, че първият е външен, а вторият навлиза дълбоко в колоидните частици. Съществува и явлението обратна разтваряне, което се състои в разтваряне на вода в масла. В случая на нейоногенни повърхностноактивни вещества се идентифицира друг метод за повишаване на разтворимостта на хидрофобните съединения - свързване към повърхността на мицела чрез химични връзки (по-специално водород).
Широко разпространено разпространение
Колоидните разтвори винаги присъстват вътре и около лицето. Те включват кръв, лимфа, лепила и бои, които често се използват при различни строителни и довършителни работи. Получават се гелове от колоидни разтвори в резултат на коагулация и утаяване. Те включват, например, желе, мармалад, агар-агар, желатин, карагенани. Последните се използват за подобряване структурата на продуктите, по-специално пасти. Навсякъде в човешкото тяло има колоидни разтвори, обогатени с протеини.
Употреба в медицината

В медицината навсякъде се използват колоидни разтвори. Ето няколко примера за тяхното използване. Колоидното сребро, което е малка метална частица, диспергирана във вода, се използва за лечение на изгаряния, стомашни язви и дванадесетопръстника, за измиване на носната лигавица, за да се предотврати разпространението на вирусни инфекции.
Фармацевтичната индустрия предлага голям избор от колоидни разтвори за различни цели. Сред тях са универсални лекарства, които могат да се използват като зарастване на рани при изгаряния, хемороиди; противовъзпалително - със студ, възпалено гърло, синузит; аналгетици - за облекчаване на зъбобол и не само. Те включват колоидния разтвор на хилядолетието. Гелът съдържа алое, пшеничен протеин, жен-шен, витамин Е и други полезни добавки. Много фармацевтични продукти за външна употреба са всъщност колоиден разтвор. За ставите, например, се използва Artro Complex, който съдържа такъв полезен компонент като акулов хрущял.
Приложение в живота и индустрията
Колоидните разтвори формират основата за промиване и почистване на ПАВ. Замърсителите проникват в мицелите и по този начин се отстраняват от повърхността.
Друг важен аспект на използването на мицелообразуващите повърхностно активни вещества е производството на полимери, по-специално латекси, поливинилов алкохол и лепила от растителен произход. Различни пластмаси, кожени заместители се основават на емулсията. Повърхностноактивни вещества също се използват при почистване отпадъчни води и питейна вода.
Предимствата на козметиката на базата на колоидни разтвори са проникването на активните вещества през човешката кожа и структурата на косата. Такива средства се използват ефективно срещу стареене. Те включват, по-специално, Millenium Neo gel. Колоидният разтвор помага на компонентите, съдържащи се в него, да достигнат по-дълбоките слоеве на кожата, заобикаляйки епидермиса.