Химични свойства на арените. Обща формула и характеристики на арените
Ароматни въглеводороди, наричани още арени, са представени от органични вещества. Съставът на техните молекули съдържа едно или повече бензенови ядра (пръстени). Бензенът, наричан още бензен, е първият представител хомоложни серии арена. Химичните свойства, структурата на молекулата и видовете химични връзки в нейната молекула имат редица характеристики. Ще ги разгледаме в нашата статия, както и ще се запознаем с други съединения от групата на ароматните въглеводороди.
Как да се установи структурната формула на арените
През 1865 г. немският учен Ф. Кекуле предложил пространствен модел на най-простата арена - бензен. Тя имаше вид на плосък шестоъгълник, във върховете на който бяха въглеродни атоми, които бяха свързани заедно с три прости и двойни връзки, редуващи се един с друг. Експериментално откритите химични свойства на анесите обаче не съответстват на формулата, предложена от F. Kekule. Например, бензолът не обезцветява разтвора. калиев перманганат и бромна вода, което показва липсата на pi връзки в молекулите на арената. Каква е структурата на бензола в действителност? Нито единични, нито двойни връзки ароматни въглеводороди не. Експериментално е установено, че тези съединения съдържат между въглеродните атоми еквивалентен вид химична връзка, наречена сесква или ароматна. Ето защо те не влизат в окислителна реакция с разтвори на KMnO4 и Br2. Извежда се общата формула на анесите - CnH2n-6. Всички специфични свойства на ароматните съединения могат да се обяснят с тяхната електронна структура, която ще изучаваме по-нататък.
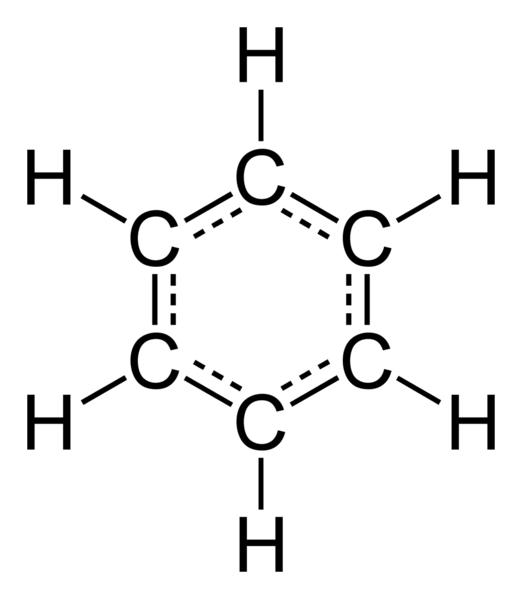
Електронна формула
Като използваме бензен като пример, установяваме как въглеродните атоми са свързани помежду си. Оказа се, че всичките шест въглеродни атома са под формата на sp2 хибридизация. Въглеродът е свързан с водороден атом и два съседни въглеродни атома с три сигма връзки. Това е, което формира плоска шестоъгълна форма на молекулата. Все пак, всеки въглероден атом има още една отрицателно заредена частица, която не участва в хибридизацията. Електронният му облак е под формата на гира и се намира над и под равнината на шестоъгълника, наречен бензенов пръстен. Освен това, всичките шест гири се припокриват и образуват обща ароматна (една и половина) връзка. Именно тя определя всички физически и химически характеристики на веществата. Това е електронната структура на арените.

Какво е бензол?
По-добро разбиране на характеристиките на ароматни въглеводороди ще помогне за запознаване с първия представител на този клас - бензол. Лесно подвижната, горима безцветна течност със специфична миризма, неразтворима във вода, е бензол. Както самото съединение, така и неговите пари са токсични. Съгласно общата формула на арените количественият и качествен състав на молекулата на веществото може да се изрази, както следва: C6H6. Както и при другите ароматни въглеводороди - толуен, антрацен или нафтален, за бензола са типични реакциите на изгаряне и заместване на водородните атоми на бензеновото ядро. Особеност на твърдата оксидация на всички ароматни съединения е силно димният пламък. Сместа от бензолови пари с въздух е експлозивна, така че всички експерименти с веществото в лабораторията се извършват само в аспиратор. Бензолът, както и другите ароматни вещества, не добавя вода или водородни халогениди. Той също така не обезцветява калиев перманганат и бромна вода. Хомолозите на бензола, като толуол или кумол, могат да бъдат окислени, като в този случай реакцията не се подлага на самия бензенов пръстен, а само на радикала.

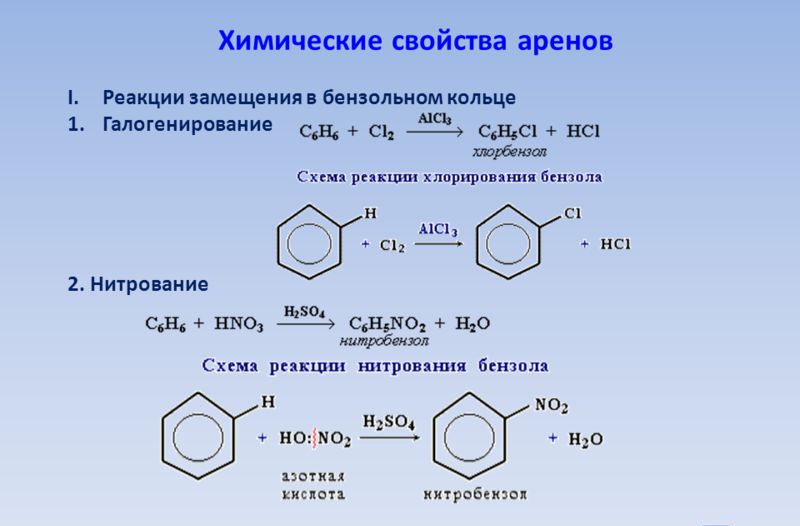
Химични свойства на арените
Какви реакции са способни на съединения, съдържащи бензенови пръстени и една и половина връзки между въглеродните атоми? Първо, това са реакции на заместване, които са много по-лесни за тях, отколкото за алканите. Представете си запис на каталитичната реакция между бензол и бром с участието на железен бромид, водещ до образуването на бромобензен - безцветна течност, неразтворима във вода:
C6H6 + Br2 → C6H5Br + HBr
Ако като катализатор се използва алуминиев хлорид, е възможно да се постигне пълно заместване на всички водородни атоми в бензолната молекула. В този случай се образува хексахлорбензол, чиито безцветни кристали се използват в методите за защита на семената на култивираните растения и при преработката на дърво за удължаване на срока на годност. За по-пълно описание на арените, добавете някои факти. За добавяне на други вещества, като хлор, са необходими специални условия. В нашия случай това ще бъде ултравиолетовото излъчване на реагиращата смес. Продуктът от реакцията е хексахлорциклохексан, или, както се нарича също, хексахлоран. Това е добре познат в селското стопанство инструмент - инсектицид, използван за борба с насекоми вредители.
Ad

Как и защо се получава нитробензен?
Продължаваме прегледа на химичните свойства на анесите. Използвайки концентрирани азотни и сулфатни киселини (нитрираща смес) в една реакция, е възможно да се получи продукт, важен за органичния синтез от бензен - нитробензен. Той е бледожълта течност, мазна на вид, с миризма на бадеми. Той е неразтворим във вода, но често се използва като разтворител за много органични вещества: лакове, мазнини и др. Нитробензенът е многотонен продукт, тъй като се използва като суровина за производството на анилин. Това вещество е толкова важно за химическата промишленост, че си заслужава да се замислим по-подробно. Известен руски химик Н.Н. Зинин през 1842 г. анилин се получава от нитробензен чрез реакцията на редукция на амониев сулфид. В съвременните условия, контактният метод е станал широко разпространен, при което смес от водни и нитробензонови пари преминава при температура от 300 ° С над катализатора. Полученият ароматен амин се използва по-нататък за производството на експлозиви, багрила, лекарства.
От какво се произвеждат ароматите?
Най-обещаващо е да се получи анекс от продукта от коксуващи се въглища и в процеса на рафиниране. Циклопарафините, съдържащи се във въглищния катран, се хидрогенират над катализатора при температури до 300 ° С, реакционният продукт е бензен. Дехидрогенирането на алканите също води до образуването на ароматни въглеводороди. Реакцията на Зелински-Казан бензен се получава от етин чрез преминаване през тръба с активен въглен, нагрята до 600 ° С. Получаването на арени, например толуен, се провежда при използване на реакцията на Friedel-Crafts. Метилбензен (толуен) може също да бъде добит с използване на хептан. Получените видове арени се използват като разтворители и добавки към моторните горива, при производството на анилинови багрила и токсични химикали.
Ad

нафталин
През 50-те и 70-те години на миналия век нафталинът е едно от най-предпочитаните средства за защита на кожата и вълнените продукти от молци в ежедневието. С дълготрайната си употреба облеклото придобива характерна, много устойчива миризма. По-важно е обаче използването на нафталин като суровина за синтеза на лекарства, багрила, експлозиви. Основните методи на неговото производство се основават на преработката на рафинирани нефтопродукти и отпадъци от производството на етилен - пиролизна смола. Веществото, за разлика от бензола, съдържа две бензолни ядра, следователно реакциите на нитриране и халогениране се извършват по-бързо. Продължавайки да даваме примери за арените, нека се спрем на друг важен ароматен въглеводород за индустрията - винилбензол.
стирен
Съвременната индустрия на строителни материали е невъзможна без полимерни материали: светлина в преработка, трайна и износоустойчива. Полимери, получени от винилбензол, като полистирен (експандиран полистирен), SAN и ABS пластмаси, се използват при производството на опънати тавани, подови настилки, изолация на стени. Стиренът се получава от етилбензол под формата на безцветна, запалима течност със специфичен мирис. В бъдеще тя се подлага на полимеризация и се извлича твърда стъклена маса - полистирол. Той служи като първоначален продукт при производството на гореспоменатите строителни материали. Винилбензен се използва като разтворител, използван заедно с бутадиен реакции на полимеризация което води до синтеза на стирен-бутадиенови каучуци.
Ad

Номенклатура на ароматни съединения
Името на арените съгласно международната класификация по IUPAC включва наименованието на заместител, към който се добавя думата "бензен". Например, C6H5CH3 е метилбензен, С6Н5С2Нз е винилбензен. Тези съединения имат тривиални наименования, така че първото съединение се нарича толуен, а второто - стирен. Арените могат да съдържат два заместителя, например два метилови радикала. Те могат да се присъединят към карбоксилния цикъл в три позиции: при 1 и 2 въглеродни атома, след това говорят за орто позициите на заместителите. Ако радикалите са разположени в 1 и 3 въглеродни частици, тогава става въпрос за мета позиционирането на заместителите, при 1 и 4 въглеродни атома, това е алтернативно заместване. По-висшите хомолози на бензола могат да бъдат представени като производни на наситени въглеводороди, в молекулите на които един водороден атом е заместен с фениловия радикал С6Н5-. Например, съединение с формула C6H5C6H13 ще се нарича "фенилхексан".
В нашата статия, ние изучавахме химичните свойства на анесите, както и описание на техните свойства и приложения в промишлеността.