Ароматни въглеводороди: всичко около тях
Химията е много интересна наука. Тя изучава всички вещества, които съществуват в природата, и много от тях. Те са разделени на неорганични и органични. В тази статия ще разгледаме ароматни въглеводороди, които принадлежат към последната група.
Какво е това?
Това е така органична материя които са съставени от едно или повече бензенови ядра - стабилни структури от шест въглеродни атома, свързани в полигон. Тези химични съединения имат специфичен мирис, който може да се разбере от името им. Въглеводородите от тази група са циклични, за разлика от алканите, алкините и т.н. 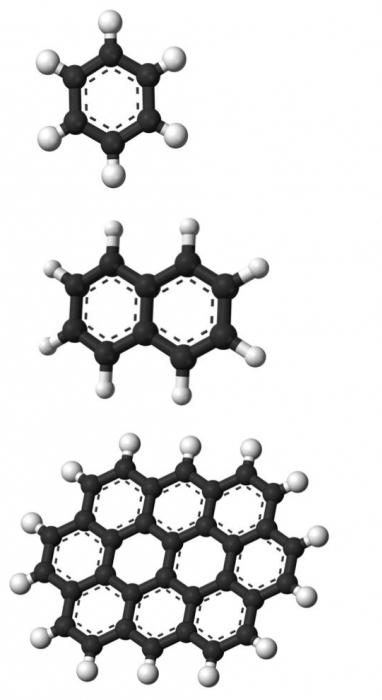
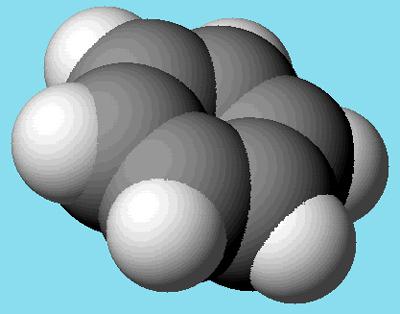
Ароматни въглеводороди. бензол
Това е най-простото химическо съединение от тази група вещества. Съставът на неговите молекули се състои от шест въглеродни атома и същото количество водород. Всички други ароматни въглеводороди са бензенови производни и могат да се получат с неговото използване. Това вещество при нормални условия е в течно състояние, безцветно, със специфичен сладник, не се разтваря във вода. Кипва се при температура от +80 градуса по Целзий и се замразява при +5.
Ad
Химични свойства на бензен и други ароматни въглеводороди
Първото нещо, което трябва да потърсим е халогенирането и нитрирането.
Реакции на заместване
Първият е халогенирането. В този случай, за да се осъществи химичното взаимодействие, е необходимо да се използва катализатор, а именно железен трихлорид. Така, ако към бензола (С6Н6) се добави хлор (С1), се получава хлорбензен (С6Н5С1) и хлороводород (НС1), който се отделя като чист газ със силна миризма. Това означава, че в резултат на тази реакция един водороден атом е заменен с хлорен атом. Същото може да се случи, когато към бензола се добавят други халогени (йод, бром и др.). Втората реакция на заместване - нитриране - следва подобен принцип. Тук концентриран разтвор действа като катализатор. сярна киселина. За този вид химическа реакция необходимо е да се добави азотна киселина (HNO 3 ), също концентрирана, към бензола, в резултат на което се образуват нитробензен (C 6 H 5 NO 2 ) и вода. В този случай водородният атом е заместен с група от азотен атом и две оксигенатни съединения. 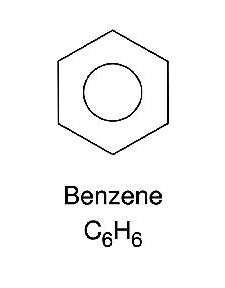
Свързващи реакции
Това е вторият вид химични взаимодействия, при които ароматните въглеводороди могат да влязат. Те съществуват и в два вида: халогениране и хидрогениране. Първият се среща само в присъствието на слънчева енергия, която действа като катализатор. За да се осъществи тази реакция, хлорът трябва също да се добави към бензола, но в по-големи количества, отколкото за заместване. За една молекула бензол трябва да отчитат три хлора. В резултат на това получаваме хексахлороциклохексан (C6H6Cl6), т.е. шест хлор също ще бъде прикрепен към съществуващите атоми.
Ad
Хидрогенирането се осъществява само в присъствието на никел. За целта смесете бензол и водород (Н2). Пропорциите са същите като при предишната реакция. В резултат се получава циклохексан ( С6Н12 ). Всички други ароматни въглеводороди също могат да влязат в този тип реакция. Те се срещат на същия принцип, както при бензола, само при образуването на по-сложни вещества.
Получаване на химикали от тази група
Да започнем все едно с бензола. Той може да бъде получен с помощта на реагент, такъв като ацетилен (С2Н2). От трите молекули на дадено вещество, под въздействието на висока температура и катализатор, се образува една молекула от желаното химично съединение.
Също така, бензол и някои други ароматни въглеводороди могат да бъдат извлечени от каменовъглен катран, който се образува при производството на металургичен кокс. Толуен, о-ксилен, м-ксилен, фенантрен, нафталин, антрацен, флуорен, хризен, дифенил и други могат да бъдат приписани на тези, получени по този начин. Освен това вещества от тази група често се извличат от нефтопродукти.
Ad
Какви са различните химични съединения от този клас?
Стиренът е безцветна течност с приятен мирис, слабо разтворим във вода точка на кипене на вода е +145 градуса по Целзий. Нафталенът е кристално вещество, също слабо разтворимо във вода, се топи при температура +80 градуса и кипи при +217. При нормални условия, антраценът също е представен под формата на кристали, но вече не е безцветен, но жълт на цвят. Това вещество не е разтворимо във вода или в органични разтворители. Точка на топене - +216 градуса по Целзий, кипене - +342. Фенантренът прилича на блестящи кристали, които се разтварят само в органични разтворители. Точка на топене - +101 градуса, кипене - +340 градуса. Флуорен, както подсказва името, е способен на флуоресценция. Това, подобно на много други вещества от тази група, е безцветни кристали, неразтворими във вода. Точка на топене - 118, кипене - +294. 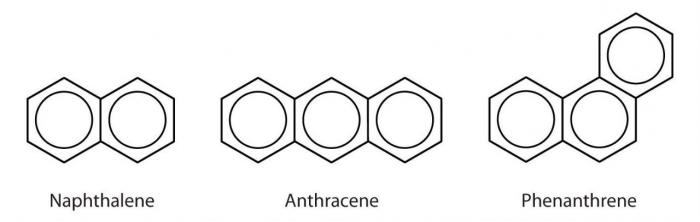
Използването на ароматни въглеводороди
Бензенът се използва при производството на багрила като суровина. Използва се и при приготвянето на взривни вещества, пестициди и някои лекарства. Стиренът се използва при производството на полистирол (пяна), използвайки полимеризацията на оригиналното вещество. Последният е широко използван в строителството: като топло- и звукоизолация, електроизолационен материал. Нафталинът, подобно на бензола, участва в производството на пестициди, багрила и лекарства. В допълнение, той се използва в химическата промишленост за производството на много органични съединения. Антраценът се използва и при производството на багрила. Fluoren играе ролята на полимерен стабилизатор. Фенантренът, както и предишното вещество и много други ароматни въглеводороди, е един от компонентите на оцветителите. Толуенът се използва широко в химическата промишленост за извличане на органични вещества, както и за производството на експлозиви.
Ad

Характеризиране и използване на вещества, произведени от ароматни въглеводороди
Те включват преди всичко продуктите на разглежданите химични реакции на бензола. Хлоробензен, например, е органичен разтворител, също се използва при производството на фенол, пестициди, органични вещества. Нитробензенът е компонент на полиращите агенти за метал, използва се при производството на някои цветове и аромати и може да играе ролята на разтворител и окислител. Хексахлорциклохексан се използва като отрова за борба с насекоми вредители, както и в химическата промишленост. Циклохексан се използва при производството на бои и лакове, при приготвянето на много органични съединения във фармацевтичната промишленост.
Ad
заключение
След като прочетете тази статия, можем да заключим, че всички ароматни въглеводороди имат един и същ вид химична структура, която позволява да се комбинират в един клас съединения. Освен това техните физични и химични свойства също са доста сходни. Външен вид, точки на кипене и точки на топене на всички химикали от тази група не се различават много. Много ароматни въглеводороди се използват в същите отрасли. Вещества, които могат да се получат вследствие на халогениране, нитриране и реакции на хидрогениране, също имат подобни свойства и се използват за подобни цели.