Тип атомна хибридизация
В процеса на определяне на геометричната форма на химическата частица е важно да се има предвид, че двойките валентни електрони на главния атом, включително тези, които не образуват химическа връзка, са далеч един от друг в пространството.
Характеристики на термина
Като се има предвид въпросът за ковалентното химическо свързване често използвали това понятие като хибридизация на атомни орбитали. Този термин е свързан с подреждането на формата и енергията. Хибридизацията на атомните орбитали е свързана с процес на квантово химическо преструктуриране. Орбиталите в сравнение с оригиналните атоми имат различна структура. Същността на хибридизацията е в това, че електронът, който е разположен до ядрото на свързан атом, не се определя от определена атомна орбитала, а от тяхната комбинация с равен основен квантов номер. По принцип този процес се отнася до по-високите атомни енергийни орбитали с електрони.
Специфика на процеса
Видовете хибридизация на атоми в молекули зависят от това как се случва ориентацията на новите орбитали. Според типа на хибридизацията е възможно да се определи геометрията на йон или молекула, за да се приемат особеностите на химичните свойства.
Видове хибридизация
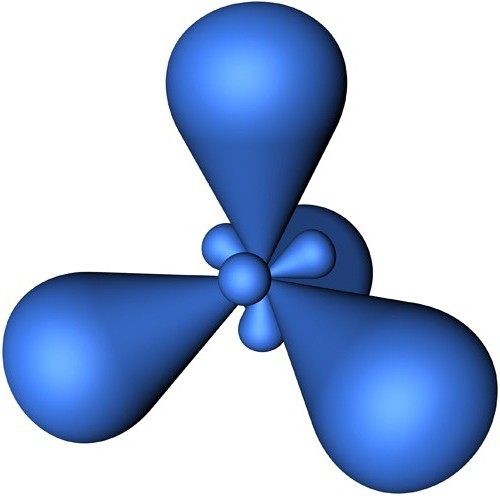
Този тип хибридизация, подобно на sp, е линейна структура, ъгълът между връзките е 180 градуса. Пример за молекула с подобна хибридизационна опция е BeCl2.
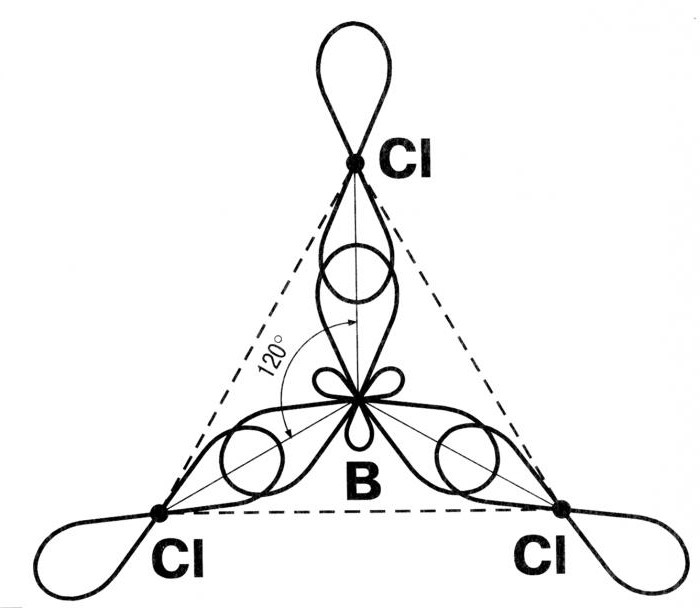
Следващият тип хибридизация е sp 2 . Молекулите се характеризират с триъгълна форма, ъгълът между връзките е 120 градуса. Типичен пример за такъв вариант на хибридизация е ВС13.
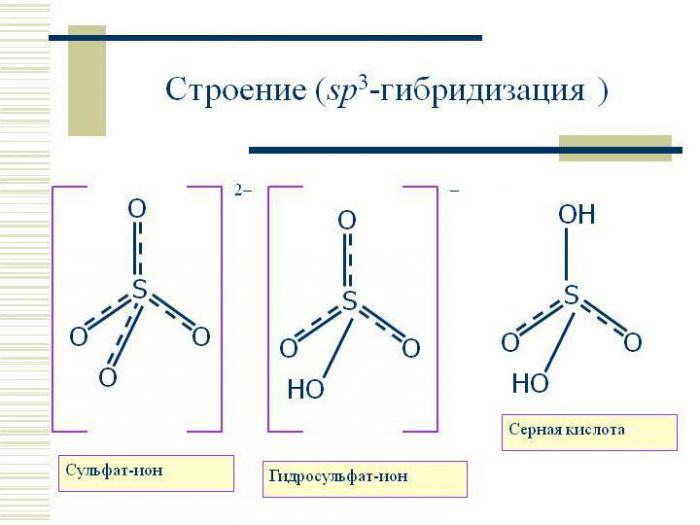
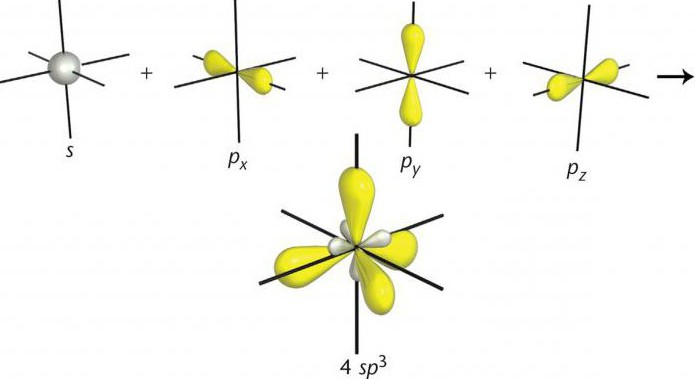
Типът на sp3 хибридизацията предполага тетраедрична структура на молекулата, типичен пример за вещество с тази хибридизационна опция е метановата молекула CH 4 . Валентният ъгъл в този случай е 109 градуса 28 минути.
Не само двойки електрони, но и неразделени двойки електрони участват пряко в хибридизацията.
Хибридизация във водната молекула
Например, във водната молекула между атоми на кислород и водород има две ковалентни полярни връзки. Освен това самият кислороден атом има два чифта външни електрона, които не участват в създаването на химическа връзка. Тези 4 електронни двойки в пространството заемат определено място около кислородния атом. Тъй като всички те имат еднакъв заряд, те се отблъскват в пространството, електронните облаци са на значително разстояние един от друг. Видът на хибридизацията на атомите в дадено вещество предполага промяна във формата на атомни орбитали, те се изваждат и привеждат в съответствие с върховете на тетраедъра. В резултат на това водната молекула придобива ъглова форма, а между кислород-водородните връзки валентният ъгъл е 104,5 ° .
За да се предскаже вида на хибридизацията, може да се използва донорно-акцепторния механизъм за образуване на химични връзки. В резултат на това се извършва припокриване на свободните орбитали на елемент с по-ниска електронегативност, както и орбиталите на елемент с по-голяма електрическа негативност, върху която се намира двойка електрони. В процеса на компилиране електронна конфигурация атомът отчита степента им на окисление.
Правила за идентифициране на вида на хибридизация
За да се определи вида на въглеродна хибридизация, можете да използвате някои правила:
- разкрие централния атом, изчисли броя на σ-връзките;
- поставя частица от окислително състояние на атомите;
- запис на електронната конфигурация на главния атом в желаната степен на окисление;
- направи диаграма на разпределението на валентните електрони в орбитали, свързващи електрони;
- излъчват орбитали, които пряко участват в образуването на връзка, намират неспарени електрони (ако броят на валентните орбитали е недостатъчен за хибридизация, орбиталите на следните енергийно ниво).
Геометрията на молекулата се определя от вида на хибридизацията. Наличието на pi връзки не го засяга. В случай на допълнително свързване е възможна промяна на валентния ъгъл, причината е взаимното отблъскване на електрони, формиращи множествена връзка. Така че, в молекулата азотен оксид (4) с sp 2 хибридизация, валентният ъгъл се увеличава от 120 градуса до 134 градуса.
Амонячна хибридизация
Неразделена двойка електрони влияе върху получения индекс на диполния момент на цялата молекула. Амонякът има тетраедрична структура с неразделена двойка електрони. Йонните връзки на азот-водород и азот-флуор имат показатели от 15 и 19 процента, дължините са дефинирани съответно като 101 и 137 pm. По този начин в молекулата на азот флуорида трябва да има по-голям диполен момент, но експерименталните резултати предполагат обратното.
Хибридизация в органични съединения
Всеки клас въглеводороди има свой собствен тип хибридизация. Така при образуването на молекули от класа на алканите (наситени въглеводороди), всичките четири електрона на въглеродния атом образуват хибридни орбитали. Когато те се припокриват, се образуват 4 хибридни облака, простиращи се до върховете на тетраедъра. Освен това техните върхове се припокриват с нехибридни s-орбитали на водород, образувайки проста връзка. За наситени въглеводороди, характеристиката на sp3 хибридизацията е характерна.
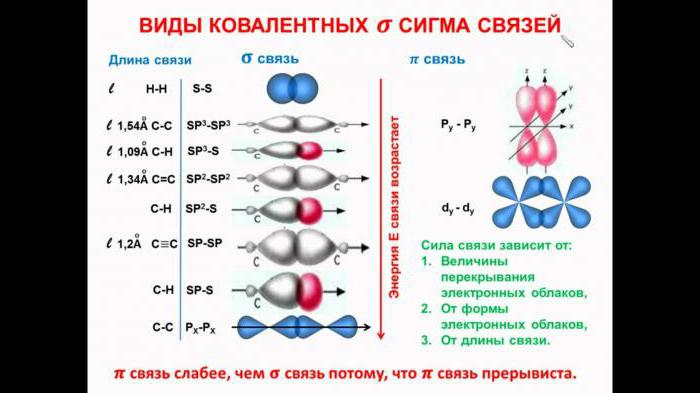
В ненаситените алкени (техният типичен представител е етилен), само три електронни орбитали участват в хибридизацията - s и 2 p; три хибридни орбитали образуват триъгълна форма в пространството. Нехибридни р-орбитали се припокриват, създавайки многократна връзка в молекулата. Този клас органични въглеводороди се характеризира с sp2 хибридното състояние на въглеродния атом.
Алкините се различават от предишния клас въглеводороди в това, че в процеса на хибридизация участват само два вида орбитали: s и p. Двата нехибридни р-електрона, останали при всеки въглероден атом, се припокриват в две посоки, образувайки две многократни връзки. Този клас въглеводороди се характеризира с sp-хибридното състояние на въглеродния атом.
заключение
Чрез определяне на вида на хибридизацията в молекулата може да се обясни структурата на различни неорганични и органични вещества и да се предвидят възможните химични свойства на дадено вещество.