Окисляващият агент е приемащ електрони атом.
Окислителят и редуциращият агент се използват за формулиране на реакцията в органична и неорганична химия. Разгледайте основните характеристики на такива взаимодействия, идентифицираме алгоритъма за съставяне на уравнението и подреждането на коефициентите.

дефинира
Окислител е атом или йон, който при взаимодействие с други елементи приема електрони. Процесът на получаване на електрони се нарича редукция и се свързва с намаляване на степента на окисление.
В курса неорганична химия Разглеждат се двата основни метода за определяне на коефициента. Редуциращият агент и окислителят в реакциите се определят чрез вземане на електронен баланс или чрез метод на полуреакция. Ще се спрем на първия метод за поставяне на коефициенти в OVR.
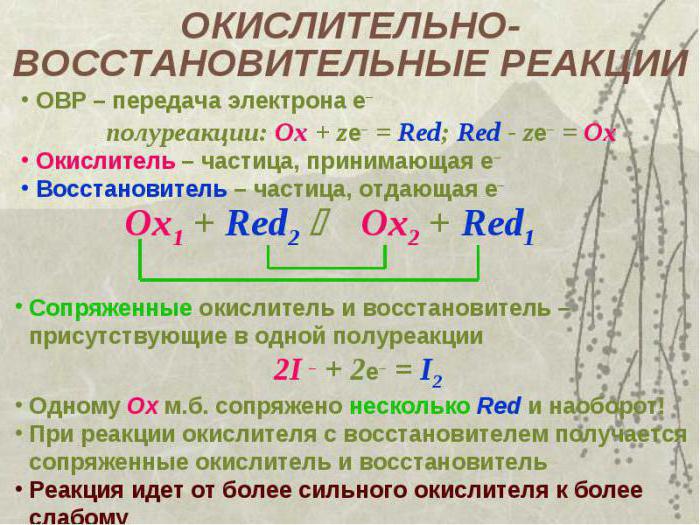
Състояния на окисляване
Преди да определите окислителя в реакцията, трябва да поставите окислителни състояния всички елементи в веществата, участващи в трансформацията. Той представлява заряда на атом от елемент, изчислен по определени правила. При комплексните вещества сумата на всички положителни и отрицателни окислителни състояния трябва да бъде нула. За металите на основните подгрупи тя съответства на валентността и има положителна стойност.
За неметалите, които се намират във формулата в края, степента се определя чрез изваждане на номера на групата от осем и има отрицателна стойност.
За прости вещества тя е равна на нула, тъй като няма процес на приемане или освобождаване на електрони.
За сложни съединения, състоящи се от няколко химични елемента, се използват математически изчисления за определяне на степените на окисление.
Така, окисляващ агент е атом, който в процеса на взаимодействие понижава своето окислително състояние, а редуциращият агент, напротив, увеличава неговата стойност.
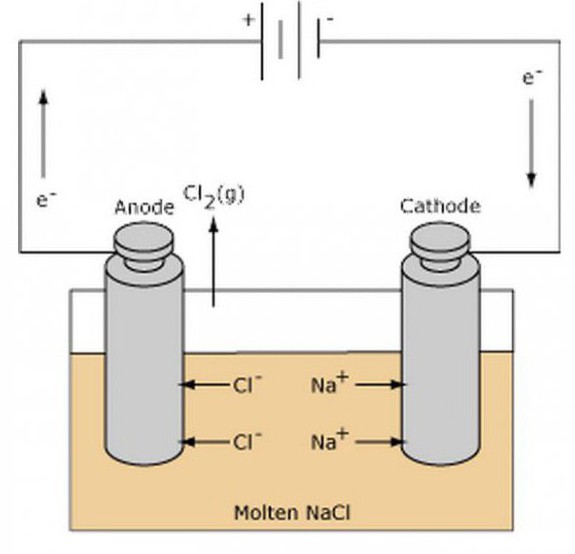
Примери iad
Основната характеристика на задачите, свързани с разпределението на коефициентите при окислително-редукционни реакции, е определянето на пропуснатите вещества и формулирането на техните формули. Окисляващ агент е елемент, който ще приеме електрони, но в допълнение към него, редуциращият агент, който ги дава, трябва да участва в реакцията.
Даваме обобщен алгоритъм, чрез който можете да изпълнявате задачите, предложени на завършилите гимназия в един държавен изпит. Помислете за няколко конкретни примера, за да разберете, че окислителят не е само елемент в сложна субстанция, но и просто вещество.
Първо, необходимо е да се подредят стойностите на окислителните състояния за всеки елемент, като се използват определени правила.
След това трябва да анализирате елементите, които не са участвали във формирането на веществата, и да съставите формула за тях. След елиминиране на всички празнини, можете да пристъпите към процеса на извличане на електронния баланс между окислителя и редуктора. Получените коефициенти се поставят в уравнението, ако е необходимо, като се добавят към онези вещества, които не са включени в баланса.
Например, използвайки електронния балансов метод, е необходимо да завършим предложеното уравнение, поставете необходимите коефициенти преди формулите.
H 2 O 2 + H 2 SO 4 + KMnO 4 = MnSO 4 + O 2 + ... + ...
В началото ще определим стойностите на окислителните състояния, които ще получим
+K + Mn +7 O 4 -2 = Mn +2 S +6 O 4 -2 + O 2 0 + …+… H 2+ O 2 - + H 2+ S + 6 O 4 -2 + K + Mn +7 O 4 -2 = Mn + 2 S + 6 O 4 -2 + O 2 0 + ... + ...
В предложената схема те се различават по кислород, а също и в манган калиев перманганат. По този начин редукторът и окислителят се намират от нас. В дясната част няма вещество, в което да има калий, затова вместо пропуски съставяме формулата на нейния сулфат.
След това пишем електронния баланс. Кислородът в този случай ще покаже редуциращи свойства, давайки два електрона. Манганът ги взема, показвайки окислителна способност.
Последната стъпка в тази задача е да се определят коефициентите.
5H2O2 + 3H2SO4 + 2KMnO4 = 2Mn SO4 + 5O2 + 8H2O + K2SO4
Киселини, калиев перманганат, водороден пероксид. Всички метали проявяват редуциращи свойства, превръщайки се в реакции в катиони с положителен заряд.
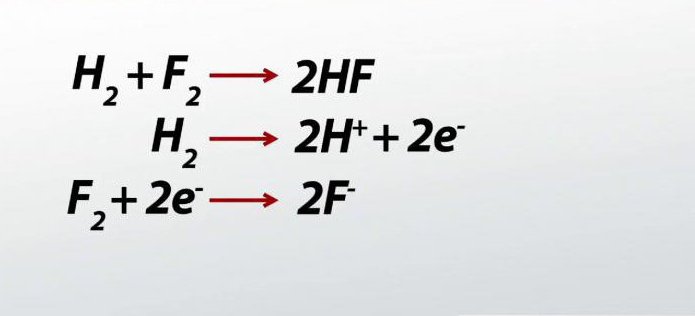
заключение
Процесите, свързани с приемането и освобождаването на отрицателни електрони, се случват не само в неорганичната химия. Метаболизмът, който се извършва в живите организми, е ясен вариант на хода на редокс реакциите в органичната химия. Това потвърждава важността на разглежданите процеси, тяхната релевантност за живата и неживата природа.