Общата формула на амините. Свойства и структура на амините
Органични бази - това наименование често се използва в химията за съединения, получени от амоняк. Водородните атоми в неговата молекула се заменят с въглеводородни радикали. Става дума за амини - съединения, които повтарят химичните свойства на амоняка. В нашата статия ще се запознаем с общата формула на амините и техните свойства.
Молекулна структура
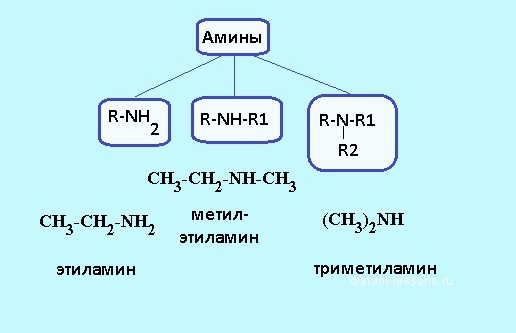
В зависимост от това колко водородни атоми се заменят с въглеводородни радикали, се разграничават първични, вторични и третични амини. Например, метиламин е първичният амин, в който водородната частица е заместена от групата -СНЗ. Структурната формула на амините е R-NH2, може да се използва за определяне на състава на органичната материя. Пример за вторичен амин може да бъде диметиламин, който има следната форма: NH2-NH-NH2. В молекулите на третичните съединения, трите водородни атома на амоняка са заменени с въглеводородни радикали, например, триметиламинът има формулата (NH 2 ) 3 N. Структурата на амините влияе върху техните физични и химични свойства.
Физически характеристики
Общото състояние на амините зависи от това какво моларна маса радикали. Колкото по-малка е тя, толкова по-малка е специфичната плътност на веществото. Амини с по-нисък клас са представени от газове (например, метиламин). Те имат изразена миризма на амоняк. Средните амини са леко миришещи течности, а съединенията с голяма маса въглеводородни радикали са без мирис. Разтворимостта на амините зависи и от масата на радикала: колкото е по-голяма, толкова по-лошо се разтваря веществото във вода. Така структурата на амините определя тяхното физическо състояние и характеристики.
Химични свойства
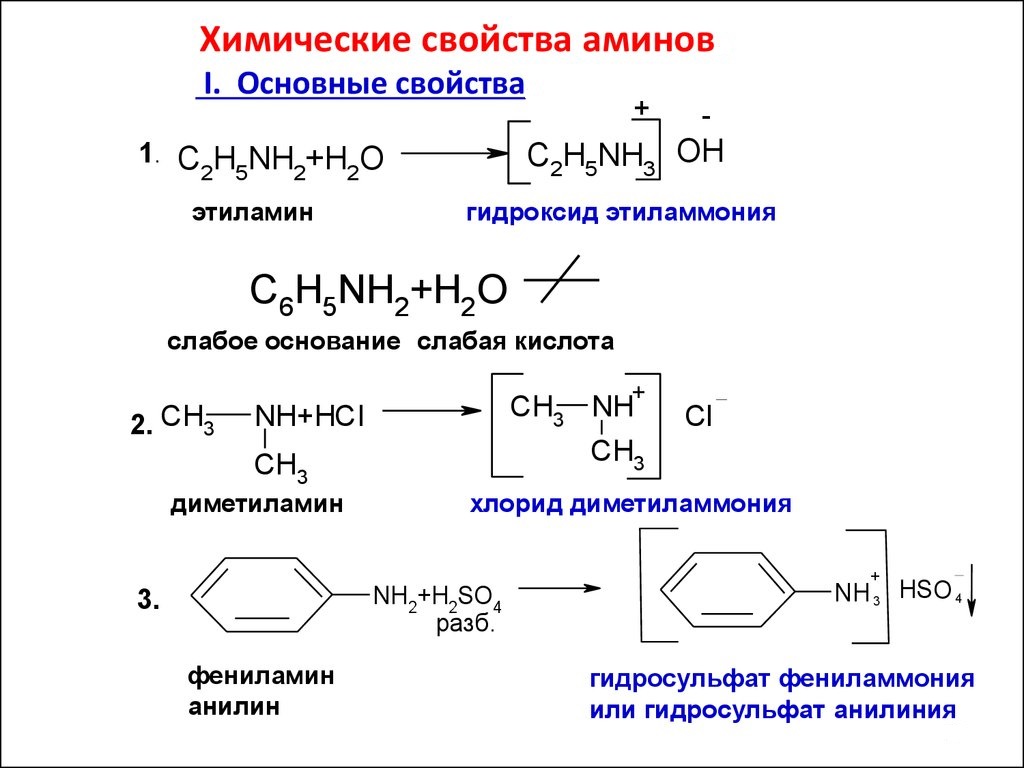
Характеристиката на веществата зависи главно от трансформациите на аминогрупата, в които водещата роля се приписва на неговата самотна електронна двойка. Така както органична материя клас амини са производни на амоняк, те са способни на реакции, характерни за NH 3 . Например, съединенията се разтварят във вода. Продуктите от тази реакция ще бъдат вещества, проявяващи свойствата на хидроксиди. Например, метиламин, чийто атомен състав отговаря на общата формула на наситените амини R - NH2, образува съединение с вода - метиламониев хидроксид:
СН3-NH2 + H20 = [СНЗ-NH3] OH
Органичните основи взаимодействат с неорганични киселини и в продуктите се открива сол. Така метиламинът със солна киселина дава метил амониев хлорид:
CH3-NH2 + НС1 -> [CH3NH3] CI
Реакции на амини, чиято обща формула е R-NH2, с органични киселини заместват водородния атом на аминогрупата със сложен анион на киселинния остатък. Те се наричат реакции на алкилиране. Както при реакцията с нитритна киселина, ациловите производни могат да образуват само първични и вторични амини. Триметиламин и други третични амини не са способни на такива взаимодействия. Добавяме също така, че алкилирането в аналитичната химия се използва за разделяне на смеси от амини, той също служи качествен отговор върху първични и вторични амини. Сред цикличните амини анилинът е важен. Той се извлича от нитробензола чрез редукция на последния с водород в присъствието на катализатор. Анилинът е суровина за производство на пластмаси, багрила, експлозиви и лекарства.

Характеристики на третичните амини
Терциерните амонячни производни се различават по своите химични свойства от едно- или двузаместени съединения. Например, те могат да взаимодействат с халогенни производни на наситени въглеводороди. В резултат се образуват тетраалкиламониеви соли. Сребърен оксид реагира с третични амини, докато амините се превръщат в тетраалкиламониеви хидроксиди, които са силни основи. Може да се образуват апротни киселини, като борен трифлуорид, с триметиламин комплексни съединения.
Качествен тест за първични амини
Азотната киселина може да служи като реагент, с който да се открият едно- или двузаместени амини. Тъй като не съществува в свободно състояние, за да се получи в разтвор, първо се провежда реакция между разредена хлоридна киселина и натриев нитрит. След това се добавя разтвореният първичен амин. Съставът на неговите молекули може да бъде изразен с помощта на общата формула на амините: R-NH 2. Този процес е придружен от появата на молекули на ненаситени въглеводороди, които могат да бъдат определени чрез реакция с бромна вода или разтвор на калиев перманганат. Изонитрилната реакция може да се счита за качествена. В него първичните амини взаимодействат с хлороформ в среда с прекомерна концентрация на хидроксилни аниони. Резултатът е образуването на изонитрили с неприятна специфична миризма.

Характеристики на реакцията на вторични амини с нитритна киселина
Технологията за производство на HNO 2 реагент е описана по-горе. След това към разтвора, съдържащ реагента, се добавя органично амонячно производно, съдържащо два въглеводородни радикали, например, диетиламин, молекулата на който отговаря на общата формула на вторичните амини NH2-R-NH2. В реакционните продукти намираме нитросъединението: N-нитрозодиетиламин. Ако се действа с хлоридна киселина, съединението се разлага на хлоридната сол на изходния амин и нитрозилхлорида. Добавяме също така, че третичните амини не са способни на реакции с азотиста киселина. Това се обяснява със следния факт: нитритната киселина принадлежи към слабите киселини, а нейните соли, когато взаимодействат с амини, съдържащи три въглеводородни радикали, са напълно хидролизирани във водни разтвори.
Начини за получаване
Амините, общата формула на която е R-NH2, могат да бъдат получени чрез редукция на съединения, съдържащи азот. Например, това може да бъде редукция на нитроалканите в присъствието на катализатор - метален никел - при нагряване до + 50 ° С и при налягане до 100 атм. Нитроетан, нитропропан или нитрометан се превръщат в амини в резултат на този процес. Вещества от този клас могат също да бъдат получени чрез редукция на водород на съединения на нитрилни групи. Тази реакция протича в органични разтворители, в присъствието на никелов катализатор. Ако като редуциращ агент се използва метален натрий, в този случай процесът се извършва в алкохолен разтвор. Нека да цитираме като пример още два метода: аминиране на халогеналкани и алкохоли.
В първия случай се образува смес от амини. Аминирането на алкохолите се извършва по следния начин: смес от метанол или пари с етанол с амоняк се прехвърля върху калциев оксид, който действа като катализатор. Получените първични, вторични и третични амини обикновено могат да бъдат разделени чрез дестилация.
В нашата статия изследвахме структурата и свойствата на азотсъдържащите органични съединения - амини.