Правило за пристрастие при радиоактивен разпад
Правилото за предразсъдъци за радиоактивното разпадане в радиохимията и ядрената физика, което също е известно като закона Soddy-Faience, е правилото, което определя трансформацията на един елемент в друг по време на радиоактивен разпад. През 1913 г. то е обяснено самостоятелно от двама учени: английския радиохимик Фредерик Содди и американския физик-химик с полските корени Казимир Фаянс.
Успехите на Фредерик Содди в областта на радиоактивността

Содди, заедно с Ръдърфорд, е начело на откриването на радиоактивни атомни трансформации. Така през 1903 г. Содди открива, че радийът отделя хелиеви ядра по време на неговия разпад. Този учен също показа, че атомите от един и същ химически елемент могат да имат различни маси, което го накара да развие концепцията за изотопите. Soddy определи правилата за отстраняване на химични елементи по време на алфа и бета радиоактивни разпадания, което беше важна стъпка в разбирането на връзката между семействата на радиоактивните елементи.
През 1921 г. Фредерик Содди бе награден Нобелова награда за химия за важни открития във физиката на радиоактивните елементи и за изследване на природата на изотопите.
Произведения на Казимир Фаянс

Този учен проведе важни изследвания на радиоактивността на различни изотопи и разработи квантова теория на електронната структура на молекулите. През 1913 г., едновременно с Фредерик Содди и независимо от него, Фаянс открива правилата за изместване, които управляват превръщането на някои химични елементи в други в процеса на радиоактивни разпадания. Fayans също открили нов химичен елемент, протоктиниум.
Концепцията за радиоактивност

Преди да разгледаме законите на радиоактивния разпад и правилата за изместване, е необходимо да разберем понятието радиоактивност. Във физиката тази дума означава способността на ядрата на някои химически елементи да излъчват радиация, която има следните свойства:
- способност за проникване в човешките тъкани, имащи разрушителен ефект;
- способност за йонизиране на газове;
- стимулиране на флуоресцентния процес;
- преминаване през различни твърди и течни тела.
Поради тези способности тази радиация обикновено се нарича йонизираща. Естеството на радиацията може да бъде или електромагнитно, например, Рентгенови лъчи или гама-лъчение, или да имат корпускуларен характер, емисиите на хелиеви ядра, протони, електрони, позитрони и други елементарни частици.
Така радиоактивността е феномен, наблюдаван в нестабилни атомни ядра, които спонтанно могат да се превърнат в ядра на по-стабилни елементи. С прости думи, един нестабилен атом излъчва радиоактивно лъчение, за да стане стабилно.
Нестабилни атомни изотопи
Нестабилните изотопи, т.е. атомите на същия химически елемент, които имат различни атомни маси, са в възбудено състояние. Това предполага, че те имат повишена енергия, която те се стремят да дадат, за да преминат в равновесно състояние. Като се има предвид, че всички енергии на атома са квантовани, т.е. имат дискретни стойности, тогава самото радиоактивно разпадане се дължи на загубата на специфична кинетична енергия.

Нестабилният изотоп в процеса на радиоактивен разпад става по-стабилен, но това не означава, че новообразуваното ядро няма да има радиоактивност, може да се разпадне. Ярък пример за този процес е ядрото на уран-238, което от няколко века преживява серия от разпадания, превръщайки се в атом от олово. Отбележете, че в зависимост от вида на изотопа, той може спонтанно да се разпадне, както в милионни части от втората, така и в милиарди години, например, един и същ уран-238 има период на полуразпад (време, за което половината от разпадането на ядрата) е равно на 4,468 милиарда години, в същото време, за изотопа калий-35, този период е 178 милисекунди.
Различни видове радиоактивност
Прилагането на определено правило за радиоактивно отклонение зависи от вида на радиоактивния разпад, който изпитва даден елемент. Като цяло се разграничават следните видове радиоактивност:
- алфа разпад;
- бета разпад;
- гама-разпад;
- разпад с излъчване на свободни неутрони.
Всички тези видове радиоактивен разпад (с изключение на излъчването на свободни неутрони) са установени от физик от Нова Зеландия. Ърнест Ръдърфорд от началото на 20-ти век.
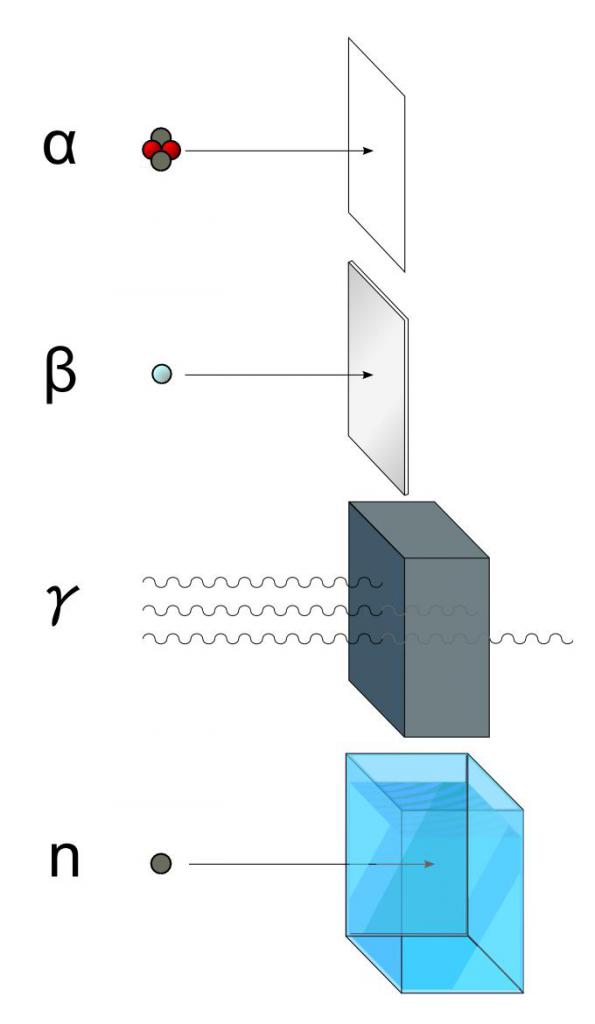
Корпускулни типове гниене
Алфа-разпадът е свързан с излъчването на хелий-4 ядра, т.е. тя е въпрос на корпускуларна радиация, чиито частици се състоят от два протона и два неутрона. Това означава, че масата на тези частици е 4 в атомни единици маса (AEM), а електрическият заряд е +2 в единици на елементарния електрически заряд (1 елементарен заряд в системата SI е равен на 1.602 * 10 - 19 C). Емитираното хелиево ядро преди разпадането е част от нестабилното изотопно ядро.
Естеството на бета-разпадането е емисията на електрони, които имат маса от 1/1800 AEM и заряд -1. Поради отрицателен електронен заряд този разпад се нарича бета-отрицателен. За разлика от алфа-частицата, електронът не съществуваше преди разпадането в атомното ядро, а се формира в резултат на превръщането на неутрон в протон. Последният остава в ядрото след разпадането и електронът напуска атомното ядро.
Впоследствие бе открит бета-позитивен разпад, който се състои в излъчване на позитрон-античастица на електрона. Радиоактивният позитрон се формира в резултат на обратната реакция, отколкото електрона, т.е. протонът в ядрото се превръща в неутрон, загубвайки своя положителен заряд.
При поредица от радиоактивни трансформации на едно ядро в друго, се излъчват неутрони с различни енергии. Подобно на протон, неутронът има маса от 1 AEM (по-точно неутрон е 0.137% по-тежък от протон) и има нулев електрически заряд. По този начин при този вид разпад родителското ядро губи само 1 единица от своята маса.
Гама гниене
Гама-разпадът, за разлика от предишните видове разпад, има електромагнитна природа, т.е. тази радиация е подобна на рентгеновата или видимата светлина, но дължината на вълната на гама-излъчването е много по-малка от тази на всяка друга електромагнитна вълна. Гама лъчите нямат маса за почивка и зареждане. В действителност, гама лъчи - това е допълнителната енергия, която е съществувала преди колапса в ядрото на атома, причинявайки неговата нестабилност. Химичният елемент запазва позицията си в периодичната таблица. Д. И. Менделеев с гама гниене.
Правила за радиопредаване
Използвайки тези правила, лесно можете да определите кой химичен елемент трябва да бъде получен от даден родителски изотоп с определен тип радиоактивен разпад. Ние обясняваме тези правила за пристрастие във физиката:
- С алфа-разпад, тъй като ядрото губи 4 АЕМ маси и +2 единици заряд, се образува химичен елемент, който е 2 позиции вляво в периодичната таблица на Д. И. Менделеев. Например, 92 U 238 = 90 Th 234 , тук индексът е зарядът, а горната е масата на ядрото.
- В случая на бета-отрицателен разпад, зарядът на родителското ядро се увеличава с 1 единица, докато масата остава непроменена (масата на излъчения по време на този разпад електрон е само 0.06% от масата на протона). В този случай правилото за равновесното изместване гласи, че трябва да се образува изотоп на химичен елемент, който стои една клетка вдясно от майчиния елемент в таблицата на Д. И. Менделеев. Например, 82 Pb 212 = 83 Bi 212 .
- Правилото за изместване по време на бета-положителния разпад (излъчване на позитрон) гласи, че в резултат на този процес се образува химически елемент, който е с 1 позиция вляво от основния елемент и има същата маса на ядрото, както и него. Например, 7 N 13 = 6 С 13 .