Квантово-механичен модел на атома и неговата структура
Планетарният квантовомеханичен модел на атома на Бор често се помни за чистата и позната картина на електроните. Те се въртят около централното ядро, като планети около слънцето. Поради това може да бъде трудно да се замени картината на тази, която по-точно представлява квантово-механичния модел на атома, използван от съвременните физици.
Как се движи и движи атомът?
Атомът има малко ядро и вълни от остри орбити. Местоположението и движението на електроните се описва от вълните на тяхната материя. Тези структури предсказват вероятността да се намери електрон в даден регион на атома. Но откъде идва квантово-механичният модел на атома на Бор?
Планетарният модел инициира процеса на въвеждане на квантовата теория в структурата на атома. Бор въвежда идеята за стационарни състояния, в които атомът е стабилен. Преходите между тези състояния обясняват съществуването на спектрални линии. В случай на водород, той е в състояние да получи енергийни нива:
Ad
- Преходите между неговите енергийни нива съответстват на линиите в водородния спектър.
- Неговият модел не може да прогнозира нивата на енергия за други атоми (въпреки че нивата на алкални метали, подобни на водород, могат да бъдат приближени до истината).
Отделно, работата на Хайзенберг и Шрьодингер е извършена, за да се измислят начини за по-пълно описание на квантовите енергийни нива на атомите.
Аналогии на Хайзенберг и Шрьодингер: как те доведоха уравнението до доказателството за вълна
Квантово-механичният модел на структурата на атома има уникален набор от свойства. Хайзенберг използвал матрици, а Шрьодингер разработил вълновото уравнение, за да докаже абсолютността на разликата в поведението на кванта. Двойствеността на частиците е показана по-подробно във видеото.
Ad

Уравненията на Шрьодингер осигуряват представяне на плътността на вероятностите на електроните около ядрото на атома. Повечето определения на квантовата теория и квантовата механика предлагат същото описание и за двете. Те по същество описват квантовата теория, в която както енергията, така и материята имат характеристиките на вълните в някои условия и характеристиките на частиците в други.
За да направят идеята по-ясна, хората започнаха да провеждат експерименти по отношение на умственото обещание.

- Квантовата теория предполага, че енергията идва в отделни пакети, наречени кванти (или, в случай на електромагнитно излъчване, фотони).
- Квантовата теория има някакво математическо развитие, често наричано квантова механика, което предлага обяснения за поведението на електроните вътре в електронните облаци на атомите.
Основните разпоредби на квантово-механичния модел на структурата на атома е двойствеността на електронните вълни в електронния облак, което ограничава способността ни едновременно да измерваме енергията и позицията на електрона.
Скрити черти на електроните
Колкото по-точно измерваме енергията или позицията на електрона, толкова по-малко знаем за другото. Не можем да отбележим точно позицията и инерцията на електрона едновременно. Това прави невъзможно да се предвиди траекторията на частица. Следователно поведението на електрона се описва по различен начин от поведението на частиците с нормален размер. Трябва да знаете:
- Най-често срещаният начин за описване на електроните в атомите в съответствие с квантовата механика е да се реши уравнението на Шрьодингер за енергийните състояния на електроните в този облак.
- Когато един електрон е в тези състояния, неговата енергия е ясно определена и позицията не е.
- Позицията се описва от карта на разпределението на вероятностите, наречена орбитална.
Траекторията, която обикновено свързваме с макроскопични обекти, се замества от електрони в облаци от електрони, а статистическите описания не показват пътя, а областта, в която е намерена. Тъй като електронът в атомния електронен облак определя неговото химично поведение, за да разбере химията, е необходимо да се опише конфигурацията на електроните в ключа на квантово-механичния модел на атома.
Принцип на несигурност на Хайзенберг: областта вътре в атома
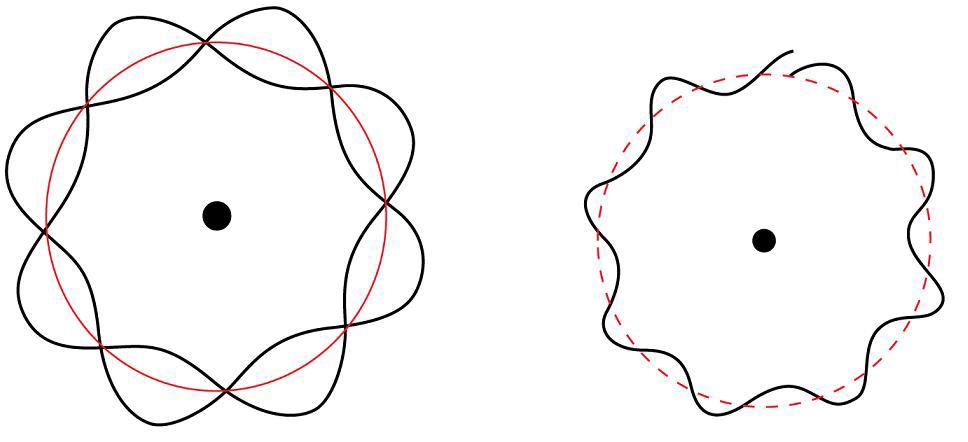
Луи дьо Бройл предлага всички частици да се разглеждат като материални вълни с дължина на вълната - ламбда, дефинирана от следното уравнение:
Lambda = действително време (час) + миливолта час
Ервин Шрьодингер предложил квантово-механичен модел на атома. Накратко: третира електроните като вълни на материята.
Квадратът на вълновата функция представлява вероятността да се намери електрон в дадена област в рамките на един атом. Атомната орбита се дефинира като областта вътре в атома, където е електрона.
Принципът на несигурността на Хайзенберг гласи, че не можем да знаем нито енергията, нито позицията на електрона. Следователно, когато научим повече за позицията на електрона, знаем по-малко за неговата енергия и обратно. Електроните имат присъщо свойство, наречено спин. Всеки два електрона, заемащи една и съща орбита, трябва да имат противоположни завъртания.
Ad
Светлинен етер в квантовия свят
Природата на светлината е предмет на изследване още от древността. През седемнадесети век Исак Нютон провежда експерименти с лещи и призми. Той успя да докаже, че бялата светлина се състои от отделни цветове на дъгата, комбинирани заедно. Нютон обяснява резултатите от своята оптика с "корпускуларен" изглед на светлината, в който светлината се състои от потоци изключително малки частици, движещи се с високи скорости в съответствие с законите на Нютон за движение. Трябва да се отбележи:
Кристиан Хюйгенс показа, че оптичните явления като отражение и пречупване могат да бъдат обяснени еднакво добре от гледна точка на светлината като вълни, движещи се с висока скорост през среда, наречена „светещ етер“. Тя прониква в цялото пространство.
Ad
В началото на деветнадесети век Томас Янг демонстрира, че светлината, минаваща през тесни, тясно разположени процепи, създава интерференционни модели, които не могат да бъдат обяснени от гледна точка на нютоновите частици, но могат лесно да се интерпретират от гледна точка на вълните.
- По-късно, през деветнадесети век, след като Джеймс Клерк Максуел разработи своята теория за електромагнитното излъчване и показа, че светлината е видима част от огромния спектър от електромагнитни вълни, гледната точка на частицата на светлината става напълно дискредитирана.
Днес тези области се наричат класическа механика и класическа електродинамика (или класически електромагнетизъм).
Как напредва идеята за въвеждане на нови концепции във физиката

В края на деветнадесети век учените видяха, че физическата вселена е приблизително съставена от две отделни области:
- материя, образувана от частици, движещи се съгласно законите на Нютон за движение;
- електромагнитно излъчване, състоящо се от вълни, контролирани от уравненията на Максуел.
Парадоксите доведоха до модерната структура на квантово-механичния модел на атома Шрьодингер, който тясно свързва частици и вълни на фундаментално ниво, наречен дуалността на вълновата частица, която замени класическия поглед.
Дискретна вълна на Бор: как се държат емисионните спектри на водорода
Според модела на Бор, емисионните спектри на различни елементи съдържат дискретни линии. Видимата област на емисионните спектри на водорода може да бъде представена с помощта на таблицата.
Ad
| Основен квантов номер | Брой поднива | Брой на електроните |
| 1 | 1 | 2 |
| 2 | 2 | 8 |
| 3 | 3 | 18 |
| 4 | 4 | 32 |
Това е схематично представяне на квантите, където е известен броят на електроните и нивата. В живота във вакуумни условия е невъзможно да се каже със сигурност, че има ограничение на поднива, но не може да има повече от 7. Квантованите емисионни спектри показват, че Бор може да съществува вътре в атома само при определени атомни радиуси и енергии.

Чрез конструиране на модел, Бор извлича уравнение, което правилно предвижда различни енергийни нива в водороден атом. Квантово-механичният модел е подходящ само за представяне на този конкретен случай. Нивата съответстват на емисионните линии в спектъра на веществото.
Модел на Бор, който е доказал едно-електронните водородни системи
Скоростта на електроните при енергийното ниво на основното състояние на водорода е 2,2 × 10 6 s ÷ m, където s е дължината, m е масата. Можем да заместим константа, както и масата и скоростта на електрона в уравнението на де Бройл. Но в същото време не можеше да обясни електронната структура в атомите, съдържащи повече от един електрон.
Ако се обърнем към химията, квантово-механичният модел на водородния атом трябва да се състои само от протони. Когато се срещат с електрони или неутрони, частицата започва да се държи като вълна. В други случаи атомите на друго вещество могат, независимо от структурата, да се държат като вълни или частици. Накратко, квантово-механичният модел на водородния атом е материалният дуализъм на вълната, но не и частица.
Припокриване на вълни едно върху друго: как пътеките на пресичане на атоми не се смесват
Радиовълните от мобилен телефон, рентгеновите лъчи, използвани от зъболекарите, енергията, използвана за готвене във вашата микровълнова фурна, лъчистата топлина от горещите обекти и светлината от телевизионния екран са всички форми на електромагнитно излъчване, които показват вълноподобно поведение. Трябва да запомните:
- Вълната е колебание или периодично движение, което може да прехвърля енергия от една точка на пространството към друга.
- Разклащането на края на въжето прехвърля енергия от ръката ви към другия край на въжето; падането на камъче в езерото води до разпространение на вълни по повърхността на водата; разширяването на въздуха, което съпътства мълния, генерира звукови вълни (гръмотевици), които могат да пътуват за няколко мили.
- Във всеки от тези случаи кинетичната енергия се предава чрез веществото (въже, вода или въздух), докато веществото остава на място.
Вълните не трябва да се ограничават до пътуване по материя. Както показа Максуел, електромагнитните вълни се състоят от електрическо поле, осцилиращо във времето с перпендикулярно магнитно поле. Те са перпендикулярни на посоката на движение. Тези вълни могат да преминат през вакуум с постоянна скорост от 2.998 × 108 m / s, където c е скоростта на светлината.