Физични свойства на сероводорода и неговото приложение
Сред всички химически съединения, познати в съвременния свят, има няколко, които могат да бъдат разграничени, може би дори най-необразованият човек знае за тяхното съществуване. Защо тези елементи и съединения са толкова популярни? Това е просто - те се намират навсякъде. Тези съединения включват сероводород.
Относно връзката
Анализът на всяко съединение започва с изучаването на неговата структура. Това е структурата, която определя физичните и химичните свойства на сероводорода. Молекулата на това вещество съдържа само 3 атома: 2 водород и 1 сяра. Свързващи компоненти ковалентни полярни връзки, поради неметалната природа на съединението. Структурата на молекулата се отнася до ъгловата, която е доказана от учените след кратко проучване. Ъгълът е 92 градуса, което е малко по-различно от структурата на водната молекула.

Физични свойства
Всеки човек, анализирайки ново вещество за себе си, на първо място насочва вниманието си към физическите си свойства: физическо състояние, цвят, мирис и т.н. Може би трябва да започне с миризмата на сероводород, тя е известна на всички - развалени яйца. Разбира се, никой не може да го нарече приятен. Какви са физичните свойства на сероводорода, въпреки разпространението му, е известно само на тези, които работят с него или усърдно посещават училище. При стандартни условия веществото има газообразна структура. Би било голямо пропуск да се опишат физическите свойства на сероводорода и да не говорим за промяната на свойствата му при температури над 20 градуса по Целзий, защото при тези условия е възможно пълно разтваряне на сероводорода с вода. Водата, съдържаща това съединение има леки киселинни свойства, дисоциацията има постепенна природа.

За човек веществото е доста опасно - това е вид отрова, дори и в малки количества. Една десета от процента от сероводородния газ може да доведе до парализа на дихателните пътища на човека, което е фатално за 8 минути (това е времето, през което мозъкът може да живее без нов кислород).
Токсичните свойства на сероводорода се отнасят за всички същества, чиято кръв съдържа хемоглобин. Желязото, което се съдържа в големи количества в червените кръвни клетки, много лесно реагира с молекулите на сероводорода, за да образува сулфид, който не може да пренася кислород.
Противоотровата за сероводорода е много проста - просто трябва да вдишвате въздух, наситен с кислород и да имате лека смес от хлор, която неутрализира действието на сярата. Експериментите и изследванията, свързани с сероводорода, трябва да се извършват при специални условия.
Производство на сероводород
Реакцията на получаване на сероводород най-често се извършва в присъствието на затворен изпарителен шкаф, който намалява възможността за отравяне на учените. При тази реакция чистият водород и сярата взаимодействат помежду си, без да оставят никакви остатъчни продукти.

Производство на сероводород
В училищата сероводородът се използва по-често за получаване на опит, който не е свързан с риск за здравето на учениците. Реакцията се провежда, като се използва железен (II) сулфид и разтвор на една от киселините, сярна или солна. За да постигнете гарантиран резултат, ще ви е необходим чифт сулфидни парчета с размера на обикновен грах. Следващата стъпка ще бъде да се напълни тръбата с разтвор на киселина до половината, след това тръбата трябва да бъде затворена. тръба за изпускане на газ поставете под капака и загрейте. Ако реакцията продължи, се отделят малки газови мехурчета. Този метод за получаване на сероводород е ефективен само за производство на малко количество газ.
Веществото може да се получи и при използване на метално желязо и кристална сяра. Полученият сулфид по време на реакцията, за пълното придобиване на физичните свойства на сероводорода, трябва да се смеси със сярна киселина.
Химични свойства
Сероводородът реагира с кислорода, пламъкът придобива син оттенък при изгаряне на сероводород. При пълно изгаряне на продукта се образува серен оксид и вода. Полученият оксид е разтворим във вода и разтворът придобива слаби киселинни свойства. Показателят за този процес е лакмусова хартия който е оцветен в контакт със субстанцията в синьо. По този начин е обичайно да се получава сяра в промишлен мащаб.
При взаимодействие с халогени и соли се появяват достатъчно силни редуциращи свойства на веществото, което се отнася както до химични, така и до физични свойства. В лабораторни условия бромът и хлорът се използват за провеждане на експеримента и наблюдение на реакцията на взаимодействието на сероводорода с халогените. Продуктът от тази реакция ще бъде кристална сяра.
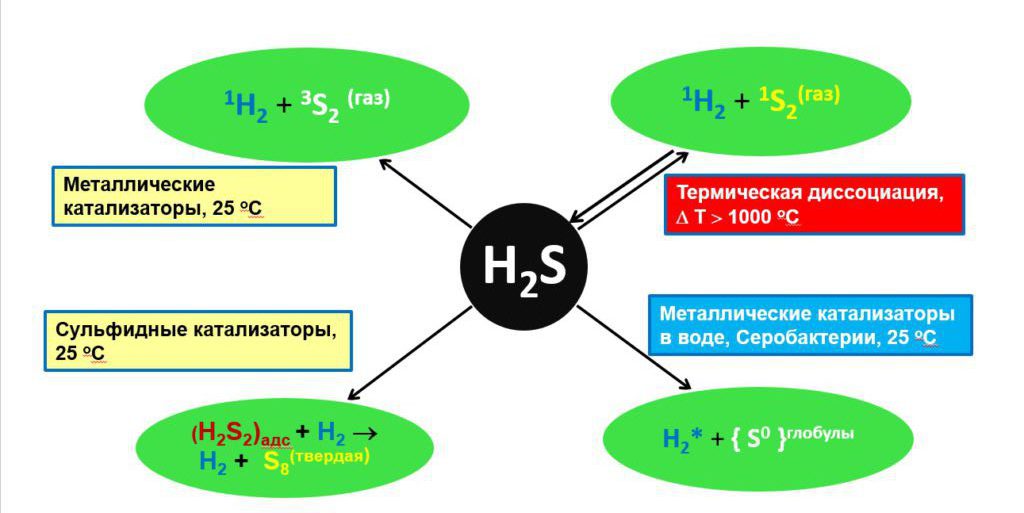
Реакцията на вода и сероводород води до образуване на хидроксиден катион. В допълнение, съединението има способността да образува други вещества - сулфиди и хидросулфиди. Съединения на алкалоземни и алкални метали реагират с сероводород, за да образуват безцветни вещества, докато в същото време реакцията с тежки метали провокира появата на черна субстанция.
приложение
Беше открита сяра - едно от първите вещества, чието свойство се запалва. Веществото, наред с други неща, се добавя към обикновения природен газ, който е във всяка кухня. Физическите свойства на сероводорода и неговото използване са доста обширни, поради което много хора са чували за това вещество. Водородният сулфид преди това се използва като отрова за насекоми и вредители, но се отстранява от производството поради много случаи на човешко отравяне. Поради токсичността на съединението, трябва да се работи изключително внимателно.

В природата веществото се среща често. Това е резултат от гниещи продукти на телата на различни животни, газът често се намира в разтворена форма в естествените води. Трудно е да се опишат всички физични свойства на сероводорода, тъй като има много такива. Основните са описани по-горе. Използването на сероводород в промишлеността също е много широко. някои химични експерименти промишлените процеси изискват присъствието му.