Принципът на Паули във физиката и химията: особености на приложението
Историята на атомната физика има много възходи и падения. Но благодарение на техническия прогрес, всяко предположение, възникнало в умовете на теоретиците, може да бъде тествано в лабораторията. Тъй като много аспекти на поведението на елементарните частици все още не са податливи на законите на логиката, учените-откриватели на микросвета са се съгласили да ги приемат "както е", без да обясняват причините. Принципът на Паули се отнася до резултатите от онези експерименти, които все още не са намерили единственото им обяснение.
Противоречия в атомната теория
Едно от най-често срещаните погрешни схващания в атомната физика е планетарният модел на атомите, предложен от английски учен. Ърнест Ръдърфорд. В крайна сметка се оказа, че не е напълно надеждна, но направи възможно да се направят толкова правилни заключения, че ползите от нея са безспорни. 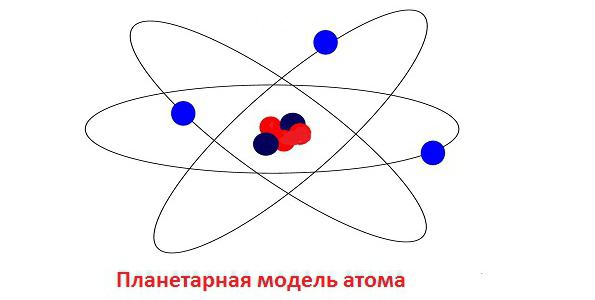 Едно от основните противоречия на атома Ръдърфорд е способността на електроните да излъчват. В резултат на загубата на енергия, всеки електрон в крайна сметка трябваше да спре движението си и да падне в ядрото. Но всеки атом (с изключение на един радиоактивен) е по същество стабилен, може да съществува за произволно дълго време и не показва никакви признаци на самоунищожение. За да реши този проблем, той взе таланта на блестящия датски физик Нилс Бор.
Едно от основните противоречия на атома Ръдърфорд е способността на електроните да излъчват. В резултат на загубата на енергия, всеки електрон в крайна сметка трябваше да спре движението си и да падне в ядрото. Но всеки атом (с изключение на един радиоактивен) е по същество стабилен, може да съществува за произволно дълго време и не показва никакви признаци на самоунищожение. За да реши този проблем, той взе таланта на блестящия датски физик Нилс Бор.
Борска теория
През 1913 г. младият непознат физик от Дания предложи да включи две промени в класическата физика, с които беше възможно да се обяснят фактите от наблюденията и да се направят много полезни открития. Бор не може да обясни причината за поведението на електроните в орбита, така че принципът на "както е" е поставен в основата на неговите правила. Тези правила по-късно служеха на добра служба и проправиха пътя за нови открития.
Правила на Бор

Първото правило беше това планетарен модел на атома, предложено от Ръдърфорд, все още е вярно. Но електроните в него се движат в орбитите си без радиация. Второто правило на Бор твърди, че движението на електроните е възможно само по определени "разрешени" орбити. За електрон, който се движи по разрешена орбита, произведението на импулса и радиуса на тази орбита винаги е кратно на константата на Планк. Така електронните орбити могат да бъдат разположени само върху тях енергийни нива за което важи следното правило:
(електронен импулс * обиколка на орбитата) = n * h,
където h е постоянна дъска, а n е естествено число. Така, с най-малката разрешена орбита, n = 1. Третото правило гласи, че електроните на атомите могат да бъдат преместени (например чрез бомбардиране с тежки частици) на свободна външна орбита. След това електронът може да се върне към свободна вътрешна орбита. В този случай атомът излъчва излишък от енергия под формата на квантова светлина.
Квантови граници
Квантовото правило на Бор приема, че електроните, които са най-близо до ядрото, имат най-малката допустима орбита. На това ниво електронът има минимална енергия. Може да се очаква, че всички електрони в един атом ще трябва да заемат тази орбита и да останат на това ниво. Това обаче не се случва. Принципът на Паули помогна да се обясни това противоречие.
Волфганг паули
Този известен австрийски физик е роден във Виена през 1869 година. В Мюнхенския университет той получава отлично цялостно образование, но посвещава всичките си научни разработки на квантовата физика. На двадесетгодишна възраст Паули написал статия за преглед на Физическата енциклопедия, много страници от които все още са актуални и днес. Неговите научни статии рядко се публикуваха, най-важните му мисли и хипотези се изразяваха в кореспонденция с неговите научни колеги. Най-оживена е кореспонденцията с Н. Бор и В. Хайзенберг. Това беше съвместната работа на тези трима учени, които положиха основите на съвременната квантова физика. Въз основа на експерименталните данни на тези трима изтъкнати учени, Паули формира свой собствен принцип. За него през 1945 г. австрийският учен получи Нобелова награда.
Електронно движение
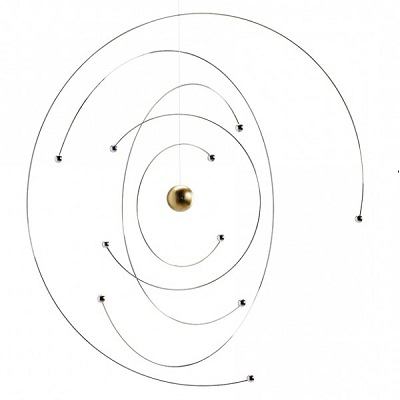
Изследвайки движението на електрона, В. Паули среща много странни моменти в поведението на тази елементарна частица. Например, когато се движат, електроните се държат така, сякаш се въртят около оста си. Подходящият момент на въртене на електрона се нарича спин. На едно място в орбита могат да се поберат два електрона и техните завъртания трябва да са противоположни. един към друг като принципа на Паули. Физиката на това ограничение е валидна не само за електрони, но и за други частици с полуцелова спинова стойност.
Периодичната система и принципът на Паули
Химията използва принципа на несигурност, за да обясни вътрешната структура на веществата. Сега става напълно разбираемо защо в първия ред на периодичната таблица има само два елемента. Както водородът, така и хелийът разполагат с една по-ниска орбита, в която има само едно двойно място за електрони с противоположни завъртания. Следващата орбита съдържа осем такива места. Следователно вторият ред на периодичната система успява да вземе осем елемента. Този модел обхваща всички серии на периодичната система. 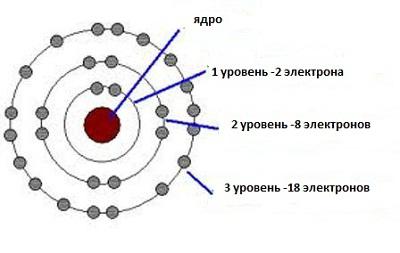
Физика на звездите
Колкото и да е странно, законите на поведението на елементарните частици се простират далеч отвъд микросвета. Например, звездната физика се занимава с вътрешния свят на стареещите звезди. Принципът на Паули работи тук, само че се разбира малко по-различно. Сега това правило казва, че в определен пространствен обем има възможност да се установи само до две елементарни частици с противоположни завъртания. Особено ясно този закон е валиден при наблюдение на стареещите звезди. Както знаете, след експлозията звездата на суперновата бързо се срива, но не всички звезди се превръщат в черни дупки. С увеличаване на прага на ограничителната плътност (и за старееща звезда тази стойност е от порядъка на 10 7 kg / m 3 ), вътрешното налягане на космическото тяло бързо нараства. Този процес има специален научен термин - налягането на изроден електронен газ. Така звездата спира да губи обема си и се превръща в малко небесно тяло с размерите на нашата Земя. Такива звезди в астрофизиката се наричат бели джуджета.
резултати
Принципът на несигурността е един от първите закони на новия тип, който се различава от всички идеи за света, около който знаем. Новите закони са фундаментално различни от правилата на класическата физика, позната ни от детството. Ако старите правила говорят за това какво може да се случи, когато се предприемат определени действия, тогава законите на нов тип показват, че нещо не трябва да се случва.

Алгоритмите за решаване на много проблеми трябва да се основават на леко модифицирания принцип на Паули. Прекъсвайки в самото начало невъзможни решения на проблемите, има шанс да намерим единствения верен отговор. Практическото използване на принципа на неопределеност значително намалява времето, необходимо за компютърна обработка на информацията. По-рано известен само в кръга на теоретичните физици, принципът на Паули отдавна е излязъл извън границите на квантовата физика, като по този начин обозначава нови методи за изучаване на законите на природата.