Изотопи на водород: свойства, характеризиране и приложение
Всеки химичен елемент има разнообразие от естествен или изкуствен произход, наречен изотопи. Разликата между тях се състои в неравния брой неутрони в ядрата и следователно в атомното тегло, както и в степента на стабилност. Що се отнася до броя на протоните, това е същото, поради което елементът всъщност остава. В тази статия се обръщаме към изотопите на водорода - най-лекия и най-често срещан елемент във Вселената. Трябва да разгледаме техните свойства, тяхната роля в природата и областта на практическото приложение.
Колко вида има водородът?
Отговорът на този въпрос зависи от това какви са изотопите на водорода.
За този елемент са установени три естествени изотопни форми: протий - лек водород, тежък деутерий и супер тежък тритий. Всички те се намират в естествена форма.
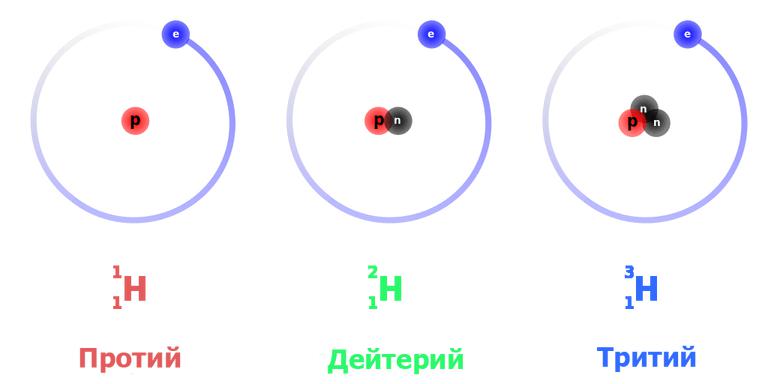
Освен тях, има четири изкуствено синтезирани изотопа: кадиум, пентиум, хексиум и септиа. Тези видове се характеризират с изключителна нестабилност, времето на живот на техните ядра се изразява със стойности от порядъка на 10 -22 - 10 -23 секунди.
Така, днес всички седем изотопни вида са известни от водорода. Ще насочим вниманието си към три от тях от практическо значение.
Лек водород
Това е най-простият атом. Водородният изотоп протий с атомна маса 1.0078 а. E. m. Има ядро, което се състои само от една частица - протон. Тъй като е стабилен (теоретично времето на протона се оценява на не по-малко от 2,9 × 10 29 години), алуминиевият прот също е стабилен. При записване на ядрени реакции тя се обозначава като 1 H 1 (индексът е атомният номер, т.е. броят на протоните, горният е общият брой на нуклоните в ядрото), понякога просто p - „протон“.
Ad
Лекият изотоп е почти 99,99% от целия водород; само малко повече от стотен процент представлява другите форми. Протиум прави решаващ принос за преобладаването на водород в природата: във вселената като цяло, около 75% от масата на барионната материя и около 90% от атомите; на Земята - 1% от масата и до 17% от атомите на всички елементи, които съставляват нашата планета. Като цяло, protium (по-точно, протонът като един от основните компоненти на Вселената) може безопасно да бъде наречен най-важният елемент. Тя осигурява възможност за термоядрен синтез в дълбините на звездите, включително и на Слънцето, и поради това се формират други елементи. Освен това лекият водород играе важна роля в изграждането и функционирането жива материя.
Ad

В молекулярна форма водородът влиза в химични взаимодействия при високи температури, тъй като разделянето на достатъчно силна молекула изисква много енергия. Атомният водород се характеризира с много висока химична активност.
деутерий
Тежкият изотоп на водорода има по-сложно ядро, състоящо се от протон и неутрон. Съответно атомната маса на деутерия е два пъти по-голяма - 2,0141. Приетото обозначение е 2 H 1 или D. Тази изотопна форма също е стабилна, тъй като в процесите на силно взаимодействие в ядрото протонът и неутронът постоянно се превръщат един в друг и последният няма време да претърпи гниене.
На Земята водородът съдържа от 0,011% до 0,016% деутерий. Концентрацията му варира в зависимост от околната среда: в морската вода този изотоп е по-голям, а в състава на, например, природния газ - значително по-малко. На други тела на Слънчевата система съотношението на деутерий към светли водород може да бъде различно: например, ледът на някои комети съдържа по-голямо количество тежък изотоп.
Ad
Деутерият се топи при 18,6 K (лек водород при 14 K) и кипи при 23,6 K (съответната протиева точка е 20,3 K). Тежък водород показва, по принцип, същите химични свойства като протий, образувайки всички характерни типове съединения за този елемент, но някои характеристики, свързани със сериозна разлика в атомната маса, са присъщи за него, защото деутерият е 2 пъти по-тежък. Трябва да се отбележи, че по тази причина изотопните форми на водорода се характеризират с най-големите химически разлики между всички елементи. По принцип по-ниските стойности (5-10 пъти) на реакциите са характерни за деутерий.
Ролята на деутерия в природата
Ядрата от тежък водород участват в междинните етапи на термоядрения цикъл. Слънцето свети благодарение на този процес, на един от етапите, на които се образува водороден изотоп деутерий, който се слива с протон, и се получава хелий-3.
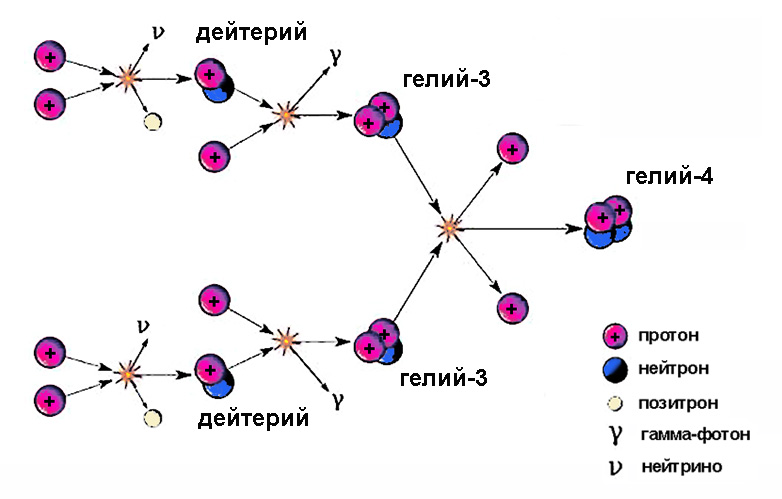
Водата, която включва, освен протий, един атом деутерий, се нарича лек тежък и има формулата HDO. В молекулата на тежката вода D2O, деутерият напълно замества лекия водород.
Тежка вода характеризиращи се с бавен ход на химични реакции, в резултат на което във високи концентрации е вредно за живите организми, особено за по-висшите, като бозайниците, включително хората. Ако водата съдържа една четвърт водород, заместен от деутерий, продължителното му използване е изпълнено с развитие на безплодие, анемия и други заболявания. При замяна на 50% от водорода бозайниците умират след една седмица консумация на такава вода. Що се отнася до краткосрочното увеличение на концентрацията на тежък водород във водата, то е практически безвредно.
Ad

Как да получите тежък водород
Най-удобният начин да се получи този изотоп в състава на водата. Има няколко начина за обогатяване на водата с деутерий:
- Ректификацията е процесът на разделяне на смеси на компоненти, които кипят при различни температури. Разделянето се постига чрез многократно изпаряване и кондензация на смес от изотопи в течен водород или вода на специално оборудване - дестилационни колони, в които газообразните и течните фази текат в противоположни посоки.
- Електролитно разделяне. Методът се основава на факта, че електролиза на водата лекият изотоп се разцепва по-активно от неговите молекули. Електролизата се извършва на няколко етапа.
- Ion изотопен обмен, при който има взаимна замяна на йони с различни изотопи в състава на реагентите. Понастоящем този метод, използващ вода и сероводород като реагенти, е най-ефективният и икономичен.

тритий
Свръхтежкият изотоп на водорода, в ядрото на който има протон и два неутрона, има атомна маса от 3 016 - приблизително три пъти повече от тази на протий. Тритий се обозначава със символа Т или ЗН1. То се топи и кипи при още по-високи температури: съответно 20,6 K и 25 K.
Той е радиоактивен нестабилен изотоп с период на полуразпад 12.32 години. Тя се формира при бомбардиране на ядрата от атмосферни газове, например азот, частици от космически лъчи. Разпадането на изотопа настъпва с излъчването на електрон (т.нар. Бета-разпад), докато един неутрон в ядрото преминава в протон, а химичният елемент повишава атомния номер с един, превръщайки се в хелий-3. В природата тритийът присъства в следи - много малък.
Ad
Супер-тежък водород се образува в ядрени реактори с тежка вода, когато деутерият се улавя от бавни (топлинни) неутрони. Част от него е достъпна за извличане и служи като източник на тритий. Освен това той се получава като продукт на разпадане на литий, когато се облъчва с топлинни неутрони.
Тритий се характеризира с ниска енергия на разпадане и представлява известна радиационна опасност само когато влезе в организма с въздух или храна. Гумени ръкавици са достатъчни, за да предпазят кожата от бета лъчение.
Използване на водородни изотопи
Лекият водород се използва в много индустрии: в химическата промишленост, където се използва за производство на амоняк, метанол, солна киселина и други вещества, в рафинирането на нефт и металургията, където е необходимо да се възстановят огнеупорни метали от оксиди. Използва се и на някои етапи от производствения цикъл (в производството на твърди мазнини) в хранителната и козметичната промишленост. Водородът е един от видовете ракетно гориво и се използва в лабораторните практики в науката и промишлеността.
Деутерият е незаменим в ядрената енергия като отличен неутронен модератор. Той се използва в този капацитет, както и като охлаждаща течност в реактори с тежка вода, което позволява използването на природен уран, което намалява разходите за обогатяване. Той, заедно с тритий, е компонент на работната смес в термоядрени оръжия.

Химичните свойства на тежкия водород дават възможност да се използва при производството на медицински препарати, за да се забави тяхното елиминиране от организма. И накрая, деутерият (като тритий) има перспективи за качество на горивата в термоядрената енергия.
Така че виждаме, че всички изотопи на водорода са някак си „в бизнеса” както в традиционните, така и в високите технологии, с оглед на бъдещето на технологиите, технологиите и научните изследвания.