Глицерин: структурна формула, свойства и приложения
Това е най-простият триатомен алкохол. Химичната формула на глицерола е C3H5 (OH) 3 . Тя е чиста вискозна течност. Без мирис, сладък на вкус. Тя не е отровна, затова се използва широко в ежедневието, хранително-вкусовата промишленост, козметиката и медицината. Структурната формула на глицерола е показана на фигурата. Но как се извлича?
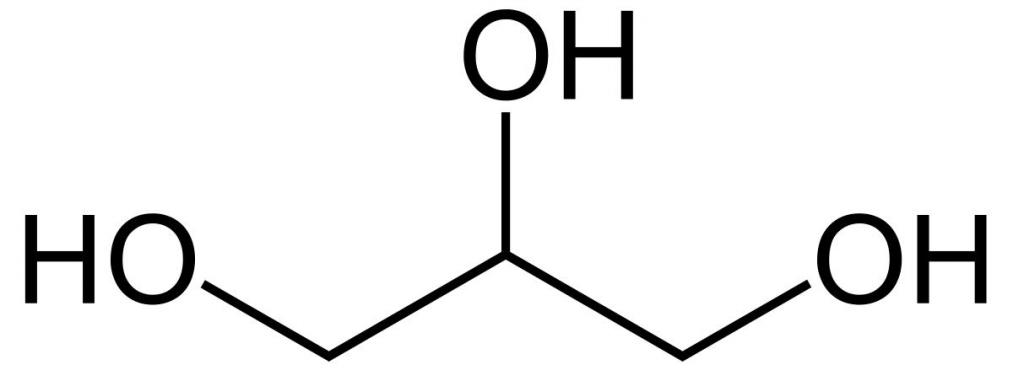
Начини за получаване на глицерин
Почти целият глицерол се извлича от мазнините. От химическа гледна точка те са естери на глицерола. По време на осапуняването на тези мазнини (сапун) се образува глицерин като страничен продукт. След това е много лесно да се откроява от реакционната смес.
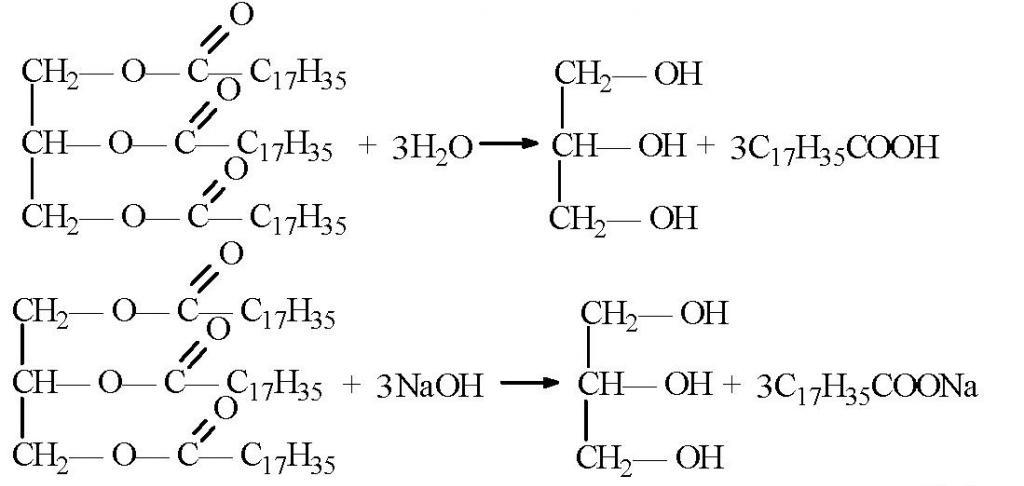
Възможно е да се синтезира глицерин по други начини. Например, от ацетон. В този случай той се редуцира с водород до получаване на изопропилов алкохол. На следващия етап водната молекула се разцепва чрез дехидратация, за да се получи пропилен, който след това се хлорира. Полученият дихлоропропан се хлорира още веднъж, за да се получи трихлоропропан. Последният етап от производството на глицерол е хидратиране при нагряване. На този етап, всичките три молекули на хлор се заменят с хидроксилни групи. По подобен начин сега в индустрията се получава синтетично вещество. Само като суровина се използва пропилен, който се отделя от страничните газове по време на дестилацията на маслото.
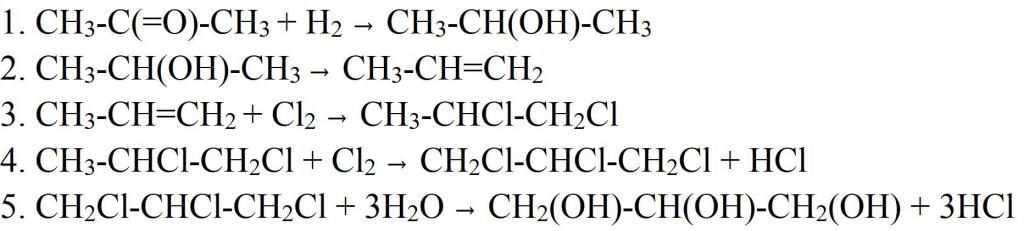
Но от пропилена, за да се получи глицерин може да бъде друг начин. За тази цел пропиленът се окислява до акролеин. Окисляването се извършва с въздушен кислород в присъствието на катализатор (мед) и повишена температура. След това към него се добавя водороден пероксид, за да се получи дихидриден алдехиден алкохол. Като катализатор за тази реакция се използва осмиев оксид (VIII). Алдехидната група в полученото съединение се хидрогенира, превръщайки я в трета хидроксилна група. Така се оказва, глицерин.
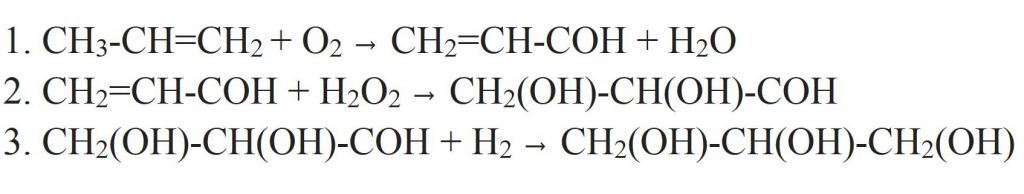
Друга версия на синтеза наведнъж предложи Е. Е. Вагнер. Чрез окисляване на алилов алкохол с калиев перманганат в алкална среда, глицеролът може да бъде получен в един етап.
Физични свойства
Глицеринът е безцветна течност без мирис със сладникав вкус. Той е хигроскопичен, т.е. има тенденция да абсорбира вода. При температура от 20 ° С се топи, а при температура 290 ° С се загрява с частично разлагане. Смесва се с вода и алкохоли във всяко съотношение. Това се дължи на химическата формула. Хидроксилните групи позволяват на глицерола да образува много водородни връзки с водни молекули. Това осигурява разтваряне.
Ad
Да се разтвори глицерин и в ацетон и някои други органични вещества. Неразтворим в бензен и етери. Самият той може да бъде такъв за много органични и неорганични съединения. Неговата плътност в течно състояние е 1.26 g / cm 3 . Също така трябва да се отбележи, че глицеринът е много вискозна течност. Имотът е 1474 пъти повече от водата.
Химични свойства
Идват от структурна формула глицеринът съдържа три хидроксилни групи. Следователно, за него ще бъдат характерни химични реакции на едноосновните алкохоли. Освен това киселинните свойства на глицерола са много по-силни от тези на всеки друг едноокисен алкохол. Така че, тя може да взаимодейства с метали, техните оксиди или основи. По-долу са представени уравненията на химичните реакции на глицерола.
Ad
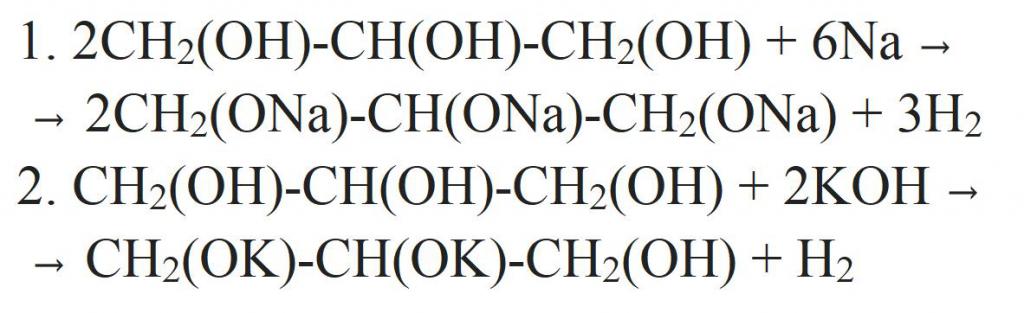
Той може също да влезе в реакции на дехидратация, образувайки много различни продукти. Така че получавате акролеин.
Отделно, трябва да се каже за заместването на хидроксилна група с халоген. Това може да се случи, когато глицеринът взаимодейства с водороден халогенид. Както може да се види от структурната формула на глицерола, в резултат на реакцията могат да се образуват моно-, ди- и три-производни. По-пълно заместване може да се постигне, ако взаимодействието се извършва с фосфорен халогенид.
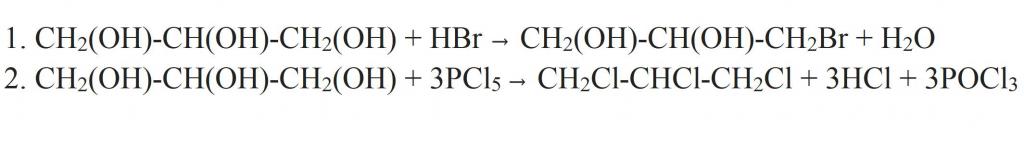
Но глицеринът има специфични свойства, които са уникални за многоатомните алкохоли. Например, взаимодейства с меден (II) хидроксид, за да образува сложно съединение от син цвят - меден глицерат. Тази реакция е качествена за всички полиалкохоли.
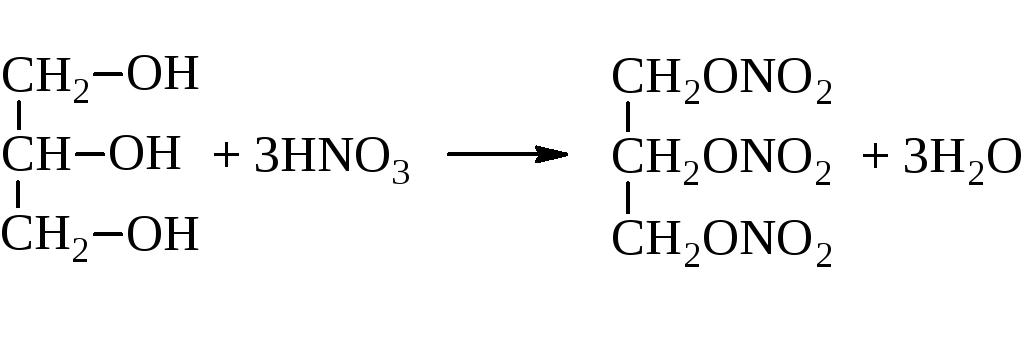
Символи за него и реакция на естерификация. Това е реакцията на взаимодействие с киселини, което води до естер. Освен това, глицеринът е естерифициран с органични и минерални киселини. Например, азотна. Тази реакция се нарича нитриране. В резултат на това се оказва много полезен, но изключително експлозивен продукт - нитроглицерин. От структурната формула на глицерола може да се види, че не всички хидроксилни групи могат да бъдат ерифицирани. Всичко зависи от условията на реакцията.
Ad
При взаимодействие с водород при високо налягане и в присъствието на катализатори се намалява една от хидроксилните групи. В резултат на реакцията се получава дихидричен алкохол - пропиленгликол.
Глицеринът може също да влезе в реакции на поликондензация, образувайки смес от полиглицероли. За това тя се загрява за много дълго време до почти 300 ° C в слабо алкална среда. Разглежда се химичната формула на глицерина.
окисляване
Глицеринът има много възможности за окисление. Крайният продукт зависи от природата на окислителя, катализаторите и други реакционни условия. По този начин, глицеринът може да бъде окислен от силни окислители, например, калиев дихромат в кисела среда. В резултат на тази реакция целият глицерин се разлага на въглероден диоксид и вода.
Ad
Окисляването може да настъпи по-внимателно. Например, чрез взаимодействие с водороден пероксид се получава алдехид или кетон. Като катализатор се използват желязо (II) соли.
Може да се извърши окисляване, за да се получи глицеринова киселина. В този случай взаимодействието се осъществява с концентрирана азотна киселина. Една от хидроксилните групи се окислява просто до карбоксилната група. По-екзотични киселини се получават също от глицерин. При взаимодействие с разтвор на калиев перманганат се образуват тартронни и мезоксални киселини. И когато се окисляват с въздушен кислород с нагряване в присъствието на бариев хидроксид, се получава смес от оксалова и мравчена киселина. Глицеринът на йодна киселина може да бъде окислен до мравчен и формалдехид.
Промишлени приложения
Поради своя състав и свойства, глицеринът се използва в промишлеността.
- В текстилната промишленост тя се използва за изработване на меки и еластични тъкани, както и за синтез на багрила и синтетични влакна.
- Използва се при производството на определени видове хартия.
- В кожарската промишленост решенията му се използват за дъбене и угояване на кожа.
- В селското стопанство семената се третират с глицерин, за да се осигури по-стабилна кълняемост.
- В производството на бои глицеринът се използва за синтез на полиращи съединения и лакове.
- При производството на опаковъчни материали, като целофан, той се използва като пластификатор.
- За опаковане се използват полимери на основата на глицерин. Хартията, напоена с глицерин, придобива огнеустойчивост.
Приложение в хранително-вкусовата промишленост
Глицеринът е хранителна добавка E422. Използва се като стабилизатор за запазване и повишаване на вискозитета на продуктите. Използва се при производството на хлебни и сладкарски изделия (особено шоколад) като сгъстител и влагозадържащ агент. Помага да се добави обем към готовите продукти. Благодарение на тази добавка, хлябът може да остане свеж повече.
Ad
Екстракти на основата на глицерин често се добавят към напитките. Те ви позволяват да направите техния вкус по-малко остър. Използва се и в производството на алкохол. Добавя се и тютюн за регулиране на влагата, премахване на дразнещия вкус.
Медицински приложения
Глицеринът е част от някои лекарства, които се използват за лечение на кожни заболявания. Има антисептични свойства, предпазва от инфекции на рани. Той също така помага за намаляване на вътречерепното и вътреочното налягане, така че се използва при лечението на мозъчен оток.
Поради факта, че глицеринът е добър разтворител, той се използва активно във фармакологичната индустрия. С това вещество може да се постигне много висока концентрация на активната съставка. Той може също да даде желаната консистенция на лекарствата. Често се добавя към мазила и кремове, тъй като предотвратява изпаряването на влагата и сушенето.
Приложение в козметологията
Глицеринът е част от много козметични продукти: сапуни, шампоани, кремове, овлажняващи маски. Когато влезе в контакт с кожата в малки количества, тя запазва влагата в горните слоеве на кожата. Въпреки това, някои твърдят, че честата употреба на продукти с глицеринова база лишава кожата от естествена влага и само изостря сухотата. Също така глицеринът често се използва като добавка в сапуна. Така че способността за измиване се увеличава.
Ефект върху човешкото тяло
Глицеринът се абсорбира добре от организма, тъй като той лесно се превръща в мазнина от храносмилателната система. Поради тази причина тя не се счита за токсична. Дневната консумация на това вещество не е ограничена. Но не забравяйте, че глицеринът е хигроскопичен, така че води до голямо освобождаване на волове в тялото, т.е. има риск от дехидратация. Поради тази причина използването му в хранителните продукти е строго регламентирано. Когато влезе в контакт с кожата, той също има ефект на изсушаване. Все още има разисквания относно необходимостта от използване на вещества в козметиката.
Така в статията се разглежда съставът и свойствата на глицерина, неговото приложение.