Диетилов етер: формула. Диетилов етер: физични и химични свойства
Преди стотици години, известният учен от онова време, Лули, който след смъртта му бил наречен алхимик, успял да открие необходимия диетилов етер. Формулата, свойствата, точката на кипене, методите за получаване на вещества ще бъдат описани подробно в тази статия. 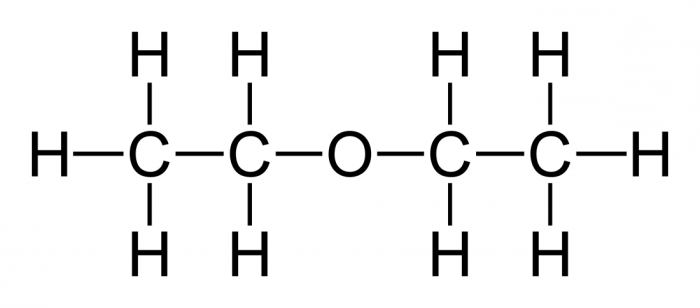
История на
През 13-ти век известният испански учен Раймонд Лул открил диетилов етер. Неговите свойства са описани през 1540 г. от не по-малко известен учен Парацелз. През 1846 г. етерът първо се опитва да се използва като анестезия. Операцията, проведена от американски лекар Д. Уорън с помощта на изпаренията на това вещество, беше успешна. Изобретателите на анестезията се считат за зъболекар У. Мортън и неговия наставник - лекар и химик С. Джаксън.
Ad
Методи за получаване на етер в 16-ти век са описани от Валериус Кордус, известен ботаник и фармацевт от Касел. От началото на XVIII век като успокоително се използва смес от алкохол-етер - това е предложението на Фридрих Хофман. Петербургският фармацевт Томас Ловиц през 1796 г. получи чист диетилов етер, формулата на който между другото има две възможности (повече за това по-късно). Но принципът на действие на гореспоменатото вещество върху човешкото тяло е обявен от английския физик М. Фарадей, след което през 1818 г. е публикувана дори научна статия, посветена на тази тема. 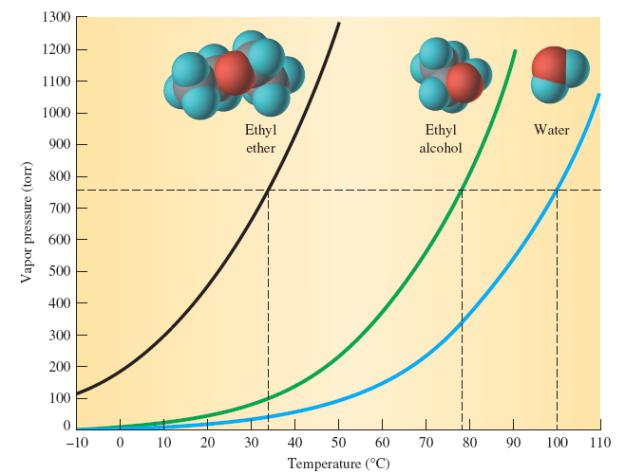
особеност
Какво се нарича прост етер? Това е така органично съединение чиито молекули се състоят от два въглеводородни радикала и кислороден атом. Най-важният прост, диетилов етер, формулата на която има следната форма:
Ad
(С2Н5) 20 или С4Н10О.
Това е безцветна, прозрачна, много подвижна летлива течност със специфичен мирис и парещ вкус.
Под влиянието на светлина, въздух, топлина и влага етерът може да се разложи, образувайки токсични алдехиди, пероксиди и кетони, които дразнят дихателните пътища.
Когато температурата на водата е 20 градуса, се разтваря с 6,5%. Той се смесва добре с мастни и етерични масла, бензол и алкохол, независимо от съотношението.
Самият етер обаче, както и неговите пари, е лесно запалим. В определено съотношение с кислород или въздух изпаренията от диетилов етер, използвани за анестезия, са експлозивни. 
Химични свойства
Всички химични свойства на етерите са характерни за диетилов етер. Така че нека по-подробно да разгледаме този въпрос. Това е доста инертна субстанция. Основната разлика от естерите е липсата на хидролиза, въпреки че има изключения. На студено тя не взаимодейства с фосфорен хлорид, метален натрий и много разредени минерални киселини. Въпреки това, концентриран киселини (сярна и водороден йодид) разлагат тези естери дори при ниски температури и нагряваният метален натрий ги разделя.
Етер с единични електронни двойки взаимодейства с протон силна киселина в резултат на което се получава нестабилно оксониево съединение:
- Ацидолиза. Сярните и йодоводородните киселини, както и FeCl3 в оцетен анхидрид, са способни да разцепват етерите. Химичната реакция е както следва: СН3-СН2-О-СН2-СН3 + HJ → CH3-CH2-OH + J-CH2-CH3.
Ad
- Реакцията на метализация, наречена реакция Shorygin. Нагретият метален натрий разделя диетилов етер: C2H5 - O - C2H5 + 2Na → C2H5ONa + C2H5Na
- Относителната химическа инертност не пречи на образуването на естери във въздуха да образуват пероксиди, което често води до експлозии в края на дестилацията.
Диетилов етер: физични свойства
Особеният мирис, ниска точка на кипене на етерите - доказателство за слаби междумолекулни ефекти, което показва ниска полярност и отсъствие на предпоставки за образуване на водородни връзки. За разлика от алкохолите, естерите имат по-силни електронно-донорни свойства, което се потвърждава от стойността на йонизационните потенциали. Подобряването на тези характеристики е свързано с положителния индуктивен ефект на групата атоми, които се получават от алкани, когато водородният атом е отстранен. 
Температурата на кипене на диетилов етер е 35.6 градуса по Целзий (тя е много по-ниска от тази на изомерните алкохоли), а замразяването е 117 ° С. Етерите почти не се смесват с вода. Обяснението за това е съвсем просто: те не могат да образуват водородни връзки, тъй като техните молекули нямат полярни връзки. Слаборазтворим във вода и диетилов етер, чиято плътност по отношение на водородния оксид е 0,714. Една от характеристиките на въпросната субстанция е тенденцията за електрифициране. Вероятността от статични разряди е особено висока при преливане или изхвърляне на химическия състав, в резултат на което може да възникне запалване. Парите на етера се образуват с въздух, който е 2,5 пъти по-лек, експлозивни смеси. Долната граница на експлозивност е 1,7%, а горната - 49%. Работейки с етер, не трябва да забравяме, че нейните двойки са склонни да се разпространяват на дълги разстояния, без да губят способността си да горят. Така основната предпазна мярка е липсата на открит пламък и други източници на запалване.
Ad
Етерът е ниско активно съединение, по-малко реактивоспособен от алкохолите. Забележително се разтваря по-голямата част от органичната материя, така че се използва като разтворител. Изключение не е диетилов етер. Физическите свойства, както и химичните, позволяват използването му в медицината и в промишлеността.
Получаване на диетилов етер
Етери не се срещат в природата - те се получават синтетично. Под въздействието на киселинни катализатори етилов алкохол при повишена температура се получава диетилов етер (формулата е дадена по-горе). Най-лесният начин за получаване на това вещество е чрез дестилация на смес, състояща се от сярна киселина и алкохол. За да направите това, е необходимо да се затопли до 140-150 градуса по Целзий. Ще ни трябва етилов алкохол и сярна киселина (в равни пропорции), пипети, епруветки и тръби за пара.
Така, след като оборудването и реактивите са подготвени, можете да започнете експеримента. В епруветка (тя трябва да е суха), се налива 2-3 мл смес от алкохол и киселина и бавно се нагрява. Веднага след като започне кипенето, горелката се отстранява и към горещата смес се добавят 5 до 10 капки етилов алкохол, като се използва пипета по протежение на стената на тръбата. Реакцията протича както следва:
Ad
- СНз-СН2-ОН (етилсулфонова киселина) + H2S04CH3-CH2-OSO3H + Н20;
- CH3-CH2-OSO3H + CH3-CH3-O;
- CH3-CH2-0-CH2-CH3 (диетилов етер) + H2S04.
Образуването на диетилов етер се доказва от появяващия се мирис. 
Употреба в медицината
Лекарите използват диетилов етер като общо упойващо средство. Свойствата на това вещество не позволяват използването му в операции, в които се включват електрически инструменти, тъй като е запалим и може да експлодира при комбиниране с въздух. Диетиловият етер е широко разпространен в хирургията, където се използва за инхалационна анестезия. В стоматологията те се лекуват с зъбни коренови канали и кариозни места, като по този начин подготвят устната кухина за пълнене. 
Диетилов етер като гориво
Веществото има високо цетаново число (85-96), така че може да се използва като изходен флуид за бензинови и дизелови двигатели. Поради високата вариабилност и ниските точки на възпламеняване диетиловият етер се използва като компонент на горивната смес за примерни дизелови двигатели. Оказва се, че това вещество е подобно на етанола.
Правилно съхранение
Диетилов етер се препоръчва да се съхранява в тъмни бутилки (внимателно запечатани) на хладно място, тъй като се разлага на светлина, в топлина и под въздействието на влага, което води до токсични вещества.