Ванадий: свойства, атомна маса, формула, приложение
Ванадий е химичен елемент, обозначен със символа "V". Атомната маса на ванадия е 50.9415 a. атомно число - 23. Това е твърд сребристо-сив, ковък и разтопим метал, рядко срещан в природата. Той е част от повече от 60 минерала и може дори да се съдържа в изкопаеми горива.

Неразпознато откритие
Ванадиевият метал за първи път е открит от мексикански минералог от испански произход, Андрес Мануел Дел Рио, през 1801 г. Изследователят отстрани нов елемент от проба от кафява руда, добита в Мексико. Както се оказа, металните соли имат голямо разнообразие от цветове, така че Дело Рио първоначално го нарича "панхромиум" (от гръцкия "παγχρώμιο" - "многоцветен").
Ad
По-късно минералогът преименува елемента еритроний (от гръцкия “ερυθρός” - “червен”), тъй като повечето от солите придобиват червен оттенък при нагряване. Изглежда, че невероятният късмет се усмихна на малко известен учен в Европа. Откриването на нов химически елемент от ванадий обеща, ако не слава, то поне признание от колегите. Въпреки това, поради липсата на тежък авторитет в научния свят, постигането на мексиканския е пренебрегнато.
През 1805 г. френският химик Hippolytus Victor Colle-Dekotils предполага, че новият елемент, изследван от Del Rio, е просто проба от оловен хромат с примеси. В крайна сметка мексиканският изследовател, за да не загуби напълно лицето си пред научното братство, прие одобрението на Colle-Decotyle и отказа да го отвори. Но постижението му не е потънало в забвение. Днес Андрес Мануел Дел Рио е признат за откривател на редкия метал.
Ad
Преоткриване
През 1831 г. швед Нил Габриел Сефстрьом отново открил химичния елемент ванадий в оксида, който той е получил при работа с желязна руда. Като свой учен, ученът избра буквата "V", която все още не е присвоена на нито един елемент. Sefström нарича новия метал заради красивия и богат цвят в чест на скандинавската богиня на красотата Ванадис.
Новината предизвика повишен интерес към научната общност. Веднага си спомни за работата на мексиканския минеролог. През същата 1831 г. Фридрих Вьолер провери и потвърди предишното откритие на Дел Рио. А геологът Джордж Уилям Феестърстон дори предложи да се обади на метала "Риони" в чест на откривателя, но инициативата не беше подкрепена.

неуловим
Изолирането на ванадиев метал в чиста форма се оказа трудно. Преди това учените работеха само с неговите соли. Ето защо истинските свойства на ванадия са неизвестни. През 1831 г. Берцелиус съобщи, че получава метализирана субстанция, но Хенри Енфийлд Роско доказа, че Берцелиус всъщност произвежда ванадиев нитрид (VN). В крайна сметка Роско произвежда метал през 1867 г. чрез намаляване на ванадиевия хлорид (VCl2) под действието на водород. От 1927 г. чистият ванадий се получава чрез намаляване на ванадиевия пентоксид с участието на калций.
Ad
Първата серийна промишлена употреба на елемента датира от 1905 година. Металът е добавен към стоманената сплав за производството на шасита състезателни автомобили, а по-късно - в модела Форд Т. Ванадий характеристики могат да намалят теглото на конструкцията, като същевременно увеличава якостта на опън. Между другото, немският химик Мартин Кенце открива ванадий в кръвните клетки (или целомични клетки) на морските обитатели - екзида - през 1911 година.

Физични свойства
Ванадийът е пластичен сиво-син метал със средна твърдост със стоманен блясък и плътност 6.11 g / cm³. Някои източници описват материала като мек, имайки предвид високата му пластичност. Кристалната структура на елемента е по-сложна от повечето метали и стомани.
Ванадийът има добра устойчивост на корозия, алкални, сярни и солна киселина. Той се окислява на въздух при температура от около 660 ° С (933 К, 1220 ° F), въпреки че пасивирането на оксида става дори при стайна температура. Този материал се топи, когато температурата достигне 1920 ° С и кипи при 3400 ° С.
Химични свойства
Ванадий под въздействието на кислород образува четири вида оксиди:
цвят | плътност | кипене | топене | |
VO (II) | черно | 5.76 g / cm³ | 3100 ° С | 1830 ° С |
V 2 O 3 (III) | черно | 4.87 g / cm3 | 3000 ° С | 1967 ° С |
VO 2 (IV) | Синьо | 4.65 g / cm3 | 2700 ° С | 1542 ° С |
V 2 O 5 (V) | оранжев | 3,357 g / cm3 | 2030 ° С | 670 ° С |
Типове (II) ванадиеви съединения са редуциращи агенти и съединения от тип (V) са окислителни агенти. Съединения (IV) често съществуват като производни на ванадиловия катион.
окис
Най-важното съединение е ванадиевият пентоксид. Това е кафяво-жълто твърдо вещество, въпреки че когато е прясно опакован от воден разтвор, неговият цвят е тъмно оранжев.
Ad

Оксидът се използва като катализатор за получаване на сярна киселина. Това съединение окислява серен диоксид (SO 2 ) до триоксид (SO3). В тази редокси реакция, сярата се окислява от +4 до +6, а ванадий намалява от +5 до +4. Формулата за ванадий е както следва:
V2O5 + SO2 → 2VO2 + SO3
Катализаторът се регенерира чрез окисляване на кислорода:
2VO 2 + O 2 → V 2 O 5
Подобни окислителни процеси се използват при производството на малеинов анхидрид, фталов анхидрид и няколко други насипни органични съединения.
Този оксид се използва и при получаването на ферованадий. Загрява се с желязо и феросилиций с добавка на вар. Когато се използва алуминий, се произвежда желязо-ванадиева сплав заедно с алуминиев оксид като страничен продукт. Благодарение на високия коефициент на термична устойчивост, ванадиевият оксид (V) се използва като детектиращ материал в болометри и микроболометрични решетки в термовизионни устройства.
характеристики на
Редките метали имат следните характеристики:
- Кристална структура: кубична центрирана.
- Проводимост на звука: 4560 m / s (при 20 ° C).
- Валенция на ванадия: V (рядко IV, III, II).
- Термично разширение: 8,4 μm / (m · K) (при 25 ° C).
- Топлинна проводимост: 30,7 W / (m · K).
- Електрическо съпротивление: 197 nm · m (при 20 ° С).
- Магнетизъм: парамагнитно.
- Магнитна чувствителност: + 255 · 10 -6 cm 3 / mol (298 K).
- Модул на еластичност: 128 GPa.
- Модул на срязване: 47 GPa.
- Модул на еластичност: 160 GPa.
- Съотношение на Поасон: 0.37.
- Твърдост по Моос: 6.7.
- Твърдост по викерса: 628-640 MPa.
- Твърдост по Бринел: 600-742 МРа.
- Категория позиция: преходен метал.
- Електронна конфигурация: 3d 3 4s 2 .
- Топлина на топене: 21,5 kJ / mol.
- Топлина на изпаряване: 444 kJ / mol.
- Моларен топлинен капацитет: 24,89 J / (mol · K).
Ванадий в периодичната таблица е в 5-та група (ванадиева подгрупа), 4-ти период, d-блок.
разпространение
Ванадий в мащаба на Вселената е приблизително 0,0001% от общия обем на веществото. Разпространява се толкова често, колкото медта и цинка. Металът се намира в спектралното сияние на Слънцето и други звезди.
Ad
Елементът е 20-тият най-често срещан в земната кора. Кристалният ванадий в кристална форма е доста рядък, но съединенията от този материал се намират в 65 различни минерали. Икономически значими от тях са патронит (VS 4 ), ванадинит (Pb 5 (VO 4 ) 3 Cl) и карнотит (K 2 (UO 2 ) 2 (VO 4 ) 2 · 3 H 2 O).
Ванадиловите йони се разпространяват обилно в морската вода и имат средна концентрация от 30 nMa. Някои източници на минерална вода също съдържат тези йони във високи концентрации. Например източници в близост до планината Фуджи съдържат до 54 µg / l.
екстракция
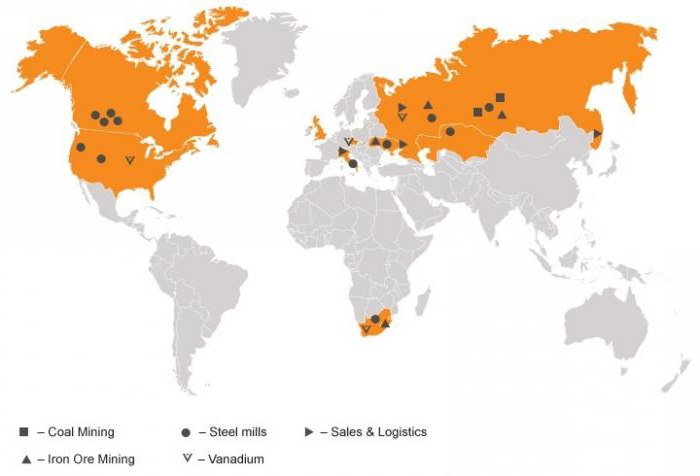
По-голямата част от този рядък метал се получава от ванадиев магнетит, намиращ се в ултрабазичните магматични габбро скали. Суровините се добиват главно в Южна Африка, Северозападен Китай и Източна Русия. През 2013 г. тези страни произведоха повече от 97% от целия ванадий (79 000 тона тегло).
Металът също присъства в бокситите и находищата на суров нефт, въглища, петролни шисти и катранени пясъци. В суров петрол са докладвани концентрации до 1200 ррт. Поради окислителните свойства на ванадий (някои от неговите оксиди) след изгаряне на такива петролни продукти, остатъците от елемента могат да предизвикат корозия в двигателите и котлите.
Около 110 000 тона на веществото се изпуска в атмосферата годишно чрез изгаряне на изкопаеми горива. Днес се разработват технологии за извличане на ценни вещества от въглеводороди.
производство
Ванадийът се използва главно като добавка към стоманените сплави, наречени феросплави. Ферованадий се получава директно чрез редукция на смес от ванадиев оксид с валентност (V), железни оксиди и чисто желязо в електрическа пещ.
Металът се произвежда чрез многостепенен процес, който започва с изгаряне на натрошени руди ванадиев магнетит с добавяне на натриев хлорид (NaCl) или натриев карбонат (Na2CO3) при температура около 850 ° С за получаване на натриев метаванадат (NaVO 3 ). Водният екстракт от това вещество се подкислява до образуване на поливанадатна сол, която се редуцира от калциевия метал. Като алтернатива на дребномащабното производство, ванадиевият пентоксид се редуцира от водород или магнезий.
Използват се и много други методи, при които ванадийът се произвежда като страничен продукт от други процеси. Неговото почистване е възможно чрез йодидния метод, разработен от Антон Едуард ван Аркел и Ян Хендрик де Бор през 1925 година. Това предполага образуването на ванадиев (III) йодид и последващото му разлагане в чист метал:
2 V + 3I 2 VI 2 VI 3
Доста екзотичен начин за получаване на този елемент е изобретен от японците. Те се размножават на асцидиански подводни плантации (тип акорд), които абсорбират ванадий от морска вода. След това се събират и изгарят. Ценен метал се извлича от образуваната пепел. Между другото, неговата концентрация в този случай е много по-висока, отколкото в най-богатите депозити.

сплави
Какво представляват ванадиевите сплави? Приблизително 85% от произвеждания рядък метал се използва за производство на ферованадий или като добавка към стоманата. В началото на 20-ти век се установи, че дори малко количество ванадий значително увеличава здравината на стоманата. Този елемент образува стабилни нитриди и карбиди, което води до подобряване на производителността на стомани и сплави.
Оттогава ванадийът се използва в оси, рамки, колянови валове, зъбни колела и други важни компоненти на колесните превозни средства. Има две групи сплави:
- Високо съдържание на въглерод от 0.15% до 0.25% ванадий.
- Бързо рязане стомани за инструменти (HSS) съдържание от 1% до 5% от този елемент.
За HSS стомани може да се постигне твърдост по-висока от HRC 60. Те се използват в хирургически инструменти. При праховата металургия сплавите могат да съдържат до 18% ванадий. Високото съдържание на карбиди на тези сплави значително увеличава износоустойчивостта. Те правят инструменти и ножове.
Благодарение на своите свойства, ванадий стабилизира бета формата на титан, повишава неговата якост и стабилност на температурата. Смесен с алуминий в титанови сплави, той се използва в реактивни двигатели, високоскоростни самолети и зъбни импланти. Най-често срещаната сплав за безшевни тръби е титан 3 / 2.5, съдържащ 2,5% ванадий. Тези материали са широко разпространени в авиационната, отбранителната и велосипедната промишленост. Друга обща сплав, произведена главно в листове, е титан 6AL-4V, където 6% алуминий и 4% ванадий.
Няколко ванадиеви сплави проявяват свръхпроводящи свойства. Първият фазов свръхпроводник А15 е V 3 Si ванадиево съединение, което е получено през 1952 година. Ванадиево-галиевата лента се използва в свръхпроводящите магнити. Структурата на свръхпроводящата фаза А15 V 3 Ga е подобна на структурата на по-често срещаните свръхпроводници: станнид триниобий (Nb 3 Sn) и ниобий-титан (Nb 3 Ti).
Напоследък учените са открили, че през Средновековието малко количество ванадий (от 40 до 270 части на милион) е добавено към някои проби от дамаска и дамаска. Това подобри свойствата на остриетата. Не е ясно обаче къде и как се добива редкия метал. Може би той е бил част от някои руди.
приложение
В допълнение към металургията, ванадийът се използва и за други задачи. Напречното сечение на улавянето на топлинни неутрони и краткият полуживот на изотопите, получени от улавянето на неутрони, правят този метал подходящ материал за използване в термоядрен реактор.
Най-често срещаният ванадиев оксид, пентоксид V 2 O 5, се използва като катализатор в производството на сярна киселина и като окислител в производството на малеинов анхидрид. Ванадиевият оксид се използва при производството на керамични продукти.
Металът е важен компонент на смесените метални оксидни катализатори, използвани в окисляването на пропан и пропилей до акролеин, акрилова киселина или амоксидиране на пропилей до акрилонитрил. Друг ванадиев оксид - диоксид VO 2 - се използва в производството на покрития от стъкло, които блокират инфрачервеното излъчване при определена температура.
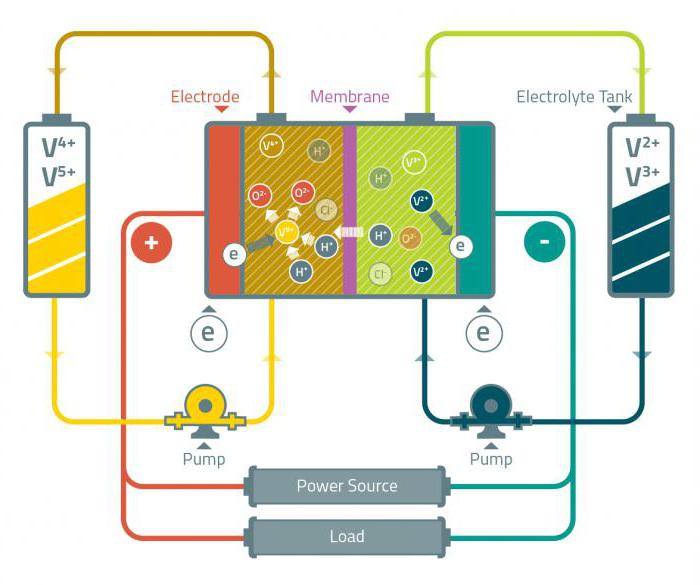
Ванадиевата редокс батерия е галванична клетка, състояща се от водни йони на ванадий в различни окислителни състояния. Батериите от този тип бяха предложени за първи път през 30-те години на миналия век, а търговската им употреба започна през 80-те години. Ванадат може да се използва за защита на стоманата от корозия.
Ванадийът е важен за човешкото здраве. Той помага за регулирането на въглеродния и липидния метаболизъм, участва в производството на енергия. На ден се препоръчва да се консумират 6-63 mcg (данни на СЗО) на веществото, идващо от храната. Достатъчно е при зърнени култури, бобови растения, зеленчуци, билки, плодове.