Сложни съединения и тяхното значение
Сложните съединения (CS) играят важна роля в активността на живите организми. Те също се използват широко в промишлеността. Днес разглеждаме тяхното видово разнообразие, приложение и история на изследването.
Въведение в комплексните съединения
Сложни съединения са вещества, образувани от комбинацията от лиганд и комплексообразуващ агент. Възпроизвеждане на ролята на взаимодействащи частици могат атоми и йони. А. Вернер през 1893 г. въвежда в света теорията на сложните съединения, наричана още координационна теория.
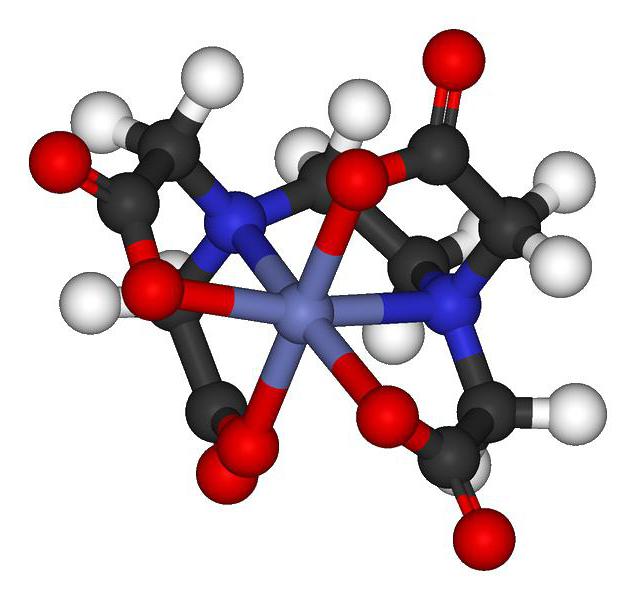
Наличието на външна сфера и пълна дисоциация в разтвор на вода в нискодисоцииращи катиони и аниони са характерни за CS. Има обаче някои видове, които нямат външна сфера, която не им позволява да се разтварят във вода. Има огромно количество ченге.
Видове съединения
Сложните съединения се разделят на три основни типа:
- Първият тип, който се различава по комплексен заряд, включва катионни комплекси, в които, обграждайки положителен йон, неутралните молекули са координирани. Вторият тип се нарича анионен комплекс, в който положително окислен атом действа като комплексообразуващ агент, а аниони от прост или сложен тип са лиганди. Третият тип се нарича неутрален комплекс, формиран от молекулярната координация около атом с неутрален заряд.
- В зависимост от естеството на лигандата, те се разделят на амониати (амоняк - лиганд), аквакомплекси (лиганд - вода), хидроксокомплекси (лиганди - хидроксидни йони), кисели комплекси (лиганди - киселинни остатъци), карбонили (лиганди - въглеродни молекули от втората валентност).
- В съответствие с местоположението на лигандите са монодентатни, бидентатни и полидентатни QS.
Историческа информация
През 1893 г. е направен първият опит да се опише изчерпателно структурата на КС, използвайки координационната теория на Алфред Вернер. Работата е извършена преди появата на теорията за електронната валентност и обичайното химични реакции на природата.

В неговата теория Вернер твърди, че съединения с неорганична природа имат ядра, съставени от образуващи сложни атоми. Атомите около комплексите се наричат координация. Те са подредени в съответствие с формата на прост полиедър. А. Вернер предположи наличието на координационен тип връзка в обща електронна двойка, която атоми или молекули биха дали на друга двойка. Отсъствието на такива съединения обаче предизвика недоверие сред химическата общност. В резултат на това през следващите две десетилетия ученият се опита да създаде необходимите вещества, които биха потвърдили неговата теория.
Вернер през 1911 г. синтезира над четиридесет молекули от оптичния тип, които не съдържат въглеродни атоми, което в крайна сметка променя мнението на учени по химията за неговата теория.
Алфред Вернер е удостоен с Нобелова награда през 1913 г. за постижения в областта на химията.
номенклатура
Сложните съединения имат система за създаване на вашите собствени имена, състояща се от пет точки:
- Първият е изразен анион, след това катион.
- Комплексната част започва с лиганд - анион, разположен във вътрешната сфера, и до края се добавя с "о".
- Монодентатни лиганди се обозначават с помощта на гръцки: моно, ди, три, тетра, пента, хекс (1, 2, 3, 4, 5, 6). При работа с полидентатни лиганди се използват трис, бис, тетракис и други.
- Определяйки вътрешната сфера с нейните компоненти, отидете на външната.
- Комплексният агент на частици с неутрален комплекс е посочен в номинативния случай.
Структурна информация
Сложните съединения имат вътрешна сфера, състояща се от редица йони или молекули с неутрална природа, здраво свързани към комплексообразуващия агент. Те се наричат лиганди. Вътрешната сфера може да носи три вида такса: "+", "-" или "0".
Външната координационна сфера е йони, които не са разположени в пространството на вътрешната сфера.
Връзката между лиганда и централния йон може да бъде причинена или от електростатично привличане, или от донорно-акцепторния механизъм.
Изомеризмът в координационните съединения е основен статистически аспект. Говорейки за изомеризма, те означават различни взаимни позиции в пространството на атоми или съставки на съединение, което ще доведе до промяна във физичните и химичните свойства на съответното съединение - изомер. CS изомерия е структурна, оптична и пространствена.
стреохимия
Сложни съединения, заедно с органична материя Високомолекулните съединения от синтетичен или естествен произход са основните обекти на стереохимичните изследвания. A. Werner се смята за един от онези учени, които дадоха развитие на цяла област от изследвания и възродиха някои области на химическата активност. Стереохимията и до днес остава отправна точка за координационни химически изследвания.
Някои свойства и методи за получаване
Получаването на комплексни съединения има доста широк спектър на избор, но такива се използват по-често:
- Разтваряне на хидроксиди във воден амоняк, които не се разтварят във вода.
- Взаимодействието на амоняк с метални соли с комплексообразуващи свойства; по-често те са метали във вторичната подгрупа.
- Взаимодействие на цианиди или роданиди с метали или соли.
- Стаята е неразтворима в H 2 O метали от амфотерния тип, а именно техните оксиди или хидроксиди в алкален разтвор.
- Сложните киселини могат да бъдат получени, например, чрез взаимодействие на злато и вода, или хидроксид на Au с НС1.
Много от качествените характеристики на съединенията зависят от техните електронни свойства, така че цветът на CS може да се определи от комплексообразуващия агент и лигандите. Разделянето на енергията на d-орбиталата позволява на електроните да се движат от неговите d xz , d xy , d zy поднива до поднива с по-висок енергиен индекс d z 2 или d z 2 - y 2 . Това явление е придружено от абсорбцията на светлинните кванти. Величината на разликата между разделените нива предизвиква абсорбцията на светлинни кванти с дължина на вълната с различна дължина, която дава определен цвят.
Сложните съединения също имат две важни магнитни свойства, според които те са класифицирани като парамагнитни и диамагнитни. Парамагнитните комплекси имат свои собствени µ-моменти и по тази причина, навлизайки във външни електромагнитни полета, в процеса на взаимодействие, те се привличат в тях. Диамагнитният комплекс няма магнитен момент и затова магнитното поле бърза да го избута. Свойствата на парамагнитната природа се определят от наличието на електрони, които нямат двойка в структурата си.
Използване на

Съединенията от сложен тип играят една от най-важните роли във всеки организъм, например кислород, свързан с хемоглобин в кръвта, се доставя от О2 през тялото в тъкани и клетки; Хлорофилът вътре в растенията също се счита за комплекс.
Използването на комплексни съединения се използва широко в промишлеността. С помощта на химични методи, които водят до образуването на KS, металите се извличат от рудата. Примерите включват чисто желязо, никел и кобалт, които се получават чрез термично разлагане на метални карбонили. Тези сложни вещества, разлагащи се, отделят необходимите метали.

Аналитичната химия може да използва КС като индикатори. Органичният и неорганичният синтез може да се ускори поради тях, тъй като свойствата на катализатора са присъщи за тях поради тяхната висока активност. Електроформирането също не може да стане без комплексни съединения, което се дължи на невъзможността да се получат такива надеждни покрития от проста сол, за разлика от цианидните съединения.