Химични свойства на карбоксилните киселини и методи за получаване
Химични съединения, които се състоят по-специално от карбоксилната група СООН, получават името карбоксилни киселини от учените. Има много имена на тези съединения. Те се класифицират по различни параметри, например, броя на функционалните групи, наличието на ароматен пръстен и т.н.
Структурата на карбоксилните киселини
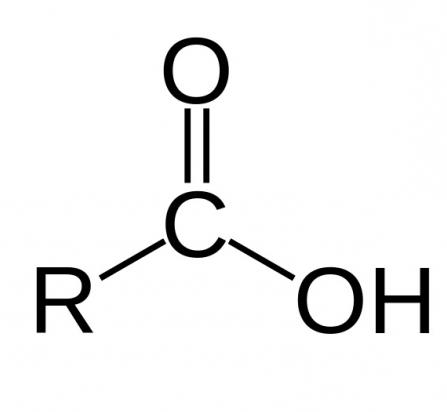
Както вече бе споменато, за да бъде киселината карбоксилна, тя трябва да има карбоксилна група, която от своя страна има две функционални части: хидроксил и карбонил. Тяхното взаимодействие се осигурява от функционалната му комбинация от един въглероден атом с два кислорода. Химичните свойства на карбоксилните киселини зависят от структурата на тази група.
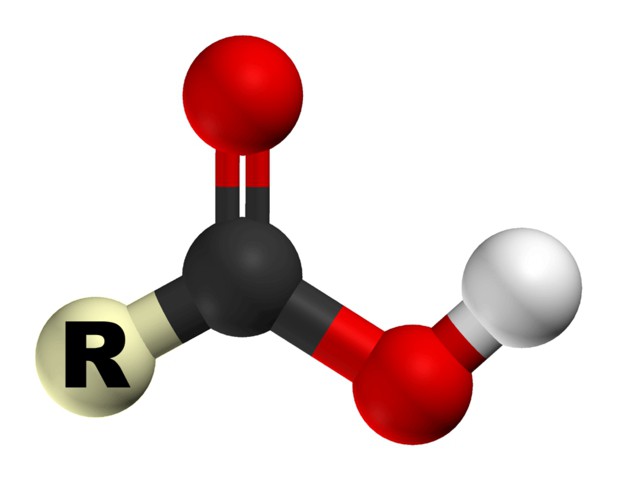
Поради карбоксилната група, те органични съединения могат да бъдат наречени киселини. Техните свойства се дължат на повишената способност на водородния йон Н + да бъде привлечен към кислорода, допълнително поляризиращ ОН връзката. Също така благодарение на това свойство органичните киселини могат да дисоциират във водни разтвори. Способността за разтваряне намалява обратно спрямо увеличаването на молекулната маса на киселината.
Сортове карбоксилни киселини
Химиците отделят няколко групи органични киселини.
Класификация на карбоксилната киселина | |
По броя на функционалните групи | монокарбоксилни |
дикарбоксилна | |
поликарбоксилан | |
По природа радикални | алифатен |
ароматен | |
цикличен | |
Според степента на насищане на радикала | ненаситен |
наситен | |
Чрез присъствието на функционални групи в радикала, т.е. чрез заместване на един водороден атом | Халоген (Cl 2 , F 2 , Br 2 , I 2 ) |
Oxogroup (COH) | |
Хидрокси (ОН) | |
Аминогрупата (NH 2) | |
Едноосновните карбоксилни киселини се състоят от въглероден скелет и само една функционална карбоксилна група. Всеки студент познава химичните свойства на карбоксилните киселини. Програма 10 по химия включва директно изучаване на свойствата на едноосновните киселини. Двуосновни и многоосновни киселини имат съответно две или повече карбоксилни групи.
Също така, чрез присъствието или отсъствието на двойни и тройни връзки в молекулата, съществуват ненаситени и наситени карбоксилни киселини. Химичните свойства и техните различия ще бъдат разгледани по-долу.
Ако органичната киселина има заместен атом в радикала, тогава нейното име включва името на заместващата група. Така че, ако водороден атом е заменен с халоген, тогава името на киселината ще съдържа името на халогена. Същите промени ще претърпят име, ако има заместване с алдехид, хидроксил или амино групи.
Изомеризъм на органична карбоксилна киселина
Почти всички органична материя имат способността за изомеризация. Карбоксилните киселини не са изключение. Различават се следните видове изомеризъм:
- Въглероден скелет.
- Междукласова изомерия.
- Пространствена изомерия;
Способността за изомеризиране пряко влияе на химичните свойства на карбоксилните киселини.
Скелетен изомеризъм е възможен за киселини, чиито въглеводороди съдържат поне четири въглеродни атома. Interclass, от своя страна, е възможно за киселини с два въглеродни атома в радикала. И само карбоксилни киселини с единични връзки в скелета са способни на пространство.
Списък и основни карбоксилни киселини
Имена и формули на известни карбоксилни киселини | ||
Систематичното име на киселината | Тривиално име | Формула на карбоксилната киселина |
Метанова киселина | мравчен | НСООН |
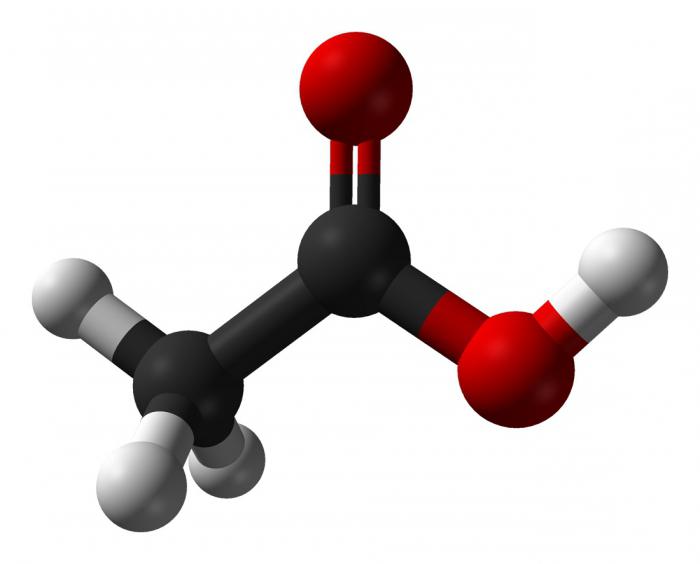
Етанова киселина | оцетен | СН2СООН |
Пропанова киселина | пропионова | CH3CH2COOH |
Бутанова киселина | масло | CH3CH2CH2COOH |
Пентанова киселина | валериан | CH3CH2CH2CH2COOH |
Пентенова киселина | акрил | СН2 = СН-СООН |
Бензолкарбонова киселина | бензоена | C6H5COOH |
хексадеканоловата | палмитинов | C15H31COOH |
Oksodekanovaya | стеаринов | C17H35COOH |
етандионова | оксалов | НООС-СООН |
пропандионовата | малонова | НОС-СН2-СООН |
бугаандиоВа | кехлибар | НОС-СН2-СН2-СООН |
Бензол дикарбоксил | фталов | HOOC-C6H5-COOH |
2-хидрокси-пропанова киселина | мандра | CH3CHOHCOOH |
Хидроксибутандионова киселина | ябълка | НОС-СН2СНОН-СООН |
2,3-дихидроксибутандионова киселина | вино | НООС-OHCH-OHCH-СООН |
3-карбокси-3-gidroksipentandiovaya | лимонена | НОСО-СН2-СНОН-СООН-СН2СООН |
2-оксопропанова киселина | пируват | CH3COCOOH |
2-хидроксибензоена киселина | салицилов | C6H5OHCOOH |
Карбоксилни киселини: химични свойства
За по-подробно разбиране на същността на карбоксилните киселини разгледайте техните свойства. В учебния план се разглеждат монобазните карбоксилни киселини в голям обем, чиито химични свойства се проявяват в реакции между водородни халиди, вода и други вещества. Всички тези видове киселини:
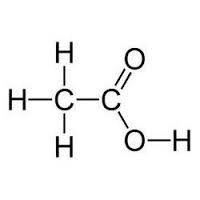
- Дисоциира се в разтвор на водородни йони и радикал с карбоксил. С това мравчена киселина се отнася до електролити със средна якост и слаба оцетна киселина, т.е. силата на дисоциацията намалява по хомоложните серии.
- Оцветете лакмусния тест в червено.
- Проведете ток на електроенергия.
- Реагира с халогени: 2RCOOH + Cl2 = 2RCOOCl + 2HCL.
- Те влизат в реакция на естерификация с алкохоли: R-COOH + R'OH = RCOOR '+ Н20.
- Взаимодейства с някои метали: RCOOH + Mg = RCOOMg + H2.
- Реагирайте с основни оксиди тип и хидроксиди, образуващи соли: RCOOH + NaOH = RCOONa + H2O.
- Реагира с соли: RCOOH + Na2CO3 = RCOONa + H2O + CO2.
Такива свойства на едноосновни киселини се обясняват с промяна в карбоксилната група, от хидроксила, от който електроните се преместват към най-близкия въглероден атом, частично угасвайки своя положителен заряд. Освен това, карбоксилните киселини, чиито химични свойства са описани по-горе, имат двупосочно взаимодействие между атомите.
Химични свойства на други едноосновни киселини
От класификацията е известно, че съществуват и едноосновни ненаситени карбоксилни киселини, чиито химични свойства се различават от тези на границата.
Така, двойносвързаните киселини в въглеводородния радикал са едноосновни ненаситени карбоксилни киселини. Химичните свойства на такива киселини се изразяват в реакциите:
- С водороден халогенид, но много по-бавен от ограничаващите и противно на правилото на Марковников, тъй като карбоксилната група намалява електронната плътност на двойната връзка: R = CH-COOH + HCl = RCl-CH2-COOH.
- С халогени: Br2 + R = CH-COOH = RBr-CHBr-COOH.
- С водород, в резултат на което двойната връзка прекъсва: Н2 + R = СН-СООН = СООН-R-CH.
- Внимателно окисление, в резултат на което се образуват хидрокси киселини: R = CH-COOH + Н20 [0] R (OH) -CH (OH) COOH.
- Радикалното окисление, което настъпва с разкъсването на киселинна молекула (например, пропенова киселина): СН3-СН = С-СООН + Н20 [О] СНЗСООН + HOOC-COOH.
- Полимеризация: n СООН- (СН = СН) -R = n (-СООН-СН-СН-R-)
Химични свойства на бикарбоксилни киселини
Дикарбоксилни органични киселини са двуосновни карбоксилни киселини. Химичните свойства на такива киселини се различават от свойствата на монокарбоксилните. Това се дължи на факта, че силата на двуосновните киселини е по-голяма от силата на едноосновните поради влиянието на втората група карбоксил и хидроксил. Освен това този ефект намалява с разстоянието от веригата на въглеродните атоми.
Двуосновните киселини притежават следните свойства:
- Киселинно декарбоксилиране (например, етанедин): HOOC-COOH (t) = HOOC + CO2. Важно е да се знае, че оксалната и малоновата киселини се декарбоксилират много по-лесно от други.
- Образуване на кисели и средни соли: HOOC-RR-COOK или HOOK-RR-COOK.
- Образуването на пълни и непълни етери.
- Малоновата киселина може да влезе в реакциите на заместване: водородът от СН2 групата на въглеводородния радикал лесно се замества с метални атоми.
Соли, образувани от карбоксилни киселини
Солите са органични съединения, получени от заместването на водороден атом и хидроксилна група на карбоксилна киселина на карбоксилна киселина с метал. Тоест, органични киселини в реакции с основи или неорганични соли са способни да образуват соли на карбоксилни киселини. Химичните свойства, чрез които се получават органични съединения като соли, се използват в битовата промишленост за производството на сапун.
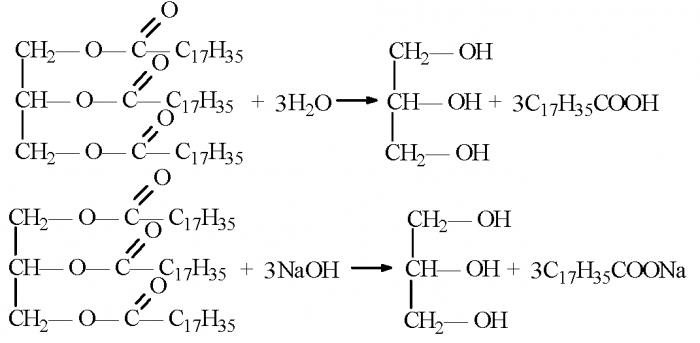
Стеаринова (октадеканова) и палмитинова (хексадеканова) киселини са най-подходящи за синтеза на твърди и течни сапуни. Олеинова (цис-9-октадецен) или миристинова (тетрадекан) киселина).
Основата на сапуна е реакцията на синтеза на естерите на горните киселини с калиева или натриева сол.
Методи за получаване на карбоксилни киселини
Съществуват много методи и методи за получаване на киселини с COOH групата, но най-често се използват следните:
- Екстракция от естествени вещества (мазнини и други неща).
- Окисляване на моноалкохоли или съединения с COH-група (алдехиди): ROH (RCOH) [0] R-COOH.
- Хидролиза на трихалоалкани в алкали с междинно производство на моно-алкохол: RCI3 + NaOH = (ROH + 3NaCl) = RCOOH + Н20.
- Сапонизация или хидролиза на естери на киселина и алкохол (естери): R-COOR '+ NaOH = (R-COONa + R'OH) = R-COOH + NaCl.
- Окисляване на алкани с перманганат (твърдо окисление): R = СН2 [О], (KMnO4) RCOOH.
Стойността на карбоксилните киселини за хората и промишлеността

Химичните свойства на карбоксилните киселини са от голямо значение за човешкия живот. Те са изключително необходими за организма, както в големи количества, съдържащи се във всяка клетка. Метаболизмът на мазнини, протеини и въглехидрати винаги преминава през етапа, на който се получава една или друга карбоксилна киселина.
Освен това, при създаването на лекарства се използват карбоксилни киселини. Не може да съществува фармацевтична индустрия без практическото използване на свойствата на органичните киселини.

Важна роля играят съединенията с карбоксилна група в козметичната индустрия. Синтезът на мазнини за последващото производство на сапун, детергенти и домакински химикали се основава на реакцията на естерификация с карбоксилната киселина.
Химичните свойства на карбоксилните киселини се отразяват в човешкия живот. Те са от голямо значение за човешкото тяло, тъй като се съдържат в големи количества във всяка клетка. Метаболизмът на мазнини, протеини и въглехидрати винаги преминава през етапа, на който се получава една или друга карбоксилна киселина.