Автоматизация на сърцето - описание, механизъм и характеристики
Сърцето на живия организъм е интересен продукт на еволюцията, орган, чиято работа се основава на взаимодействието на хуморалната и нервната системи, като същевременно запазва собствената си автономия. И нека днес учените знаят практически всичко, което се отнася до неговата структура и дейност, а е трудно да се управлява. Трябва обаче да се научи, което ще бъде отправна точка за увеличаване на продължителността на живота. Автоматизацията на сърцето, нейният метаболизъм и връзката на свиването с мембранния потенциал са много важни за медицината. Тяхното проучване и правилното разбиране ви позволява да изберете по-компетентно лечение за вашите пациенти.
Автоматизация на пейсмейкъра
Автоматизацията на сърцето е способността й самостоятелно да генерира потенциал за действие в диастолната фаза. Това е основата на автономността на това тяло, поради което не зависи от активността на мозъка. Освен това еволюционното висококачествено сърце се развива много по-рано от мозъка и центъра на сърдечносъдовия тон.
Субстратът и причината за сърдечния автоматизъм се съдържат в най-фундаменталните механизми, свързани с работата на йонните канали. Те формират разликата на токовете на противоположните страни на мембраната, която се променя с времето, генерирайки импулсен електрически ток. Неговата проводимост в специални клетки към потенциално зависими тъкани е в основата на сърдечната дейност.
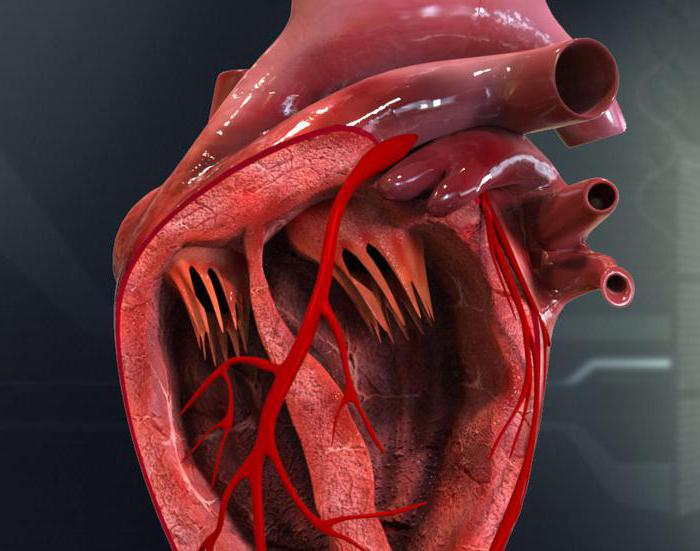
Структурата на сърдечната проводимост
В допълнение към мускулната тъкан, сърцето има своя собствена система за генериране на ритъм, поради което органът не зависи от контрола на мозъка и гръбначния мозък. Тази система е автономна и зависи само от функционирането на йонните канали на атипичните кардиомиоцити. Те са разделени на 3 вида в зависимост от особеностите на структурата и функциите. Първият тип - пейсмейкър атипични клетки P-кардиомиоцити. Вторият тип клетки са проводящи преходни клетки, третият тип са клетките на Purkinye и His, разположени субендокардиално.
Р-кардиомиоцитите са овални или кръгли клетки, пейсмейкъри, поради което се реализира сърдечен автоматизъм. Те са в голям брой в самия център на синусовия възел. Тяхното малко количество е в атриовентрикуларния възел на проводящата система.
Междинните кардиомиоцити са продълговати, продълговати, различават се от малък брой миофибрили, но са по-малки от контрактилните кардиомиоцити. Те са разположени по периферията на синусовия и атриовентрикуларния възел. Тяхната задача е да проведат импулс към снопа от него и към влакната, разположени между ендокарда и повърхностните слоеве на миокарда.
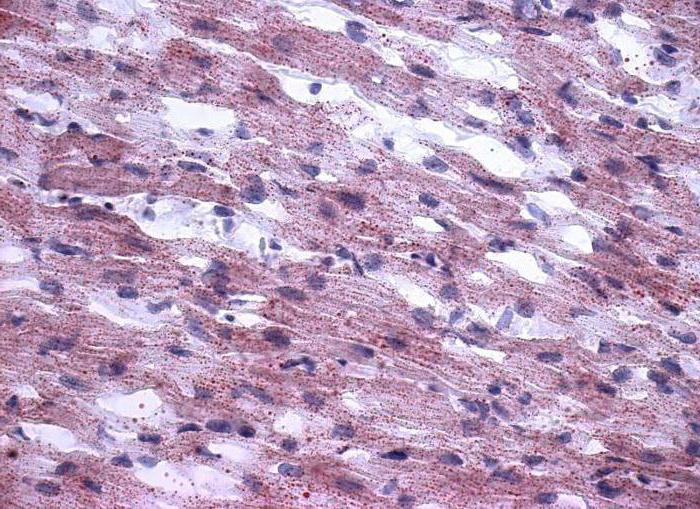
Клетките на проводящата система, локализирани в снопа от влакна от His и Purkinje, имат специална структура и се характеризират с ниска ефективност на гликолизата поради преобладаването на неговия анаеробен вариант. Те са сплескани и по-дълги от междинните кардиомиоцити и техният размер е малко по-голям от съкратителните клетки. В цитоплазмата има малко количество мускулни влакна. Тяхната задача е да свържат възлите на автоматичния сърдечен и контрактилен миокард, т.е. да проведат пулс от пейсмейкъра към сърдечен мускул.
Нормален ритъм и разпространение на пулса в сърцето
Свиването на сърцето е резултат от генерирането на сърдечен импулс, потенциала за действие на клетките на пейсмейкъра на синусовия възел. Тук е максималният брой пейсмейкъри, генериращи ритъм с честота от 60-100 пъти в минута. Предава се чрез проводящи клетки към атриовентрикуларния възел, чиято основна задача е да забави ритъма. Възбуждането достига до AV-възела чрез снопове проводящи кардиомиоцити, които също притежават автоматизъм. Въпреки това, те са в състояние да генерират ритъм с честота от 30-40 пъти в минута.
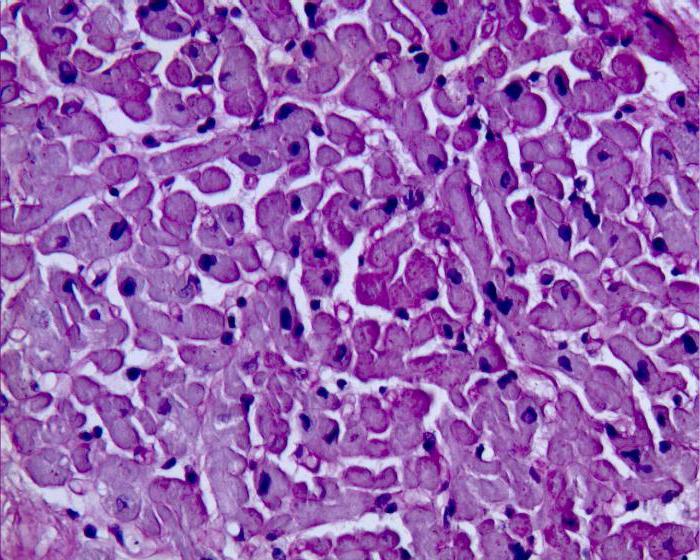
След AV възела, ритъмът обикновено се разпространява чрез провеждане на атипични кардиомиоцити към Неговия пакет, чийто автоматизъм е изключително нисък - до 20 импулса в минута. Тогава възбуждането достига до крайния елемент на проводящата система - влакна Purkinje. Способността им да генерират ритъм е още по-ниска - до 10 на минута. Освен това основният пейсмейкър, т.е. синусовият възел, генерира импулси много по-често. И всяко следващо разпространение на потенциала за действие потиска ритъма на по-ниските дивизии.
Намаляването на способността на сърдечната проводима система да генерира високочестотен ритъм от синусовия възел до влакна на Purkinje се нарича автоматичен градиент. Този процес се обяснява с намаляване на скоростта на деполяризация на мембраната: в синусовия възел спонтанната бавна диастолна деполяризация е колкото е възможно по-висока, а като се движи в дисталните части е най-малко. Градиентът на автоматизацията е насочен надолу, което е признак на нормално функциониращата сърдечна проводимост.
Промяна в мембранния потенциал на пейсмейкърите
В диастолата на сърцето, в клетките на пейсмейкъра се наблюдава следната йонна структура: количеството калиеви катиони над натриевите йони преобладава в клетката. Извън клетката, концентрацията на катиони е точно обратното. В същото време, потенциалът за почивка на клетката на пейсмейкъра е -60 mV. Калиевите токове в покой имат ниска ефективност, тъй като на мембраната има много малко йонни канали за калий. Това ги отличава от контрактилните миоцити, където потенциалът за почивка е приблизително -90 mV.

Работа на HCN канали и стартиране на SMDD
Спонтанната бавна диастолна деполяризация (SMDD), характерна за всеки атипичен кардиомиоцит, води до промяна в мембранния потенциал и е процес, отговорен за автоматичната функция на сърцето. SMDD започва с работата на HCN-йонните канали. Това са така наречените катионни канали, активирани от хиперполяризация, задвижвани от циклични нуклеотиди. САМР ги активира по време на хиперполяризацията, т.е. при потенциал за почивка, равен на -60 mV. Това означава, че след всяка реполяризация, веднага щом клетката “се презареди” и нейният мембранен потенциал достигне стойност от –60 mV, се задейства отварянето на HCN каналите. В резултат на това катионите влизат в клетката, главно чрез натриеви канали.
В резултат на малък приток на натрий, мембранният потенциал ще се увеличи до около -57 mV. Това е сигнал за активиране калциев канал Т-тип, предназначен за подаване на катиони Са2 +. Те се активират чрез слаба деполяризация и се наричат под-прагове. Това означава, че увеличаването на мембранния потенциал до -55-57 mV ще доведе до отваряне на транспортни канали за по-нататъшна деполяризация. Тези йонни канали се активират от натриеви йони, намиращи се вътре в клетката, инжектират малко калций в цитоплазмата и увеличават потенциала до -50 mV, след което бързо се затварят.
Работата на натриево-калциевия обменник
Наличието на калций в цитоплазмата е сигнал за отваряне на механизма на натриево-калциевия обменник. Смисълът на неговата работа е следният: чрез активен транспорт се отделят калциеви йони с заряд 2+ в извънклетъчното пространство, а Na + влизат в клетката. Един натриев катион в цитоплазмата получава 3 натриеви + йона, което води до увеличаване на заряда на мембраната и растеж на мембранния потенциал до -40 mV.
Генериране на потенциал за действие
При достигане на потенциал от -40 mV се отваря потенциал-зависим калциев канал от тип L. Те са способни да работят дълго време и да доведат до бързо увеличаване на концентрацията на калциеви йони в клетката. Това е най-важният процес в работата на йонните канали, тъй като поради него има лавиноподобен растеж на мембранния заряд, който формира потенциал за действие (AP). Този йонен процес повишава мембранния потенциал до пик на ниво от +30 mV, след което клетката е напълно деполяризирана и генерира необходимия импулс за работа на сърцето.
Мембранната деполяризация е активатор не само на калциевия ток, но и на калия. Въпреки това, йонните канали, които освобождават калиеви йони навън, работят със закъснение. Следователно, тяхната селекция се случва на върха на формирането на PD. В същото време, калциевият ток през L-каналите е напълно спрян и мембранният потенциал отново се намалява чрез премахване на калиевите йони срещу градиента на концентрация чрез активен транспорт. Зарядът на мембраната отново спада до -60 mV, като започва SMDD процеса след балансиране на началните концентрации на калций и натрий.
Естеството на автоматизма и неговото регулиране
Атипичният кардиомиоцит е в състояние да изпълнява функцията си поради калциевия ток през бавните йонни канали, в резултат на което се формира потенциал за действие. Този процес е в основата на възбудимостта на миокарда. SMDD, от друга страна, има различна цел. Неговата задача е да започне автоматично започване на деполяризацията с определена честота. Това е наличието на SMDD фаза, която е естеството на сърдечния автоматизъм, способността спонтанно да генерира възбуждане в клетките на пейсмейкъра.
Степента на развитие на SMDD се регулира директно от соматичната автономна нервна система. В покой, той е минимален поради инхибиращия ефект вагусен нерв. Това обаче не означава, че автоматичността на сърцето спира. Просто SMDD етап ще продължи по-дълго, което ще осигури по-дълга диастола. Интензивността на метаболитните процеси в миокарда и сърдечната проводимост намалява, а органът е под по-малък стрес.
Ефектът от ускоряване на спонтанната бавна диастолна деполяризация се постига чрез влиянието на симпатиковата нервна система и нейния медиатор адреналин. След това скоростта на DMDD се увеличава, което осигурява ранно активиране на натриево-калциевия обменник и отварянето на бавно калциеви канали. Резултатът е ускоряване на честотата на ритъма, повишаване на сърдечната честота, увеличаване на потреблението на енергия.
Фармакологични ефекти върху автоматиката на пейсмейкъра
Инхибира механизма на автоматичната сърдечна дейност и фармакологичния метод. Използвайки някои лекарствени, наркотични и отровни вещества, е възможно да се ускори генерирането на ритъм, да се забави или напълно да се блокира. Разбира се, по етични причини, отровни и наркотични вещества в тази публикация няма да бъдат разглеждани.
Следните групи лекарства могат да забавят скоростта на генериране на ритъм: адренергични блокери и блокери на калциевите канали. Това са безопасни лекарства, особено селективни бета-1-блокери. Механизмът им на действие се свежда до инактивиране на рецептора, към който обикновено е прикрепен адреналин.
Блокирайки рецептора, лекарството елиминира активиращия ефект на адреналина върху скоростта на пулсовото генериране, предпазвайки миокарда от превишаване на енергията и неефективните му отпадъци. Това е много деликатен и ефективен механизъм, а бета-блокерите значително увеличават продължителността на живота на много пациенти със сърдечни заболявания.
Блокери на калциевите канали
Втората група вещества има по-фин механизъм на действие, макар и много ефективен. Те блокират бавните канали на калциевия поток, поради което се формира потенциала за действие. На мембраната на атипичен кардиомиоцит те се изразяват в голям брой и следователно пълната им блокада, която би се превърнала в невъзможността за развитие на автоматична сърдечна функция, е невъзможна.
Използването на лекарството постига само леко забавяне в скоростта на генериране на потенциала за действие, което спомага за намаляване на честотата на ритъма. Такъв механизъм е много надежден и позволява лечение на аритмии, използвайки за тази цел не субстрат на автоматичната функция на сърцето, а самия потенциал на действие. Това означава, че блокерите на калциевите канали не влияят върху спонтанната бавна диастолна деполяризация.
Комуникация на сърдечния автоматизъм и жизнената активност
Сърцето е съставено от мускулна тъкан, съединителна и нервна. Последната има най-малка стойност в нея, тъй като е представена само от блуждаещия нерв. Съединителна тъкан осигурява присъствието на клапани и поддържа структурата на тялото, докато мускулната е отговорна за всичко останало. Производните на мускулни клетки са атипични кардиомиоцити. Това означава, че автоматизацията на сърцето, проводящата система на сърцето и мускулната му част са функционално цяло. Те образуват автономно тяло, което може да се регулира, но не изключва влиянието на други системи на тялото.
Понятия като автоматика на сърцето, естеството на автоматизма, градиентът на автоматиката са взаимосвързани и предпазват здравето. Те поддържат живота в тялото, осигурявайки постоянно кръвоснабдяване на тъканите. Кръвта в артериите е транспортна среда за хранителни вещества и свързан кислород. Поради това се осъществява процесът на клетъчно дишане и енергиен обмен. Това е основата на функционирането на многоклетъчен организъм, при прекратяването на който неизбежната му смърт е неизбежна.