Ацетилен: химични свойства, подготовка, употреба, предпазни мерки
Ацетилен (или, според международната номенклатура, етин) е ненаситен въглеводород, принадлежащ към класа на алкините. Химичната формула на ацетилена е C2H2. Въглеродните атоми в молекулата са свързани чрез тройна връзка. Той е първият в своята хомоложна серия. Това е безцветен газ. Много лесно запалим.
приемане
Всички методи за промишлено производство на ацетилен се доближават до два вида: хидролиза на калциев карбид и пиролиза на различни въглеводороди. Последното изисква по-малко енергия, но чистотата на продукта е доста ниска. Карбидният метод е обратното.
Същността на пиролизата е, че метан, етан или друг лек въглеводород се превръщат в ацетилен при нагряване до високи температури (от 1000 ° С). Нагряването може да се извърши чрез електрически разряд, плазма или изгоряла част от суровината. Но проблемът е, че в резултат на пиролизната реакция може да се образува не само ацетилен, но и много други продукти, които трябва да се изхвърлят по-късно.
2CH4 → C2H2 + 3H2
Карбидният метод се основава на реакцията на взаимодействие на калциев карбид с вода. Калциев карбид се получава от неговия оксид чрез сливане с кокс в електрически пещи. Следователно, такава висока консумация на енергия. Но чистотата на ацетилена, получена по този начин, е изключително висока (99,9%).
CaC2 + H20 → C2H2 + Ca (OH) 2
В лабораторията ацетилен може да се получи и чрез дехидрохалогениране на дихалогенни производни на алкани, използвайки алкохолен алкален разтвор.
СН2С1-СН2С1 + 2КОН → C2H2 + 2KCl + 2H2O
Физични свойства на ацетилена
Ацетиленът е газ без цвят и мирис. Въпреки че примесите могат да му дадат чесън миризма. Практически неразтворим във вода, слабо разтворим в ацетон. При температура от -83.8 ° С се втечнява.
Химични свойства на ацетилена
Въз основа на тройната връзка на ацетилена, тя ще се характеризира чрез реакции на прибавяне и реакции на полимеризация. Водородните атоми в ацетиленовата молекула могат да бъдат заменени с други атоми или групи. Следователно, може да се каже, че ацетиленът проявява киселинни свойства. Нека разгледаме химичните свойства на ацетилена при специфични реакции.
Реакции на прикачения файл:
- Хидрогениране. Извършва се при висока температура и в присъствието на катализатор (Ni, Pt, Pd). На паладиевия катализатор може да бъде непълно хидриране.
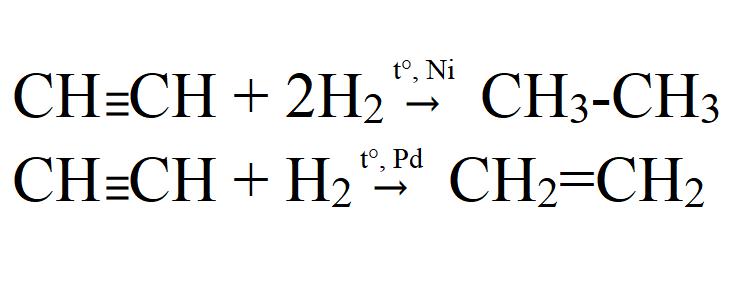
- Халогени. Тя може да бъде както частична, така и пълна. Отива лесно дори без катализатори или отопление. В светлината на хлорирането идва с експлозия. В същото време ацетиленът се разлага напълно до въглерод.
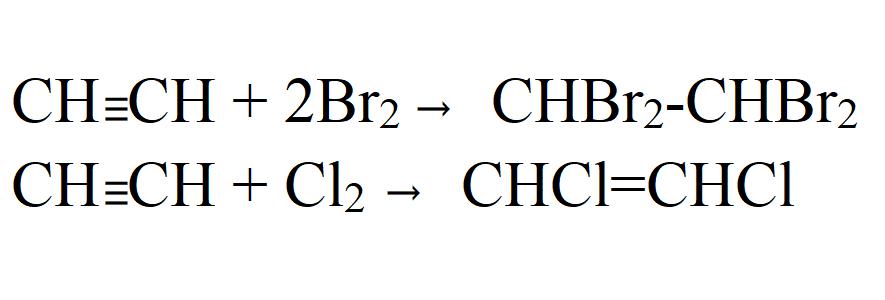
- Присъединяване към оцетна киселина и етилов алкохол. Реакциите преминават само в присъствието на катализатори.
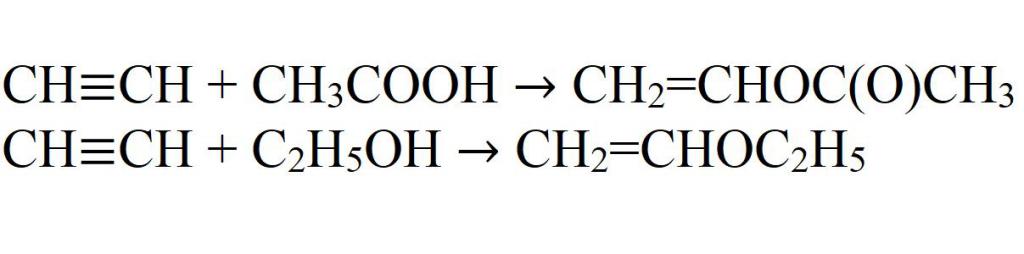
- Добавяне на циановодородна киселина.
СН = СН + HCN → CH2 = CH-CN
Реакции на заместване:
- Взаимодействието на ацетилен с метални органични съединения.
CH2CH2C2H5MgBr2C2H6 + BrMgC2CMgBr
- Взаимодействие с метален натрий. Необходима е температура от 150 ° С или предварително разтваряне на натрий в амоняк.
2CH = CH + 2Na → 2CH2CNa + Н2
- Взаимодействие със сложни соли на мед и сребро.
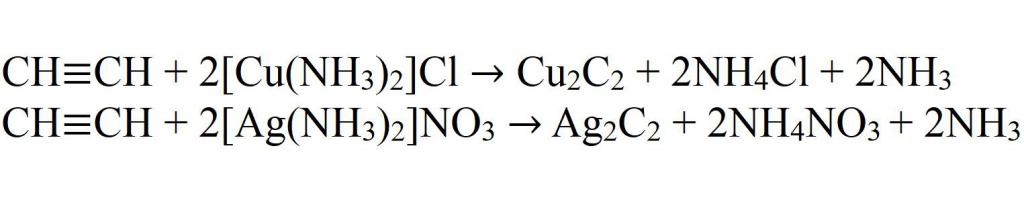
- Взаимодействие с натриев амид.
СН2СН + 2NaNH2 → NaClCNa + 2NH3
Реакции на полимеризация:
- Димеризация. В тази реакция, две ацетиленови молекули се обединяват в една. Необходим е катализатор - едновалентна медна сол.
- Тримеризиращи. При тази реакция, три ацетиленови молекули образуват бензол. Нагряване до 70 ° С, налягане и катализатор са необходими.
- Тетрамеризацията. В резултат на реакцията се получава осемчленен цикъл - циклооктатетраен. Тази реакция също изисква малко топлина, налягане и подходящ катализатор. Това обикновено са комплексни съединения на двувалентен никел.
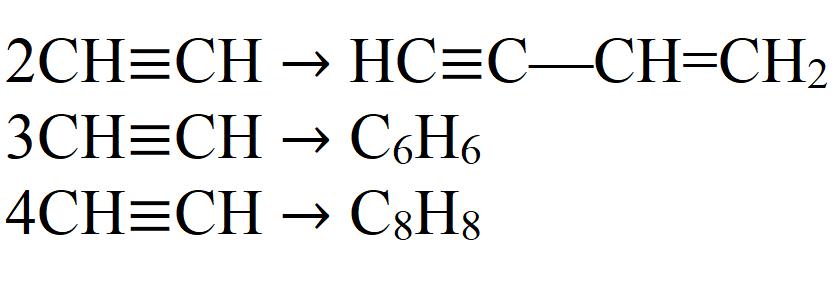
Това не са всички химични свойства на ацетилена.
приложение
Структурната формула на ацетилена ни показва сравнително силна връзка между въглеродните атоми. Когато се счупи, например по време на горене, се отделя много енергия. По тази причина ацетиленовият пламък има рекордна висока температура от около 4000 ° С. Използва се в горелки за заваряване и рязане на метал, както и в ракетни двигатели.
Пламъкът на горенето на ацетилена също има много висока яркост, така че често се използва в осветителни устройства. Използва се в експлозивна технология. Вярно е, че не се прилага самият ацетилен, а неговите соли.
Както може да се види от различни химични свойства, ацетиленът може да се използва като суровина за синтеза на други важни вещества: разтворители, лакове, полимери, синтетични влакна, пластмаси, органични стъкла, експлозиви и оцетна киселина.
безопасност
Както вече споменахме, ацетиленът е запалимо вещество. С кислород или въздух той е способен да образува изключително запалими смеси. За да предизвика експлозия, достатъчно е една искра от статично електричество, загряване до 500 ° C или малко налягане. При температура от 335 ° C чист ацетилен спонтанно се запалва.
Поради това ацетиленът се съхранява в бутилки под налягане, които се пълнят с пореста субстанция (пемза, активен въглен, азбест). Така ацетиленът се разпределя в порите, намалявайки риска от експлозия. Често тези пори се импрегнират с ацетон, поради което се образува ацетиленов разтвор. Понякога ацетиленът се разрежда с други, по-инертни газове (азот, метан, пропан).
Този газ също има токсичен ефект. При вдишване започва интоксикация на тялото. Признаци на отравяне са гадене, повръщане, шум в ушите и замаяност. Големите концентрации могат дори да доведат до загуба на съзнание.