Калциев карбид: свойства и приложение. Получаване на ацетилен
Карбидите са група от неорганични въглеродни съединения с метали, както и със силиций или бор (тъй като тези елементи проявяват метални свойства). Калциевият карбид е едно от най-търсените вещества от тази група. Относно свойствата и приложението на съединението, прочетете по-долу.
Получаване на история
Калциевият карбид е съединение, широко използвано в съвременната индустрия. През 1862 г. германският химик Фридрих Велер първо синтезира молекула от това вещество. Получавайки калциев карбид, той извършва, както следва. Ученият приготвя калциева стопилка с цинк и след това я загрява с въглища. Резултатът е карбид. Химичната формула на съединението е CaC2. Индустриалният метод за производство на карбид е предложен от ученият Муасан през 1892 година. Други имена на веществото са калциев ацетилид или калциев карбонат. Кристалната решетка на съединението е както следва:
Ad
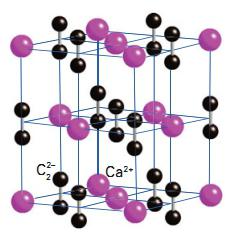
Физични свойства
Според физическите му свойства, калциевият карбид е кристално вещество с точка на топене от 2300 o C. Тази цифра е валидна само за чисти съединения. Примесите, съдържащи карбид, могат да имат други точки на топене. Основното агрегатно състояние на веществото е твърдо, а цветът варира от сиво до кафяво.
Химични свойства
Калциевият карбид абсорбира добре водата. Този процес е придружен от реакция на химическо разлагане. Важно е, че карбидният прах има дразнещо действие върху лигавиците, кожата и дихателни органи. Затова при работа със съединението е необходимо да се използват противогази или противопрашни респиратори. Калциевият карбид взаимодейства с кислород при висока температура, за да се образува калциев карбонат. Реакцията с азот води до синтез на калциев цианамид. Също така при високи температури калциевият карбид реагира с хлор, фосфор, арсен. Но все пак едно от най-важните свойства на съединението е разлагането с вода.
Ad

приемане
Производството на калциев карбид е както следва. Негасена вар и предварително натрошен кокс се смесват. Получената смес се стопява в електрически пещи. Коксът и калциевият оксид се взимат в еднакви тегловни части. Процесът протича при температура от 1900 ° С. Стопилката напуска пещта и след това се излива в специални форми. След това вече закаленият калциев карбид се раздробява и сортира според размера на парчетата. Гранулите на дадено вещество се разделят на четири фракции в съответствие с техните размери: 25 × 80, 15 × 25, 8 × 15, 2 × 8, които са определени от ГОСТ 1460-56. По своя състав технически калциев карбид съдържа 75-80% от основното вещество. Делът на примесите, като въглерод, вар и др., Съставлява до 25% от общата маса на сместа. Освен това сулфидният и калциевият фосфид, съдържащи се в техническия карбид, причиняват неговата неприятна миризма. Представете си реакцията на получаване на CaC 2 : CaO + 3C → CaC 2 + CO ↑. Образуването на калциев ацетилид е съпроводено с абсорбция на топлина. Следователно, логично е да се предположи, че реакцията на нейното разлагане, напротив, върви с освобождаването на енергия.
Ad

Транспорт и съхранение
Поради факта, че влагата моментално разлага карбида с отделянето на голямо количество топлина и образуването на взривоопасен ацетиленов газ, веществото трябва да се съхранява в херметически затворени барабани или кутии. Трябва да се помни, че ацетиленът е по-лек от въздуха и може да се натрупва в горните части на помещението. Този газ, в допълнение към наркотичното действие, има способността да се самозапали. Затова е необходимо да се използва калциев карбид с голямо внимание. Специално внимание е отделено на опаковката в производството. Готовото вещество се поставя в специални барабани (контейнер наподобяващ кутии). Такива опаковки изискват внимателно отваряне. Трябва да се използва инструмент, който не води до образуване на искри (чук или специален нож). В случай на карбид върху кожата или лигавиците, трябва незабавно да измиете засегнатата област с вода и да третирате мястото с вазелин или мазен крем. Транспортирането на връзката се извършва, като се използва само покритието видове транспорт. Доставката на карбид във въздуха е забранена. Помещенията, в които се съхранява CaC 2, трябва да бъдат добре проветрени. Също така не е позволено да се съхранява карбид заедно с други химикали. Това може да доведе до нежелани и вероятно опасни реакции. Срокът на годност на карбида е шест месеца.

приложение
Обхватът на калциевия карбид е изключително широк. На първо място, това е индустриален синтез. Калциевият карбид се използва за производство на синтетичен каучук, оцетна киселина, ацетон, етилен, винилхлорид, стирен. Намира приложение и при приготвянето на калциев цианамид. Това вещество е ценно за използването му при синтеза на различни торове и цианидни вещества. В селското стопанство всеки агроном знае такова име като регулатор на карбид-карбамид. Използва се за регулиране на растежа на растенията. За да се получи също се използва калциев карбид. В допълнение, това съединение се използва в производството на калциев цианамид. Тази реакция се основава на нагряване на калциев карбид с азот. възстановяване алкални метали също така и без използването на описаното от нас вещество. Калциевият карбид се използва в процеса на газовото заваряване. Например, широко се използват карбидни лампи. Принципът на тяхната работа се основава на взаимодействието в специален контейнер с карбид с вода и изгарянето на изхода на апарата от крайното вещество на реакцията - ацетилен. Вижте снимката на карбидната лампа.
Ad

Производство на ацетилен
Едно от най-важните приложения на калциевия карбид е използването му в производството на ацетилен. Кредитът за откриването на този метод принадлежи и на германския химик Фридрих Валер. В основата на този промишлен процес е реакцията на разлагане на карбид под влиянието на вода. CaC2 + 2H2O → C2H2 + Ca (OH) 2 ' . На изхода се образува ацетиленов газ хидратна вар, утаява. Процесът е придружен от отделянето на голямо количество топлина. Обемът на газа на изхода зависи от това колко чист е калциевият карбид за реакцията. Полученият в резултат на това ацетилен може да има различен обем - 1 kg от първоначалното вещество може да даде от 235 до 290 литра газ. Що се отнася до скоростта на реакцията, тя зависи както от малък процент примеси в калциевия карбид, така и от температурата на водата, както и от неговата чистота. Ако разгледаме теоретичната реакция на производството на ацетилен от карбид, тогава 560 мл вода е достатъчно за 1 кг карбид. На практика, обаче, обемът на водата за реакцията се увеличава. На 1 кг калциев карбид в условията на промишлен синтез се изисква от 5 до 20 литра вода. Това количество е необходимо, за да се гарантира по-добро охлаждане на ацетилена, както и да се осигури оптимална безопасност по време на работа. По-долу е немският химик Фридрих Велер.
Ad

Лазерен опит с ацетилен
Много от уроците по химия в училище са запознати с реакцията на взаимодействие между карбид и вода. Обикновено този опит ни позволява да демонстрираме реакцията за получаване на ацетилен, както и неговите физични и химични свойства. В същото време процесът на отделяне на газ протича доста енергично, така че тръбата, която изсмуква ацетилена от колбата с активните вещества, се поставя в купа с вода. Това осигурява по-малко активно и бързо движение на газа. В допълнение, в лабораторията, можете да използвате друг начин да направите не твърде силна реакция на разлагане на такива съединения като карбид. Ацетиленът в този случай отива равномерно и спокойно. За да направите това, вместо вода, трябва да вземете наситен разтвор на сол. Също така в лабораторията при провеждането на тази реакция водата трябва внимателно да се добави към карбида, поставен в мерителната колба, а не обратно.