Какво е разпределението на електроните в енергийните нива на различни химически елементи?
Разпределението на електроните в енергийните нива обяснява както металните, така и неметалните свойства на всички елементи.
Електронна формула
Съществува определено правило, според което свободните и сдвоени негативни частици се поставят на нива и поднива. Нека разгледаме по-подробно разпределението на електроните по енергийни нива.
На първото енергийно ниво има само два електрона. Орбиталите се запълват от тях с увеличаването на енергийните доставки. Разпределението на електроните в атома на химичния елемент съответства на поредния номер. На енергийни нива с минимален брой най-силно изразени привлекателна сила валентни електрони към ядрото.
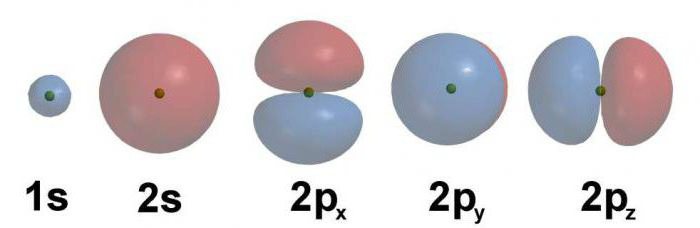
Пример за електронната формула
Помислете за разпределението на електроните от енергийни нива чрез примера на въглероден атом. Последователният му номер е 6, следователно шест протони с положителен заряд са разположени вътре в ядрото. Като се има предвид, че въглеродът е представител на втория период, той се характеризира с наличието на две енергийни нива. На първия има два електрона, на втория - четири.
Правилото на Хун обяснява подреждането в същата клетка само на два електрона, които имат различни завъртания. На второто енергийно ниво има четири електрона. В резултат на това разпределението на електроните в един атом на химически елемент има следната форма: 1s22s22p2.
Съществуват определени правила, според които разпределението на електроните по нива и нива.
Принцип на Паули
Този принцип е формулиран от Паули през 1925 година. Ученият е съгласен с възможността за поставяне в атома само на два електрона, които имат еднакви квантови числа: n, l, m, s. Имайте предвид, че разпределението на електроните в енергийните нива се получава, когато запасът от свободна енергия се увеличава.
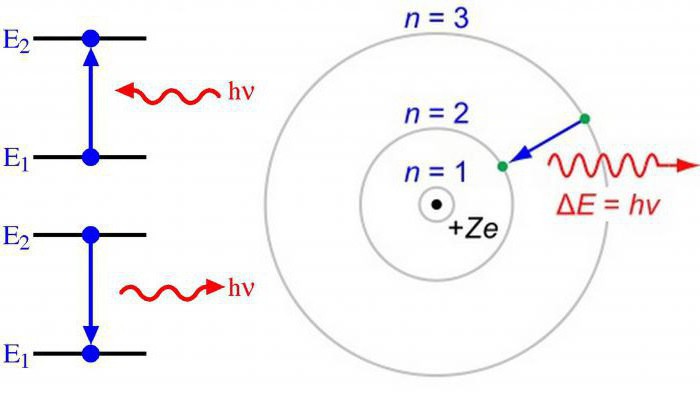
Правило Клечковски
Запълването на енергийните орбитали се извършва според увеличаване на квантовите числа n + l и се характеризира с увеличаване на енергийния резерв.
Разгледайте разпределението на електроните в калциевия атом.
В нормалното състояние електронната му формула има следната форма:
Ca 1s2 2s2 2p6 3s2 3p6 3d0 4s2.
Елементи от подобни подгрупи, свързани с d- и f-елементи, има "провал" на електрона от външното подниво, което има по-малък енергиен резерв от предишния d- или f-подниво. Подобно явление е характерно за мед, сребро, платина, злато.
Разпределението на електроните в един атом включва пълнене на поднива с несвързани електрони, които имат еднакви завъртания.
Едва след като всички свободни орбитали са напълно запълнени с единични електрони, квантовите клетки се допълват с втори отрицателни частици, надарени с противоположни завъртания.
Например, в невъзбудено състояние на азота:
1s2 2s2 2p3.
Свойствата на веществата имат ефект електронна конфигурация валентни електрони. По техния брой можете да определите по-висока и по-ниска валентност, химическа активност. Ако елементът е в основната подгрупа на периодичната таблица, е възможно чрез номера на групата да се направи външното енергийно ниво, да се определи окислителни състояния. Например, фосфорът, който е в петата група (основна подгрупа), съдържа пет валентни електрона, следователно е способен да приеме три електрона или да даде пет частици на друг атом.
Изключенията от това правило са всички представители на подгрупите на периодичната таблица.
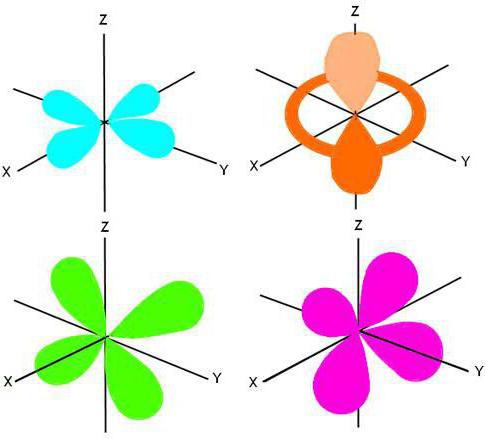
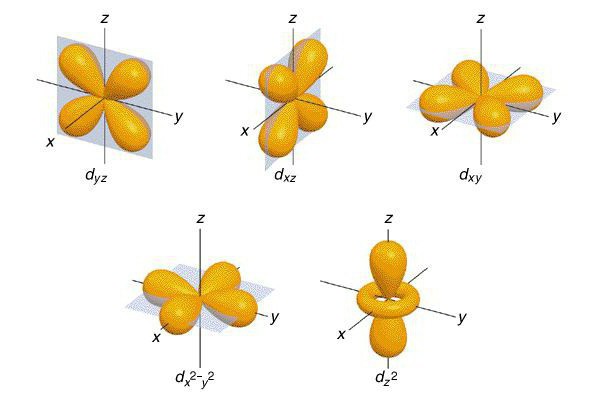
Семейни функции
В зависимост от структурата на външното енергийно ниво, има разделяне на всички неутрални атоми в Периодичната таблица на четири семейства:
- s-елементите са в първата и втората групи (основни подгрупи);
- р-семейството е разположено в III-VIII групи (A подгрупи);
- d-елементите могат да бъдат намерени в подобни подгрупи от I до VIII група;
- Семейството f се състои от актиниди и лантаниди.
Всички s-елементи в нормалното състояние имат валентни електрони на s-поднива. Наличието на свободни електрони при s- и p-поднива е характерно за р-елементите.
D-елементите в невъзбуденото състояние имат валентни електрони както на последното s-, така и на последното, но едно под-ниво.
заключение
Състоянието на всеки електрон в атома може да бъде описано с помощта на набор от основни числа. В зависимост от характеристиките на неговата структура, можем да говорим за определено количество енергия. Използвайки правилото Hund, Klechkovsky, Pauli за всеки елемент, включен в периодичната таблица, можете да създадете конфигурация на неутрален атом.
Електроните, разположени на първите нива, имат най-малко количество енергия в неизгорялото състояние. При нагряване на неутрален атом се наблюдава преход на електрони, който винаги се съпровожда от промяна в броя на свободните електрони, което води до значителна промяна в скоростта на окисление на елемента и промяна в неговата химична активност.