Вторият закон на термодинамиката. Тълкуване, теоретична и практическа обосновка
Във физиката, тъй като е точна наука, повечето догми се доказват емпирично. Така е получен вторият закон на термодинамиката, който в момента се изучава във всяко училище. Необратими термични процеси - така казва той. Заслужава да се отбележи, че на началните етапи на проучването подобно тълкуване е много по-разбираемо.
Общи изгледи
Физическият принцип, който ограничава посоката на различните процеси в България термодинамични системи е вторият закон на термодинамиката. Определението на този термин е формирано през 19 век, първо от Рудолф Клаузис, а след това от Уилям Томсън (лорд Келвин). В съответствие с двата постулата в света не може да съществува един вид машина за вечно движение от втория вид. Няма и няма да има такава инсталация, която да загрява, излъчва от всички неща, живи същества и явления, да се превърне в енергия за своята постоянна работа. На базата на това беше изведено правилото, че ефективността не може да бъде равна на единица. Това може да се сравни с работата на хладилника, където температурата, например, ще бъде равна на абсолютна нула. При такива условия кръговият обмен на топлина се изключва. 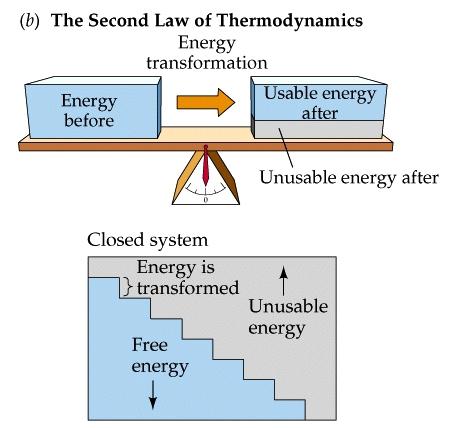
Състав на Рудолф Клаузис
Първият изказа втори закон на термодинамиката Р. Клаузис - немски физик и математик. Според него, кръгъл процес, в който резултатът се постига чрез прехвърляне на топлина от по-малко нагрято тяло към по-нагрято, е невъзможен. С други думи, температурата изцяло или частично може свободно да се движи от по-топло тяло към по-хладно, но този процес не може да се случи в обратна посока. Това ясно ни показва липсата на цикличност, порочен кръг. Такива концепции са неприемливи за термодинамиката. Топлината се обменя просто между телата и в резултат на тези действия не се произвежда излишна енергия. 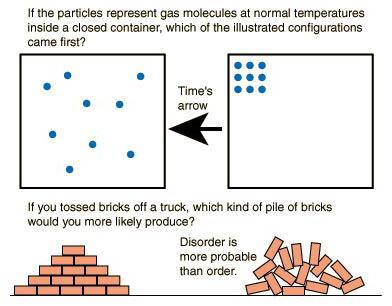
Постулат, извлечен от лорд Келвин
Подобна дефиниция на втория закон на термодинамиката, получен в писанията на Томсън - британски физик и механика. Теоретично това звучи така: "Цикличен процес, единственият резултат от който може да бъде работата, получена чрез охлаждане на топло тяло или резервоар, е невъзможна." За да разберем по-ясно тази интерпретация, нека си представим определена машина (тя не може да съществува според термодинамичния постулат). Той периодично охлажда резервоара с постоянно гореща вода, получавайки от тази топлинна енергия. Благодарение на тази енергия, машината вдига различни товари като строителния кран. В този случай няма двигател, електроцентрали и друго механично пълнене. По отношение на емпиричната физика, това е невъзможно. 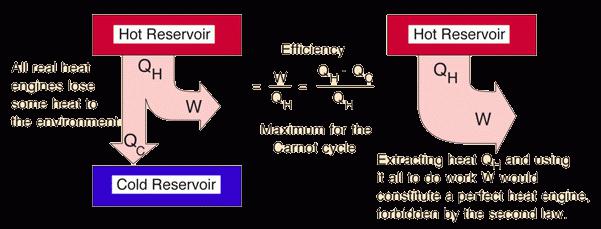
Какво е общото?
Сега ще разгледаме как тези две интерпретации са комбинирани и върху които принципно се основава вторият закон на термодинамиката. Ентропията е мярката на хаоса, която се увеличава в процеса на обмен на топлина. Това е свързващ елемент за описанието на Клаузис и Келвин. Но малко назад. Вторият закон на термодинамиката казва, че когато се заменя топлината, енергията намалява (следователно, получаването на работа не е възможно изобщо), но в същото време мярката на хаоса се увеличава. Този процес е необратим и често се нарича спонтанен. В термодинамиката ентропията непрекъснато се умножава, но нейното унищожаване е невъзможно. Ето защо дори 100 процента от енергията, която е във всяко тяло, не може да се трансформира в работа. 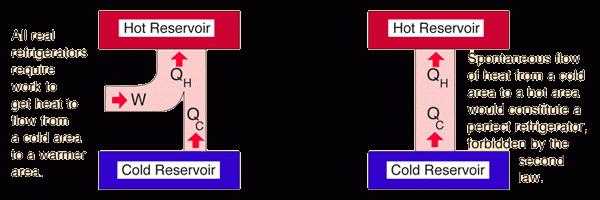
Каква е мярката на хаоса?
Понятието за ентропия за първи път е формулирано от устата на Клаузис. Използва се за определяне на мярката на необратимия процес на разсейване на енергия. Това беше нещо като разлика в отклонението на реалния процес от идеала. Ентропията в затворени системи, където всички процеси протичат циклично, има постоянна стойност. Ако процесът е необратим (което пряко засяга термодинамиката), тогава ентропията винаги има положителен смисъл. Заслужава да се отбележи, че мярката на хаоса се генерира от абсолютно всички процеси, които се случват във Вселената. С постоянни показатели за обема и енергията на тялото или резервоара, ентропията непрекъснато се увеличава. Ако тези цифри се променят периодично, тогава мярката на хаоса може да бъде намалена поради извършената работа, но пълното й унищожаване е невъзможно. Трябва да се отбележи, че ентропията на Вселената не намалява. Той остава нормален или постоянно нараства.
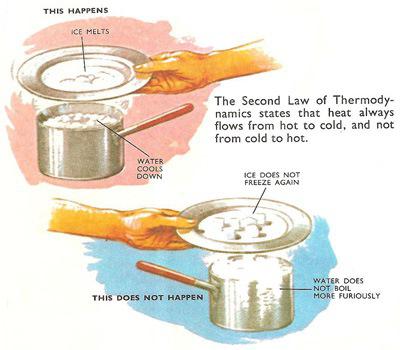
Пример за пример
Вторият закон на термодинамиката може да се обясни със стандартен пример, който често се дава на учениците. Имаме две тела с различни температури. По-нагрятото вещество ще отделя топлината си по-малко нагрята, докато техните температурни стойности станат равни. По време на този процес ентропията на първото по-топло тяло ще намалее с по-малка цифра, отколкото ще се увеличи във второто, по-хладно тяло. В резултат на това такъв спонтанен процес ще създаде ентропията на системата, чийто индекс ще бъде по-висок от общата стойност на ентропията на две тела в първоначалната позиция. С други думи, мярката на хаоса на системата от две вещества, получена от обмяната на топлина, се е увеличила. 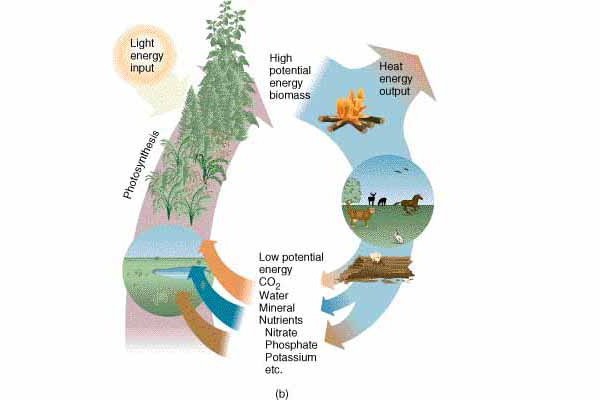
Термална смърт на Вселената
Когато провеждаше своите проучвания, Клаузис заключава, че независимо от това колко отворено ни изглежда пространството (нашата планета, нейните отделни територии, водни площи и т.н.), всичко това е в космоса. Вселената от своя страна е най-голямото затворено пространство, в което се извършват макроскопични процеси. Поради факта, че в една затворена система ентропията непрекъснато увеличава своя индекс, нашият свят се доближава до факта, че скоро в него мярката на хаоса ще достигне безкрайна стойност. Това означава, че всички процеси просто спират поради факта, че енергията е изтощена. Такава критична точка, която ще достигнем, може би, в определено бъдеще, е получила името на термичната смърт. Оказва се, че всички наши действия (движения, ходене, бягане), всички явления, които се случват на планетата (полъх на вятър, цунами, движение на литосферни плочи) - всичко това води до необратимо увеличаване на ентропията и изчерпване на енергията.
Опровержение на теорията
Човекът все още не може да съди за целия космос. Ние виждаме само част от света, в който живеем, и изследваме този ъгъл, доказвайки определени закони и формирайки собствените си идеи въз основа на това. Следователно, първото опровержение на възможността за термична смърт, която се основава на втория закон на термодинамиката, е, че Вселената може да не е затворена система. Известно е със сигурност, че 85% от космоса се състои от антиматерия, чиито свойства не са известни на никой. Второто опровержение е, че нашият космос, дори и да е затворен, е непрекъснато колебание. Поради различни колебания и промени в размера, масата, енергията и температурата, ентропията не се увеличава (в общата универсална стойност) и не намалява. Следователно, ние вече сме в състояние на термодинамично равновесие или, според думите на Клаузис, в състояние на термична смърт.
Обобщава
Вторият закон на термодинамиката е неразривно свързан с развитието на точните науки. Тя е отворена в зората на научно-техническия прогрес и става, може да се каже, отправна точка за по-нататъшна работа на учените в областта на математиката, физиката и астрономията. Трябва да се отбележи, че ние представяме всичко това особено в земни условия. Вероятно в различна среда, където гравитационните полета имат различна сила, термодинамиката ще работи по напълно различна схема.