Серен диоксид - физични свойства, подготовка и употреба
Серен диоксид има молекулна структура, подобна на озона. Серният атом, разположен в центъра на молекулата, е свързан с два кислородни атома. Този газообразен продукт на окисляване на сяра няма цвят, произвежда силна миризма и когато условията се променят, лесно се кондензира в бистра течност. Веществото е добре разтворимо във вода, има антисептични свойства. SO 2 се произвежда в големи количества в химическата промишленост, а именно в производствения цикъл на сярната киселина. Газът се използва широко за преработка на селскостопански и хранителни продукти, избелващи тъкани в текстилната промишленост.
Системни и тривиални наименования на вещества
Необходимо е да се разбере разнообразието от термини, свързани с едно и също съединение. Официалното наименование на съединението, чийто химичен състав отразява формулата SO 2 , е серен диоксид. IUPAC препоръчва да се използва този термин и неговият английски еквивалент - Серен диоксид. Учебници за училища и университети по-често споменават такова име - серен оксид (IV). Римската цифра в скоби показва валентността на атома S. Кислородът в този оксид е бивалентен, а окислителният брой на сярата е +4. В техническата литература се използват такива остарели термини като серен диоксид, анхидрид на сярна киселина (продукт на неговата дехидратация).
Ad
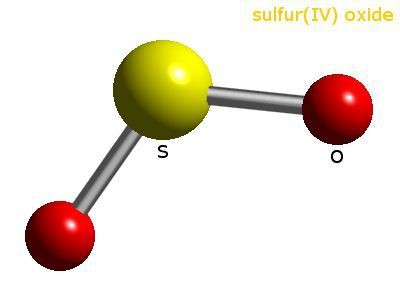
Състав и молекулярна структура на SO 2
Молекулата SO2 се формира от един серен атом и два кислородни атома. Между ковалентните връзки има ъгъл от 120 °. Сп2 хибридизацията се случва в серен атом - те са подредени във форма и енергия на облак от един s и два p-електрона. Те участват в образованието. ковалентна връзка между сяра и кислород. В една O - S двойка, разстоянието между атомите е 0,143 nm. Кислородът е по-електроотрицателен елемент от сярата, което означава, че свързващите двойки електрони се изместват от центъра към външните ъгли. Цялата молекула също е поляризирана, отрицателният полюс е О-атома, положителният е S-атом.
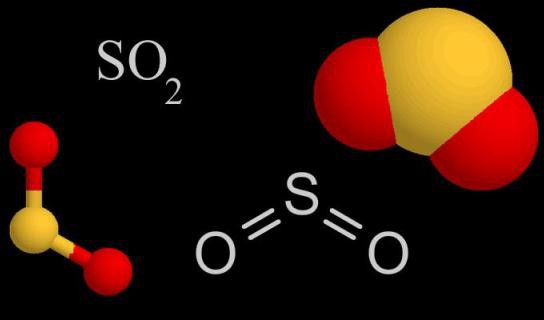
Някои физични параметри на серен диоксид
Оксидът на четиривалентната сяра при нормални условия на околната среда запазва газовото агрегирано състояние. Формулата на серен диоксид позволява определянето на относителната му молекулна и моларна маса: Mr (SO 2 ) = 64.066, М = 64.066 g / mol (може да бъде закръглено до 64 g / mol). Този газ е почти 2,3 пъти по-тежък от въздуха (M (въздух) = 29 g / mol). Диоксидът има остър, специфичен мирис на горяща сяра, което е трудно да се обърка с всеки друг. Това е неприятно, дразни лигавиците на очите, причинява кашлица. Но серният оксид (IV) не е толкова токсичен, колкото сероводород.
Ad
Под налягане при стайна температура газообразният серен диоксид се втечнява. При ниски температури веществото е в твърдо състояние, се топи при –72 ... –75,5 ° С. При по-нататъшно повишаване на температурата се появява течност, а при –10,1 ° С се образува газ. SO2 молекулите са термично стабилни, разлагането на атомна сяра и молекулярният кислород се среща при много високи температури (около 2800 ºС).

Разтворимост и взаимодействие с вода
Серен диоксид, когато се разтвори във вода, частично реагира с него, за да образува много слаба сярна киселина. В момента на получаването му той незабавно се разлага на анхидрид и вода: SO2 + H20O2H2S03. Всъщност решението не е налице сярна киселина и хидратирани SO2 молекули. Газовият диоксид взаимодейства по-добре с хладка вода, като разтворимостта му намалява с повишаване на температурата. При нормални условия, той може да се разтвори в 1 обем вода до 40 обема газ.
Ad
Серен диоксид в природата
Значителни количества серен диоксид се отделят с вулканични газове и лава по време на изригвания. Много видове човешки дейности също водят до увеличаване на концентрацията на SO 2 в атмосферата.

Сярен анхидрид се доставя във въздуха от металургични заводи, където отработените газове не се улавят по време на изгарянето на рудата. Много видове изкопаеми горива съдържат сяра, в резултат на което се отделят значителни количества серен диоксид в атмосферния въздух, когато се изгарят въглища, петрол и газ. Серен диоксид става токсичен за хората при концентрации във въздуха над 0,03%. При човек започва недостиг на въздух, може да се появят симптоми като бронхит и пневмония. Много високите концентрации на серен диоксид в атмосферата могат да доведат до тежко отравяне или смърт.
Серен диоксид - производство в лаборатория и в промишлеността
Лабораторни методи:
- Когато сярата се изгаря в колба с кислород или въздух, се получава диоксид по формулата: S + O2 = SO2.
- Възможно е да се действа върху солите на сярната киселина с по-силни неорганични киселини, по-добре е да се приема солна киселина, но е възможно да се разрежда сярната:
- Na2S03 + 2HCl = 2NaCl + H2SO3;
- Na2S03 + H2S04 (d) = Na2S04 + H2SO3;
- H2S03 = Н20 + S02.
3. Когато мед взаимодейства с концентрирана сярна киселина, не се отделя водород, а серен диоксид:
2H2S04 (конц.) + Cu = CuS04 + 2H2O + SO2.
Съвременни методи за промишлено производство на серен диоксид:
- Окисляване на естествена сяра при изгаряне в специални пещи: S + O 2 = SO 2 .
- Изпичане на железен пирит (пирит).
Основни химични свойства на серен диоксид
Сярният диоксид е активно химично съединение. При окислително-редукционните процеси това вещество често действа като редуциращ агент. Например, при взаимодействието на молекулен бром със серен диоксид, реакционните продукти са сярна киселина и бромоводород. Окислителните свойства на SO2 се появяват, когато този газ се премине през сероводород. В резултат на това се освобождава сяра, настъпва самоокисляване-самоограничаване: SO2 + 2H2S = 3S + 2H2O.
Серен диоксид проявява киселинни свойства. Тя съответства на една от най-слабите и най-нестабилните киселини - сярна. Това съединение не съществува в чист вид, възможно е да се открият киселинните свойства на разтвор на серен диоксид чрез индикатори (лакмус е розово). Сярната киселина дава средни соли - сулфити и киселинно-хидросулфити. Сред тях са стабилни съединения.
Ad
Процесът на окисление на сярата в диоксид до шестивалентното състояние в анхидрид на сярна киселина е каталитичен. Полученото вещество се разтваря енергично във вода, взаимодейства с молекули Н 2 О. Реакцията е екзотермична, образува се сярна киселина, или по-скоро, нейната хидратирана форма.
Практическо използване на серен диоксид
Основният метод за промишлено производство на сярна киселина, който изисква диоксид на елемента, има четири етапа:
- Получаване на серен диоксид чрез изгаряне на сяра в специални пещи.
- Пречистване на получения серен диоксид от всички видове примеси.
- По-нататъшно окисление до шестивалентна сяра в присъствието на катализатор.
- Абсорбция на сяра триоксид от вода.
Преди това почти целият серен диоксид, необходим за производството на сярна киселина в промишлен мащаб, се получава чрез изпичане на пирит като страничен продукт от производството на стомана. Новите видове преработка на металургични суровини използват по-малко изгарянето на рудата. Ето защо, през последните години, естествената сяра се превърна в основен изходен материал за производството на сярна киселина. Значителни глобални запаси от тази суровина, неговата наличност ни позволява да организираме мащабна обработка.
Ad

Серен диоксид се използва не само в химическата промишленост, но и в други сектори на икономиката. Текстилните мелници използват това вещество и продуктите от неговото химично взаимодействие, за да избелват коприна и вълнени тъкани. Това е един от видовете избелване без хлор, при което влакната не се разрушават.
Серен диоксид има отлични дезинфекционни свойства, които се използват в борбата с гъбичките и бактериите. Сернокиселият анхидрид се фумигира със съхранение на селскостопански продукти, винени бъчви и изби. Използва се SO 2 в хранителната промишленост като консервант и антибактериално вещество. Добавете го в сиропи, накиснете пресните плодове в него. Sulfitizatsiya
Сокът от захарно цвекло обезцветява и дезинфекцира суровините. Консервираните зеленчукови пюрета и соковете съдържат също серен диоксид като антиоксидант и консервант.
