Свойства на соли: физични и химични
Всеки ден се сблъскваме с соли и дори не мислим за ролята, която играят в нашия живот. Но без тях водата нямаше да е толкова вкусна и храната нямаше да донесе удоволствие, а растенията нямаше да растат, а животът на земята не би могъл да съществува, ако в нашия свят нямаше сол. Какви са тези вещества и какви свойства на солите ги правят незаменими?
Какво е сол
В композицията е най-многобройният клас, отличаващ се с разнообразие. это продукт реакции между кислотой и основанием, при которой водородный атом заменяется металлическим. Още през 19-ти век химикът J. Vercelius определя солта - това е продукт на реакцията между киселина и основа, в която водородният атом е заменен с метален. Във вода, соли обикновено се дисоциират в метал или амоний (катион) и киселинен остатък (анион).

Можете да получите сол по следните начини:
- чрез взаимодействието на метал и неметал, в този случай той няма да съдържа кислород;
- когато метал взаимодейства с киселина, се получава сол и се освобождава водород;
- металът може да измести друг метал от разтвора;
- кислотного и основного (еще их называют оксидом неметалла и оксидом металла соответственно); при взаимодействието на два оксида , кисели и алкални (те се наричат съответно неметални оксиди и метални оксиди);
- реакцията на металния оксид и киселината произвежда сол и вода;
- реакцията между основата и неметалния оксид също дава сол и вода;
- като се използва реакция на йонообмен, могат да реагират различни водоразтворими вещества (бази, киселини, соли), но реакцията ще продължи, ако във водата се образуват газ, вода или слабо разтворими (неразтворими) соли.
Свойствата на солите зависят единствено от химичния състав. Но първо, нека погледнем техните класове.
класификация
В зависимост от състава се разграничават следните класове соли:
- за съдържанието на кислород (съдържащо кислород и кислород);
- при взаимодействие с вода (разтворимо, слабо разтворимо и неразтворимо).
Такава класификация не отразява напълно разнообразието на веществата. Модерната и най-пълна класификация, отразяваща не само състава, но и свойствата на солите, е представена в следващата таблица.
| Солта | |||||
|---|---|---|---|---|---|
| нормален | кисел | основен | двойно | хибрид | комплекс |
| Водородът е напълно заменен | Водородните атоми не са напълно заменени с метал | Базовите групи се заменят с киселинен остатък не напълно | Състои се от два метала и един киселинен остатък | Състои се от един метален и два киселинни остатъка | Сложни вещества, състоящи се от комплексен катион и анион или катион и комплексен анион |
| NaCl | KHSO 4 | FeOHSO 3 | KNaSO 4 | CaClBr | [Cu (NH3) 4 ] SO4 |
Физични свойства
Колкото и широк да е класът на тези вещества, възможно е да се откроят общите физични свойства на солите. Това са вещества с немолекулна структура с йонна кристална решетка.
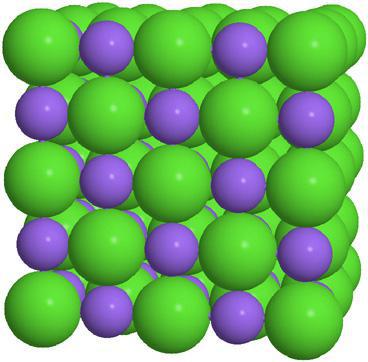
Много високи точки на топене и кипене. При нормални условия, всички соли не извършват електричество, но повечето от тях са напълно проводими в разтвора.
Цветът може да бъде много различен, зависи от металния йон, който е част от него. Железен сулфат (FeSO 4 ) е зелен, железен хлорид (FeCl 3 ) е тъмно червен, а калиев хромат (K 2 CrO 4 ) е красив, ярко жълт цвят. Но повечето соли са все още безцветни или бели.
Ad

Разтворимостта във вода също варира и зависи от състава на йони. По принцип всички физични свойства на солите имат особеност. Те зависят от кой метален йон и кой киселинен остатък е включен в състава. Ние продължаваме да разглеждаме солта.
Химични свойства на солите
И тук има важна характеристика. Както физическите, така и химическите свойства на солите зависят от техния състав. А също и на кой клас принадлежат.

Но общите свойства на солите все още могат да бъдат разграничени:
- много от тях се разлагат при нагряване, за да образуват два оксида: киселинен и основен, и безкислороден - метален и неметален;
- соли взаимодействат с други киселини, но реакцията протича само ако солта съдържа киселинен остатък от слаба или летлива киселина, или резултатът е неразтворима сол;
- взаимодействие с алкали е възможно, ако катионът образува неразтворима основа;
- възможна е реакция между две различни соли, но само ако една от новообразуваните соли не се разтваря във вода;
- може да възникне реакция с метала, но е възможно само ако вземем метал, разположен вдясно от диапазона на напрежението от метала, съдържащ се в солта.
Химичните свойства на нормалните соли са разгледани по-горе, докато други класове реагират с вещества по малко по-различен начин. Но разликата е само върху продуктите на изхода. По принцип всички химични свойства на солите се запазват, както и изискванията към реакциите.