Как да се определи степента на окисление: периодичната таблица и алгоритъмът на действие
Как да се определи степента на окисление? Периодичната таблица ви позволява да записвате това количество за всеки химичен елемент.
дефиниция
Да започнем с това, нека се опитаме да разберем какво е този термин. Състояние на окисляване според периодичната таблица тя представлява броят на електроните, които се приемат или отдават от елемент в процеса на химичното взаимодействие. Тя може да има отрицателна и положителна стойност.

Връзка към таблица
Как се определя степента на окисление? Периодичната таблица се състои от осем групи, разположени вертикално. Във всяка от тях има две подгрупи: основната и средната. За да се определят индикатори за елементи, е необходимо да се използват определени правила.
Ad
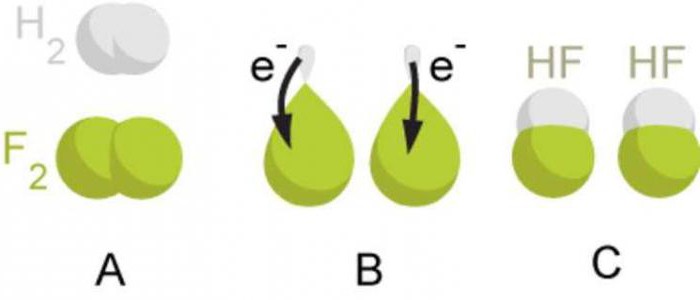
инструкция
Как да се изчисли степента на окисление на елементите? Таблицата ви позволява напълно да се справите с този проблем. Алкални метали които са разположени в първата група (основна подгрупа), степента на окисление се проявява в съединенията, тя съответства на +, е равна на тяхната по-висока валентност. Металите на втората група (подгрупа А) +2 окислително състояние.
Таблицата ви позволява да определите тази стойност не само за елементи с метални свойства, но и за неметали. Максималната им стойност ще съответства на най-високата валентност. Например, за сярата ще бъде +6, за азот +5. Как се изчислява минималната (най-ниската) стойност? Таблицата отговаря на този въпрос. Необходимо е да се извади числото на групата от осем. Например, в кислород ще бъде -2, в азота -3.
За прости вещества, които не влизат в химично взаимодействие с други вещества, определяният индекс се счита за нула.
Да се опитаме да идентифицираме основните действия, свързани с подреждането в бинарните съединения. Как да се постави в тях степента на окисление? Периодичната таблица помага за решаването на проблема.
Например, вземете калциев оксид CaO. За калций, разположен в основната подгрупа на втората група, стойността ще бъде константа, равна на +2. За кислород с неметални свойства, този индикатор ще бъде отрицателна стойност и съответства на -2. За да проверим точността на дефиницията, обобщаваме получените числа. В резултат на това получаваме нула, следователно изчисленията са правилни.
Ad
Подобни показатели се дефинират в друго бинарно съединение CuO. Тъй като медта е разположена във вторична подгрупа (първата група), следователно, изследваният индикатор може да показва различни стойности. Следователно, за да го определите, трябва първо да определите индикатора за кислород.
В неметал, разположен в края на бинарна формула, степента на окисление има отрицателна стойност. Тъй като този елемент се намира в шестата група, при изваждане от осем на шест, получаваме, че окислителното състояние на кислорода съответства на -2. Тъй като няма индекси в съединението, индексът на окисление на медта ще бъде положителен, равен на +2.
Как иначе се използва химическата таблица? Степента на окисление на елементите във формулите, състоящи се от три елемента, също се изчислява по специфичен алгоритъм. Първо, поставете тези индикатори в първия и последния елемент. За първия, този индикатор ще има положителна стойност, съответства на валентността. В крайния елемент, който служи като неметален, този индикатор има отрицателна стойност, дефинира се като разлика (номер на група се взема от осем). При изчисляване на степента на окисление на централния елемент се използва математическо уравнение. В изчисленията се вземат предвид индексите, които са налични за всеки елемент. Сумата от всички окислителни състояния трябва да бъде нула.
Ad
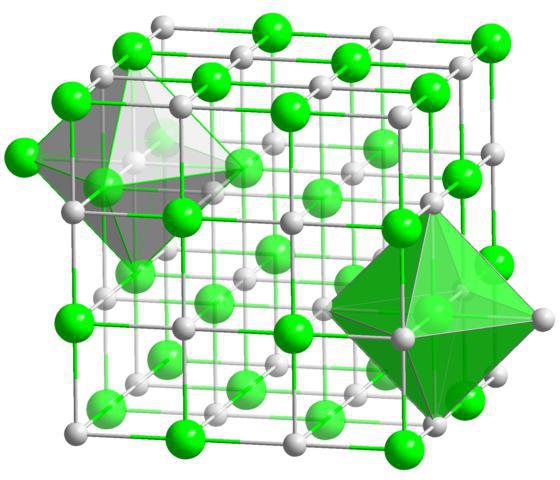
Пример за определяне в сярна киселина
Формулата за това съединение е H2SO4. В водорода състоянието на окисление ще бъде +1, в кислорода - -2. За да се определи степента на окисление в сяра, правим математическото уравнение: + 1 * 2 + X + 4 * (-2) = 0. Получаваме, че степента на окисление в сяра съответства на +6.
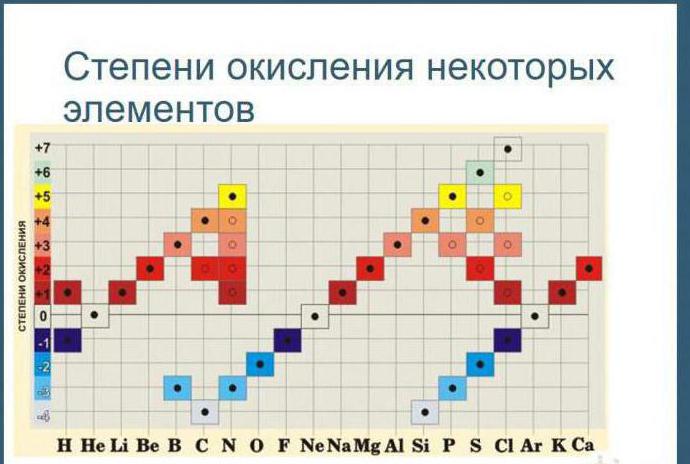
заключение
Когато използвате правилата, можете да подредите коефициентите в окислително-редукционните реакции. Този въпрос е разгледан в деветия клас по химия в училищната програма. В допълнение, информация за степените на окисление ви позволява да изпълнявате задачи OGE и EGE.