Енергията на Гибс и нейното използване за описване на възможността за процесите
Концепцията за свободната енергия на Гибс беше въведена в химията, за да се обясни възможността за спонтанно или спонтанно възникване на определена реакция. Изчисляването на тази енергия изисква познаване на промяната в ентропията на процеса и количеството енергия, което се абсорбира или освобождава по време на неговото прилагане.
Йосия Уилард Гибс

Свободна енергия, която определя възможността за различни процеси, се обозначава с буквата G. Тя е наречена енергия на Гибс в чест на американския теоретик-физик на Йосая Уилард Гибс от 19-ти век, който е допринесъл съществено за развитието на съвременната теория на термодинамиката.
Интересно е да се отбележи, че неговата първа теза, след като защитава Гибс, получава титлата доктор, пише за формата на зъбите на зъбните колела. В това проучване той използва геометрични методи, за да развие идеалната форма на тези зъби. Ученият започва да изучава термодинамиката едва на възраст от 32 години и в тази област на физиката постига голям успех.
Основни термодинамични понятия
Стандартната енергия на Гибс е енергия при стандартни условия, т.е. при стайна температура (25 ° С) и атмосферно налягане (0,1 МРа).
За да се разберат основните принципи на термодинамиката, трябва да се въведат и понятията ентропия и енталпия на системата.
Енталпията се разбира като вътрешна енергия на система, която е при дадено налягане и обем. Тази стойност се обозначава с латинската буква H и е равна на U + PV, където U - вътрешна енергия системи, P - налягане, V - обем на системата.
Ентропията на системата е физическа величина, която характеризира мярката на разстройството. С други думи, ентропията описва местоположението на частиците, които изграждат тази система, т.е. характеризира вероятността за съществуването на всяко състояние на тази система. Обикновено се обозначава с латинската буква S.
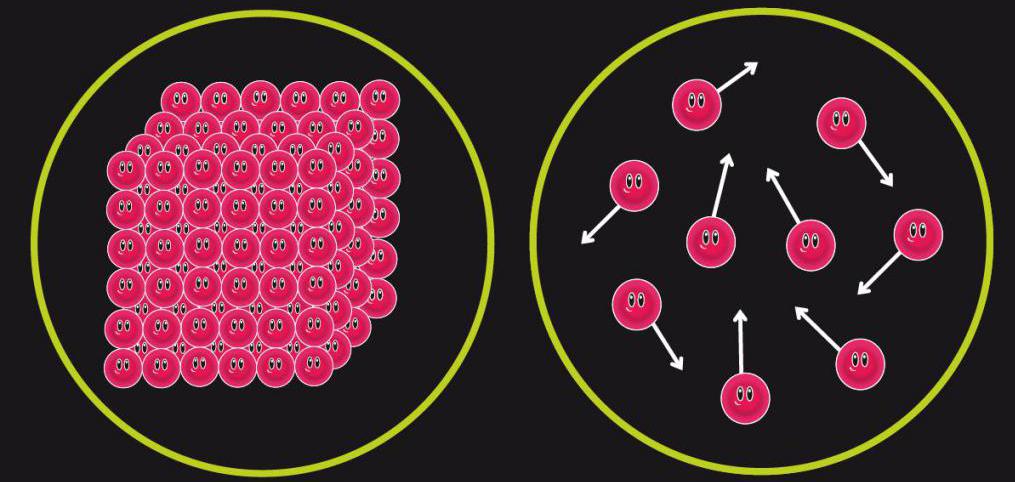
Енталпията е енергийна характеристика, а ентропията е геометрична. Отбележете, че за разбирането и описанието на протичащите термодинамични процеси абсолютните стойности на ентропията и енталпията не носят полезна информация, а са важни само величините на техните промени, а именно ΔH и ΔS.
Термодинамични твърдения
Този закон помага да се разбере в каква посока реакцията може произволно да продължи, или ще бъде в равновесие. Следните твърдения са фундаментални за термодинамиката:
- Вторият закон на термодинамиката казва, че процесът във всяка система възниква произволно, неговата ентропия трябва да се увеличи, т.е. ΔS> 0.
- При постоянна температура и налягане промяната на енергията на Гибс на системата се определя по формулата ΔG = ΔH - TΔS.
- Ако за всеки процес ΔG <0, то продължава спонтанно и се нарича ексергоничен.
- Посоката на произволния ход на дадена реакция може да зависи от температурата в системата.
Спонтанни процеси
В химията случайните процеси са тези, които се случват без външно въвеждане на енергия към тях. Произволността на перколирането показва вероятността за такава възможност и по никакъв начин не е свързана с кинетиката на процеса. Така че, той може да продължи бързо, т.е. да има експлозивен характер, но може да продължи много бавно в продължение на хиляди и милиони години.

Класически пример за спонтанно възникваща реакция е превръщането на въглерода под формата на диамант в въглеродна алотропна модификация на графита. Такава реакция е толкова бавна, че през живота си човек няма да забележи никакви промени в оригиналния диамант, така че казват, че диамантите са вечни, макар че ако изчакате достатъчно време, можете да видите как един брилянтен камък става черен, като графит.
Освобождаване и абсорбция на енергия

Друг важен аспект на произволно протичащите процеси е освобождаването или абсорбцията на топлина, в първия случай те говорят за екзотермичен процес, във втория - за ендотермичен процес, т.е. знак за промяна на енталпията ΔH. Отбележете, че както екзотермичните, така и ендотермичните процеси могат да протичат произволно.
Основен пример за случаен процес е запалването на горивната смес в цилиндъра на двигателя с вътрешно горене. При тази реакция се отделя голямо количество топлинна енергия, която се преобразува с ефективност от около 30% механична енергия принуждавайки коляновия вал да се върти. Последният предава въртящия момент чрез предаване към колелата на автомобила, а автомобилът се движи.
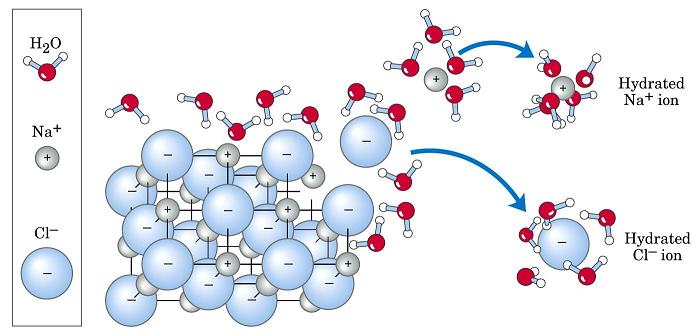
Пример за ендотермична реакция, която протича самостоятелно с абсорбцията на топлина е разтварянето на обикновен натриев хлорид във вода. В тази реакция ΔH = +3.87 kJ / mol> 0. Този факт може да бъде проверен чрез измерване на температурата на водата преди солта да се разтвори в него и след разтварянето му. Получената разлика между крайната температура и началната температура ще бъде отрицателна.
Енергийният процес на Гибс
Ако някой процес се осъществява в система с постоянно налягане и температура, тогава вторият закон на термодинамиката може да бъде пренаписан, както следва: G = H - TS. Стойността на свободната енергия на G - Gibbs има размер kJ / mol. Определянето на спонтанността на дадена реакция зависи от знака на промяната в това количество, т.е. В резултат на това вторият закон на термодинамиката приема формата: ΔG = ΔH −TΔS. Възможни са следните случаи:
- ΔG <0 - реакцията се нарича ексергонична и се случва случайно в посока напред с образуването на продукти;
- ΔG> 0 - ендергонична реакция, която не може произволно да се случи в посока напред, но независимо ще се движи в обратна посока с увеличаване на броя на реагентите;
- ΔG = 0 - системата е в равновесие и концентрациите на реагентите и продуктите остават постоянни за произволно дълго време.
Анализ на полученото уравнение
Въведеният израз за втория закон на термодинамиката ни позволява да определим в кой случай процесът може да продължи произволно. За да направите това, е необходимо да анализирате три величини: промяната на енталпията ΔH, промяната на ентропията ΔS и температурата Т. Отбележете, че температурата се изразява в абсолютни единици съгласно международната система на теглата и мерките, т.е.
Посоката на реакцията не зависи от температурата, ако:
- Реакцията е екзотермична (ΔH <0) и нейната ентропия се увеличава (ΔS> 0). В този случай процесът преминава произволно в посока напред;
- Ендотермичната реакция (ΔH> 0) и промяната в нейната ентропия са отрицателни (ΔS <0). Процесът никога няма да продължи спонтанно в посока напред.
Ако признаците на промени в стойностите на ΔH и ΔS съвпадат, то температурата вече играе важна роля в възможността за такъв процес. Така, екзотермичната реакция ще протече произволно при ниски температури и екзотермична реакция при високи температури.
Изчисляване на топенето на леда

Добър пример за реакция, при която знакът на енергията на Гибс зависи от температурата, е топенето на леда. За този процес ΔH = 6.01 kJ / mol, т.е. реакцията е ендотермична, ΔS = 22.0 J / mol * K, т.е. процесът се осъществява с увеличаване на ентропията.
За топенето на леда ние изчисляваме температурата, при която промяната в енергията на Гибс ще бъде нула, т.е. системата ще бъде в равновесно състояние. от втори закон на термодинамиката получаваме: T = ΔH / ΔS, замествайки стойностите на тези величини, изчисляваме Т = 6.01 / 0.022 = 273.18 К.
Ако преобразуваме температурата от Келвин до обичайните градуси по Целзий, получаваме 0 ° С. Тоест при температура над тази, стойността на ΔG <0 и разтопяването на леда спонтанно, при температура под 0 ° С ΔG> 0, и обратният процес ще възникне произволно, т.е. кристализацията на течната вода.