Хлор: валентност, химични свойства
Валентността определя способността на хлора да прикрепя към себе си атомите на други химически елементи.
Хлорът, чиято валентност има различни значения, се намира в седмата група, в основната подгрупа на таблицата на елементите. Нека разберем структурните особености на атома на този халоген.
Хлор в добро състояние
Валентността на хлорните атоми се определя от структурните особености на неговото външно ниво. Този елемент е в групата 7 (А), има седемнадесетия пореден номер. Като се има предвид, че елементът е представителен за четвъртия период, той има не само s-, p-, но и d-орбитали.
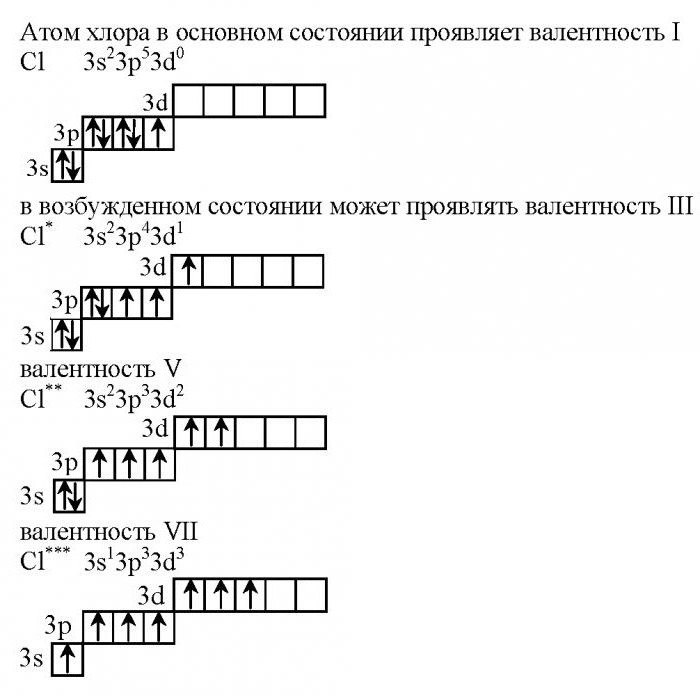
Електронна конфигурация на атома
Каква електронна формула има хлорът? Валентността е свързана с характеристиките на външното енергийно ниво следователно пишем конфигурацията на този елемент.
В невъзбудено състояние само два електрона са разположени на първото ниво на хлор, а вторият е осем, а на трето - 10. Имайте предвид, че на последното ниво има незапълнена d-орбитала, която характеризира валентните възможности на този халоген.
- 1s22s22p63s23p53d0.
В този случай валентността на хлора е равна на I. Това е типично при взаимодействие с метали (образуват се хлориди). По-високата валентност VII е хлор в съединения с неметали, например, в хлорен оксид (7), както и в перхлорна киселина.
Даваме като примери формулите на хлорните съединения, в които се проявява следната валентност: HClO 4 , Cl 2O 7 .
Последното електронно ниво в неорганичната химия се нарича валентност, тъй като именно той обяснява способността на даден елемент да влиза в химични взаимодействия с други атоми.

Възбудено състояние
Как действа хлорът при нагряване? Валентността му ще се промени, ако атомът е в възбудено състояние.
Предвид факта, че всяко енергийно ниво има определено количество енергия, електроните от първите две нива не променят първоначалната си позиция. Наблюдава се преход на един p-електрон от 3p енергийното ниво към 3d-подниво. Как това ще промени участието им в химичните реакции на хлора? Валентността му ще се промени, тя ще бъде равна на три.
Разгледайте електронната конфигурация, която хлорът придобива в този случай.
- 1s22s22p63s23p43d1.
Тази конфигурация не е стабилна, така че хлорните съединения, в които проявява степен на окисление от +3, бързо се разлагат.
Тъй като на 3-те орбитали има още четири свободни квантови клетки, е възможен последващият преход на електрона от 3p подниво, което води до образуването на друга конфигурация на хлорния атом.
- 1s22s22p63s23p33d2.
В този случай има пет несвързани електрона, така че хлорът може да показва валентност V, състояние на окисление +5.
При максимално нагряване на хлорния атом, електронът се прехвърля от 3s-подниво към 3d орбитала. В този случай, хлорът има максимална валентност от седем.
- 1s22s22p63s13p33d3.
На външно енергийно ниво има седем неспарени електрона, така че валентността на хлора в съединенията е 7.
Разпределението на електроните по нива, поднива, техният преход се извършва в съответствие с правилото на Хун и принципа на Паули.
Как е посочен хлорът в този случай? Валентността на елемента обикновено се посочва с римски цифри, а възбуденото състояние на атома се отбелязва със звездичка.
заключение
Всички разходи вътрешна енергия които преминават в процеса на възбуждане на хлорния атом, са напълно компенсирани от енергията, която се освобождава по време на образуването ковалентни връзки. Това обяснява повишената химическа активност на хлора в възбудено състояние. На максимум окислителни състояния (+7) показва свойствата на силен окислител.
Валентните възможности на атома на химичния елемент не се ограничават само от броя на несдвоените електрони в стационарна и възбудена форма. Например, при образуването на връзки в молекули чрез донорно-акцепторен механизъм се приема и използването на свободни орбитали.
Какви фактори влияят на валентния капацитет на хлорния атом? Обобщавайки, нека да кажем, че на първо място е необходимо да се отбележи броят на неспарените електрони (празни орбитали). В допълнение, атомът трябва да има свободна орбитала, към която електрони ще се прехвърлят при нагряване.