Въглеродни оксиди: химия, степен 8
Всичко, което ни заобикаля, се състои от съединения от различни химически елементи. Ние дишаме не само въздух, но и сложно органично съединение, което съдържа кислород, азот, водород, въглероден диоксид и други необходими компоненти. Влиянието на много от тези елементи върху човешкото тяло в частност и върху живота на Земята като цяло все още не е напълно проучено. За да се разберат процесите на взаимодействие на елементи, газове, соли и други образувания един с друг, в учебния курс е въведен предмет “Химия”. Клас 8 е началото на уроците по химия в съответствие с одобрената обща образователна програма.
Едно от най-често срещаните съединения в земната кора и в атмосферата е оксид. Оксидът е съединението на всеки химичен елемент с кислороден атом. Дори източникът на цял живот на Земята - вода, е водороден оксид. Но в тази статия ние не говорим за оксиди като цяло, а за един от най-често срещаните съединения - въглероден оксид. Тези съединения се получават чрез сливане на кислородни атоми и въглерод. Тези съединения могат да съдържат различни количества въглеродни атоми и кислород, но трябва да се разграничат два основни съединения на въглерода с кислород: въглероден оксид и въглероден диоксид.
Ad
Химична формула и метод за получаване на въглероден монооксид
Каква е нейната формула? Въглеродният оксид е доста лесен за запомняне - СО. Молекулата на въглеродния монооксид се образува от тройна връзка и следователно има сравнително висока сила на свързване и има много малко междуядрено разстояние (0.1128 nm). Енергията на разкъсване на това химично съединение е 1076 kJ / mol. Тройната връзка възниква поради факта, че въглеродният елемент има в атомната си структура р-орбитала, която не е заета от електрони. Това обстоятелство създава възможност въглеродният атом да стане акцептор на електронната двойка. А кислородният атом, напротив, има неразделена двойка електрони на един от р-орбиталите и затова има електрон-донорски способности. Когато тези два атома се комбинират, в допълнение към две ковалентни връзки, се появява трета - донорно-акцепторна ковалентна връзка. 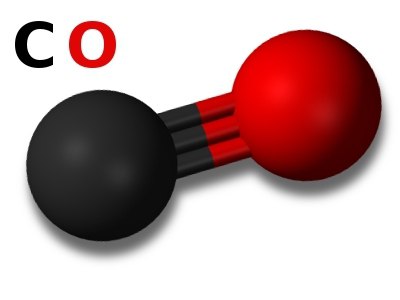
Има различни начини за получаване на СО. Един от най-простите е предаването на въглероден диоксид върху горещите въглища. В лабораторни условия се произвежда въглероден оксид, като се използва следната реакция: мравчена киселина се загрява със сярна киселина, която отделя мравчена киселина във вода и въглероден оксид.
Ad
CO се освобождава и при нагряване на оксалова киселина и сярна киселина.
Физически свойства на СО
Въглеродният оксид (2) има следните физични свойства - това е безцветен газ, който няма изразен мирис. Всички нежелани миризми, които се появяват по време на изтичане на въглероден окис, са продукти от разлагане на органични примеси. Той е много по-лек от въздуха, изключително токсичен, много слабо разтворим във вода и се характеризира с висока степен на запалимост.
Най-важното свойство на СО е неговото отрицателно въздействие върху човешкото тяло. Отравяне с въглероден окис може да бъде фатално. По-подробно за ефектите на въглеродния оксид върху човешкото тяло ще бъде описано по-долу.
Химични свойства на СО
Основните химични реакции, при които могат да се използват въглеродни оксиди (2), са окислително-редукционната реакция, както и реакцията на добавяне. Редокси реакцията се изразява в способността на СО да редуцира метала от оксидите чрез смесването им с допълнително нагряване.
Ad
При взаимодействие с кислород, образуването на въглероден диоксид настъпва с отделянето на значително количество топлина. Въглероден оксид изгаря с синкав пламък. Много важна функция на въглеродния оксид е неговото взаимодействие с метали. В резултат на такива реакции се образуват карбонили на метали, повечето от които са кристални вещества. Те се използват за производството на свръхчисти метали, както и за нанасяне на метални покрития. Между другото, карбонилите имат добра репутация като катализатори за химични реакции.
Химична формула и метод за получаване на въглероден диоксид
Въглеродният диоксид или въглеродният диоксид имат химичната формула СО2. Структурата на молекулата е малко по-различна от структурата на СО. При това образуване въглеродът има окислително състояние +4. Структурата на молекулата е линейна и следователно неполярна. Молекулата на СО 2 не притежава такава силна сила като СО. Земната атмосфера съдържа около 0,03% въглероден диоксид от общия обем. Увеличаването на този показател унищожава озоновия слой на Земята. В науката това явление се нарича парников ефект.
Ad
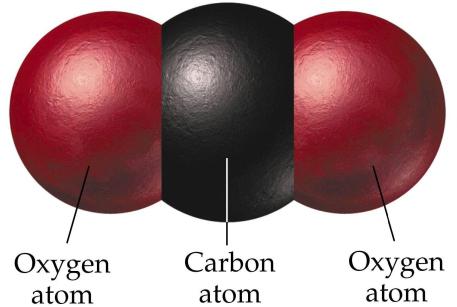
Въглеродният диоксид може да бъде получен по различни начини. В промишлеността се образува в резултат на изгарянето на димните газове. Той може да бъде страничен продукт в процеса на приготвяне на алкохол. Той може да се получи в процеса на разлагане на въздуха в основните компоненти, като азот, кислород, аргон и други. В лабораторни условия може да се получи въглероден оксид (4) в процеса на изгаряне на варовик, а у дома въглероден диоксид може да се екстрахира с помощта на лимонена киселина и сода. Между другото именно по този начин в началото на производството им се правят газирани напитки.
CO 2 Физически свойства
 Въглеродният диоксид е безцветно газообразно вещество без характерна силна миризма. Благодарение на високата степен на окисление, този газ има слабо кисел вкус. Този продукт не поддържа процеса на горене, тъй като той е резултат от изгаряне. При повишена концентрация на въглероден диоксид човек губи способността си да диша, което е фатално. Повече подробности за ефектите на въглеродния диоксид върху човешкото тяло ще бъдат описани по-долу. CO 2 е много по-тежък от въздуха и е напълно разтворим във вода, дори и при стайна температура.
Въглеродният диоксид е безцветно газообразно вещество без характерна силна миризма. Благодарение на високата степен на окисление, този газ има слабо кисел вкус. Този продукт не поддържа процеса на горене, тъй като той е резултат от изгаряне. При повишена концентрация на въглероден диоксид човек губи способността си да диша, което е фатално. Повече подробности за ефектите на въглеродния диоксид върху човешкото тяло ще бъдат описани по-долу. CO 2 е много по-тежък от въздуха и е напълно разтворим във вода, дори и при стайна температура.
Един от най-интересните свойства на въглеродния диоксид е, че той няма течно състояние на агрегация при нормално атмосферно налягане. Въпреки това, ако въздействието върху структурата на излагане на въглероден диоксид на температура от -56.6 ° C и налягане от около 519 kPa, след това тя се превръща в безцветна течност.
Ad
При значително понижаване на температурата газът е в състояние на така наречения „сух лед“ и се изпарява при температура по-висока от -78 ° С.
Химични свойства на CO 2
Характерни са химичните свойства на въглеродния оксид (4), чиято формула е СО2 киселинен оксид и притежава всички свои свойства.
1. При взаимодействие с вода се образува въглена киселина, която има слаба киселинност и ниска стабилност в разтворите.
2. При взаимодействие с алкали въглеродният диоксид образува съответната сол и вода.
3. По време на взаимодействието с оксидите на активния метал насърчава образуването на соли.
4. Не поддържа горенето. Само някои активни метали, като литий, калий, натрий, могат да активират този процес.
Влияние на въглеродния оксид върху човешкото тяло
 Нека се върнем към основния проблем на всички газове - въздействието върху човешкото тяло. Въглеродният оксид принадлежи към групата на изключително опасните газове. За хората и животните това е изключително силно отровно вещество, което, ако се погълне, сериозно засяга кръвта, нервната система на тялото и мускулите (включително сърцето).
Нека се върнем към основния проблем на всички газове - въздействието върху човешкото тяло. Въглеродният оксид принадлежи към групата на изключително опасните газове. За хората и животните това е изключително силно отровно вещество, което, ако се погълне, сериозно засяга кръвта, нервната система на тялото и мускулите (включително сърцето).
Въглеродният моноксид във въздуха не може да бъде разпознат, тъй като този газ няма обособен мирис. Той е опасен. Веднъж попаднал в човешкото тяло през белите дробове, въглеродният оксид активира разрушителната си активност в кръвта и започва да взаимодейства с хемоглобина стотици пъти по-бързо от кислорода. В резултат на това се появява много резистентно съединение, наречено карбоксигемоглобин. Той пречи на доставянето на кислород от белите дробове към мускулите, което води до мускулен глад на тъканите. Особено сериозно засегнати от този мозък.
Поради невъзможността да се разпознае отравянето с въглероден окис чрез обонянието, трябва да знаете някои от основните симптоми, които се появяват в ранните етапи:
- замаяност, придружена от главоболие;
- шум в ушите и трептене пред очите;
- сърцебиене и задух;
- зачервяване на лицето.
В бъдеще жертвата на отравяне се явява силна слабост, понякога повръщане. При тежки случаи на отравяне са възможни принудителни припадъци, придружени от по-нататъшна загуба на съзнание и кома. Ако пациентът не получи подходящо медицинско обслужване своевременно, смъртта е възможна.
Влияние на въглеродния диоксид върху човешкото тяло
Въглеродните оксиди с киселинност +4 принадлежат към участъка на задушливите газове. С други думи, въглеродният диоксид не е токсично вещество, но може значително да повлияе на потока на кислород към тялото. Когато нивото на въглероден двуокис се повиши до 3-4%, човек става сериозно слаб и започва да спи. Когато нивото се повиши до 10%, започват да се развиват силни главоболия, замаяност, слухови увреждания и понякога се наблюдава загуба на съзнание. Ако концентрацията на въглероден диоксид се повиши до ниво от 20%, тогава настъпва смърт от кислородно гладуване.
Лечението на отравяне с въглероден диоксид е много просто - да се даде на жертвата достъп до чист въздух, ако е необходимо, да се направи изкуствено дишане. В изключителни случаи трябва да свържете жертвата с вентилатор.
От описанията на влиянието на тези два въглеродни оксида върху тялото можем да заключим, че въглеродният оксид, с високата си токсичност и насоченото въздействие върху тялото отвътре, все още представлява голяма опасност за хората.
Въглеродният диоксид не се различава по такъв вид предателство и е по-малко вреден за хората, поради което именно тази субстанция използва активно дори и в хранителната промишленост.
Използването на въглеродни оксиди в промишлеността и тяхното въздействие върху различни аспекти на живота
Въглеродните оксиди се използват много широко в различни области. човешка дейност и обхватът им е изключително богат. По този начин въглеродният оксид се използва с най-голяма сила в металургията в процеса на топене на желязо. CO придоби широка популярност като материал за съхранение на храна в охладено състояние. Този оксид се използва за обработка на месо и риба, за да им придаде свеж вид и да не променят вкуса. Важно е да не се забравя токсичността на този газ и да се помни, че допустимата доза не трябва да надвишава 200 мг на 1 кг продукт. CO наскоро все повече се използва в автомобилната индустрия като гориво за автомобили на газ. 
Въглеродният диоксид е нетоксичен, така че неговият обхват на приложение е широко въведен в хранителната промишленост, където се използва като консервант или бакпулвер. CO 2 се използва и при производството на минерална и газирана вода. В твърдо състояние („сух лед“) често се използва в замразителни инсталации за поддържане на стабилна ниска температура в помещение или уред.
Много популярни са пожарогасителите с въглероден диоксид, чиято пяна напълно изолира огъня от кислород и не позволява на огъня да избухне. Съответно, друго приложение е пожарната безопасност. Бутилките в пневматичните пистолети също са заредени с въглероден диоксид. И разбира се, почти всеки от нас чете от какво се състои освежителят за въздух за стаите. Да, един от компонентите е въглероден диоксид.
Както виждаме, поради минималната си токсичност въглеродният диоксид е все по-често срещан в ежедневието на човека, докато въглеродният оксид е намерил приложение в тежката индустрия.
Има и други въглеродни съединения с кислород, ползата от формулата на въглерода и кислорода позволява използването на различни варианти на съединения с различен брой въглеродни атоми и кислород. Редица оксиди могат да варират от C2O2 до C32O8 . И за да опишете всеки един от тях, ще ви трябва повече от една страница.
Въглеродни оксиди в природата
И двата вида въглеродни оксиди, разглеждани тук, някак си присъстват в естествения свят. Така че въглеродният оксид може да бъде продукт на изгарянето на гори или в резултат на човешка дейност (отработени газове и опасни отпадъци от промишлени предприятия).
Вече известният ни въглероден диоксид също е част от сложния състав на въздуха. Съдържанието му в него е около 0,03% от общия брой. С увеличаването на този показател възниква т.нар. „Парников ефект”, от който се страхуват съвременните учени.  Въглеродният диоксид се отделя от животни и хора чрез издишване. Той е основният източник на такъв полезен елемент за растенията като въглерод, поради което много учени бързат към мястото, което показва недопустимостта на мащабния дърводобив. Ако растенията престанат да абсорбират въглероден диоксид, процентът на съдържанието му във въздуха може да се повиши до критичен за индикаторите за човешка дейност.
Въглеродният диоксид се отделя от животни и хора чрез издишване. Той е основният източник на такъв полезен елемент за растенията като въглерод, поради което много учени бързат към мястото, което показва недопустимостта на мащабния дърводобив. Ако растенията престанат да абсорбират въглероден диоксид, процентът на съдържанието му във въздуха може да се повиши до критичен за индикаторите за човешка дейност.
Очевидно много власти са забравили материала на учебника “Обща химия. Клас 8, в противен случай въпросът за обезлесяването в много части на света ще получи по-сериозно внимание. Това, между другото, се отнася и до проблема с наличието на въглероден оксид в околната среда. Количеството на човешките отпадъци и процентът на емисиите на този изключително токсичен материал в околната среда се увеличава с всеки изминал ден. И не е факт, че съдбата на света, описана в красивия анимационен филм "Уоли", когато човечеството трябваше да остави Земята затънала до основата си и да отиде в други светове в търсене на по-добър живот, няма да се повтори отново.