Основни закони на химията. Основни понятия и закони на химията
Няма да е излишно първо да дефинираме понятието “ химия ” - това е най-важната наука, която изследва структурата на веществата, техните трансформации. Тя включва следните основни понятия и закони (химия):
1. Химичните свойства на всяко вещество се установяват въз основа на състоянието на електронните черупки на (външните) молекули, които я образуват. Ядрата и вътрешните електрони остават почти непроменени по време на химичните процеси.
2. Предмет на химията - химични елементи, техните комбинации (атоми, прости, комплексни: йони, карбени, свободни радикали, молекули, радикални йони, както и материали, химични съединения, техните асоциации: клъстери, клатрати, асоциати, солвати и др. ). Има огромен брой от тях и непрекъснато нараства поради факта, че тази наука сама по себе си формира своя обект (около 10 милиона химически съединения вече са известни).
3. Вещество е вид материя с определена маса на почивка и се състои от такива елементарни частици като електрони, неутрони, протони, мезони и др. Тази наука изследва такива вещества, които се превръщат в атоми, йони, молекули и радикали. Те са: сложни, прости (химични съединения).
4. Най-малкият компонент на химически елемент, който не може да бъде разделен химически и който запазва всички първоначални свойства, определени от електрическата обвивка и ядреният заряд се нарича атом . Частта от вещество (съединение), съдържаща идентични атоми, се нарича химичен елемент , всеки от които съответства на комплекс от определени атоми.
5. Молекула е микрочастица, която има 2 или повече атома и е способна на автономно съществуване. Той има постоянен количествен, качествен състав на атомните ядра, както и постоянно число на електроните; оборудвани с уникални свойства. 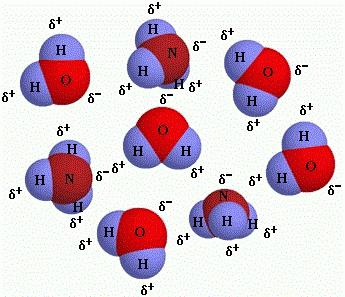
6. Обикновените вещества се образуват от атоми само от първия химичен елемент, с оглед на което те са специална форма на неговото съществуване в свободно състояние (O₂, H₂, He, O₃, S₈), а сложните вещества се образуват от различни химически елементи и могат да имат постоянен състав ( далтониди или стехиометрични съединения) или променливи (бертолиди или нестехиометрични съединения).
7. Йони са моноатомични или многоатомни частици с електрически заряд. Положително заредените йони са катиони, а отрицателно са аниони. Под формата на газ те са в свободното си състояние.
8. Валентността е способността на атома да замени или прикрепи други атоми (атомни групи) и да образува химически връзки. Валентната мярка е броят на водородните атоми (кислород), които са прикрепени към химически елемент. Водородът е моновалентен и кислородът е двувалентен.
9. Химичните реакции са превръщането на някои вещества (първоначални съединения) в вещества от различен вид (реакционни продукти), които не променят ядрата на атомите.
10. Реагенти - изходни материали или едно от най-активните изходни вещества, което определя посоката на реакцията. 
Произход на въпросното понятие
Има две гледни точки по отношение на неговия произход:
- От древното име на Египет - "Хем", което буквално се превежда като "черно", "тъмно". Вероятно поради цвета на почвата на долината на р. Нийл.
- От древния гръцки термин "chemeia" - форма на изкуство на топене на метал.
Съвременното име идва от латинската дума "chimia". Той е международен (например в немски chemie, във френски chimie, по английски химия). Известно е, че предшественикът на термина "химия" е гръцкият алхимик Зосима (V век).
Органична химия: определение, органични съединения
Това е науката, която изучава въглеродни съединения, които се произвеждат от живите организми. Към днешна дата са известни повече от 2 милиона органични съединения, разделени на групи като алкени, алкохоли, алкани и др. Повечето от тях са включени в състава на петрола и заемат водещи позиции в производството на: багрила, лекарства, пластмаси, козметика ,
Съставът на органичните съединения: въглеродни атоми и други елементи (кислород, водород), които са свързани със силни ковалентни връзки. Тези съединения, които се образуват от въглеродни атоми с водород, се наричат въглеводороди .
Основният компонент на природния газ е прост въглеводород (метан - CH₄). Органичната химия изследва точно органични съединения диференцирани по семейства и които се наричат хомоложни серии .
Горните групи (алкени, алкани) принадлежат към различни хомоложни серии, всяка от които включва хиляди съединения. Тяхното местоположение в тази серия се определя от броя на въглеродните атоми вътре в молекулите (например, молекулите на първите три съединения на редица алкани: метан - 1 въглероден атом, етан - 2, пропан - 3).
Имената на съединенията, които съдържат 1 въглероден атом, започват с префикса "мет", 2 атома - "ет", 3 атома - "опора". Такива съединения, принадлежащи към първата хомоложна серия, имат сходни химически свойства, но различни физични. А онези съединения, които имат малко въглеродни атоми, са газове, достатъчно голям брой атоми са течности, а твърдите вещества са пренаситени с атоми.
Броят на органичните съединения е доста голям поради способността на атомите да образуват дълги вериги или пръстени. Тези структурни единици са залепени заедно поради ковалентните връзки (техните електрони на външните черупки са "общодостъпни"). Въглеродните форми са прости (всяка атомна двойка разделя между тях 1 чифт електрони), 2-ра или 3-та ковалентна връзка (две и, съответно, три двойки електрони).
При реакция на достатъчно наситено съединение (органично) с друго съединение, съществуващите връзки се разрушават и някои атоми се заменят с други.
Основни стехиометрични закони на химията
Те са включени в този раздел на химията, като стехиометрия. Известно е, че то съдържа следните основни закони на химията:
- Gay Lussac-;
- Авогадро;
- еквиваленти и масово съхранение;
- множество връзки;
- консистенция на състава.
Същността на закона за опазване на масата и енергията
В основата на образуването на химически уравнения стои методът на материалния баланс, основата на който е законът за запазване на масата (химията). Според него, масата на реактивите е идентична с масата на крайните продукти на реакцията.
За първи път е открит от М. В. Ломоносов през 1748 година. Тогава френският химик А. Лавуазие (1789) стига до същите резултати.
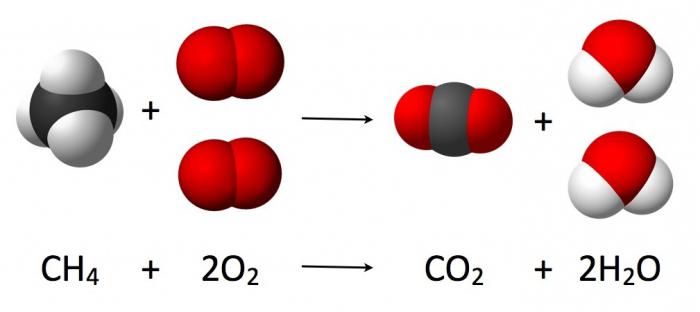
В хода на химическа реакция броят на взаимодействащите атоми е неизменна (наблюдава се само тяхното прегрупиране, съпроводено с унищожаване на изходните вещества). Текущото взаимодействие на кислород с водород, което води до образуването на вода, може да бъде записано чрез уравнението на съответната химическа реакция (както е показано на фигурата по-долу). 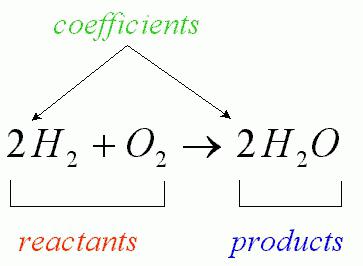
Формулите на тези химични съединения са коефициенти, които се наричат "стехиометрични". Модерната формула се дешифрира по следния начин: сумата от маси и енергии в една изолирана система е постоянна.
Той има формата: E = m · c², където
c е скоростта на светлината (3.10 m / s);
В началото на 20-ти век Алберт Айнщайн успява да докаже валидността на това уравнение за всяка форма на материята.
Същността на закона на постоянството
Той е формулиран от френските химици J. Proust и C. L. Berthollet през 1808 г. Той посочва, че всяко отделно вещество, получено по всеки известен метод, винаги има постоянен количествен и качествен състав.
Законът за постоянството на материята (химията) дава възможност да се изрази съставът на веществата по химични признаци, съответните индекси (например, H20, C2H2OH, CH3). В началото на 20-ти век (1912–1913) видният руски професор Н. С. Курнаков разкрива съществуването на съединения с променлив състав, които той нарича бертолиди .
Ако си припомните следващия урок по химия, законът за постоянството на състава се счита за справедлив за вещества, които имат молекулярна структура. Както вече бе споменато по-рано, освен вещества с постоянен състав, съществуват и вещества с променливи: редуването на монолитни структурни единици (йони, атоми) протича в нарушение на установената периодичност.
Поради наличието на съединения с различен състав, законът на постоянството на състава (химия) съдържа разяснения относно факта, че съществува пряка връзка между структурата на състава на съединенията и методите за тяхното получаване: ако има молекулна структура, тогава съставът не се променя в зависимост от който и да е метод на получаване, но в ситуация, когато структурата е немолекулна (йонна, атомна и метална решетка) - съставът зависи от специфичните условия на производство. 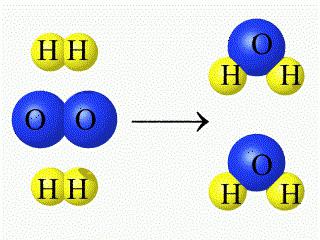
Закон за еквивалентни формулировки
Той е открит от германския химик Н. Рихтер и се състои от следното: масите на вещества, които взаимодействат (химически) са равни или са кратни на масите на техните химически еквиваленти (химия клас 11).
Еквивалентът е условна или действителна частица от вещества, способни да заменят, освобождават, прикрепват и т.н., което е равно на първия водороден йон от йонообменни или киселинно-базични реакции; Реконтозни реакции на 1-ия електрон.
По различен начин може да се каже, че мол еквиваленти (определено количество вещество, съдържащо толкова структурни елементи, колкото са въглеродните атоми в 12 g от изотопа ¹2С) на първото вещество, реагира с точно същия мол еквиваленти, но от различно вещество ,
Математически този закон е:
mₐ: Mₔ (A) = mᵦ: Mₔ (B), където
mₐ е масата на някое вещество А,
mᵦ е масата на вещество В,
Mₔ (A) е масата (моларен) еквивалент на съответното вещество А,
Mₔ (B) - маса (моларен) еквивалент на веществото Б.
Случва се, че едно реагиращо вещество първоначално се намира в твърдо състояние, а другото в газообразно състояние. Тогава разглежданият закон се изразява със следната формула:
mₐ: Mₔ (A) = Vb: V (B).
Същността на закона за множествените отношения
Той е формулиран от английския химик Д. Далтън през 1803 г. Неговата същност е, че в ситуация, при която 2 химични елемента създават няколко съединения (молекулярни), масовите фракции на всеки от тях са свързани като цели числа (химия клас 11).
В процеса на взаимодействие на кислород и азот се получават 5 оксида. В появяващите се молекули на 1 g азот се получава следното количество кислород в грамове: 0.57, 1.14, 1.71, 2.28, 2.85. Те корелират в пропорции: 2: 1, 1: 1, 2: 3, 1: 2, 2: 5 (състави: NO, NO, N20, NO2, N20).
Законите на Авогадро и отношенията между тях
Същността на последното: при еднакви условия обемите на газовите реагенти се отнасят един към друг и обемите на получените газови продукти като цели числа (J. Gay-Lussac).
В случай на взаимодействие на газообразни вещества, техните обеми са свързани като коефициенти (стехиометрични) уравнения на реакцията: 2H₂ + O₂ = 2H2O (g).
Що се отнася до Законът на Авогадро, след това неговата формулировка е както следва: идентични обеми газ в същите условия съдържат същия брой молове.
Математически, тя може да бъде представена, както следва:
n (x) = m: M (x), където
n (x) е необходимия брой молове на дадено вещество,
m е масата на съответното вещество
М (х) е моларната маса на реагента.
Последици от този закон:
- 1 моларно газообразно вещество замества обем от 22.4 литра (при нормални условия).
- 1 mol газообразно вещество съдържа идентичен брой молекули, което е равно на 6.023 1023 - брой на Авогадро.
- При известни маси газообразни вещества или техните моларни маси е възможно да се определи относителната плътност: mₐ: mᵦ = pₐ: pᵦ, където
pₐ, pᵦ - плътност на веществата А и B, g / cm ³.
И така, основните закони на химията (стехиометрични) са изброени по-горе. След това ще се разглежда газ и термодинамика.
Газови закони на химията
Само четири закона:
1. Boyle - Mariotta: ако температурата е постоянна стойност (T = const) в рамките на изотермичния процес, тогава произведеното от масата на газа налягане е обратно пропорционално на неговия обем: pV = const.
2. Gay-Lussac: ако налягането на газа е постоянно (p = const) вътре изобарен процес тогава обемът му е правопропорционален на абсолютната температура: V: T = const. 
3. Чарли: ако обемът на газа е постоянна стойност в рамките на изохоричния процес, тогава неговото налягане е пряко пропорционално на абсолютната температура: P: T = const.
4. Комбиниран газ: pV: T = const.
Това са основните закони на газовата химия.
Законите на химическата термодинамика
Има три от тях:
1. Закон за запазване на енергията (химия): ако в хода на който и да е процес енергията на първия вид изчезне, тогава "идва" различна форма на енергия, за да я замени и в различно количество, което е строго еквивалентно на първото. Следователно може да се каже, че в рамките на всяка изолирана система общата енергийна резерв остава непроменена.
2. В границите на една изолирана система процесите, които възникват спонтанно, увеличават ентропията (трансформацията) на системата.
3. Ако температурата се стреми към нула, тогава ентропията на системата остава непроменена (независимо от нейните параметри).
Това са основните закони на термодинамиката (химията).
Същността на закона на масите
Това е основният закон на физическата химия. Законът за действие на масите (в химията): скоростта, с която протича химична реакция, е пропорционална на произведението от концентрациите на реактивите.
В случай на хомогенна реакция с първия етап (А + В - реакционни продукти), този закон може да бъде представен като уравнение:
v = k · cₐ · cᵦ, където
v е скоростта на реакцията
cₐ, cᵦ - концентрации на реактиви, съответно А и В, mol / l,
k е константата на скоростта на реакцията.
Законът за действие на масите (в химията) дава възможност да се идентифицира физическия смисъл на тази константа: тя е равна на скоростта на реакцията при концентрациите на реагентите при 1 mol / l или стойността на техния продукт е равна на единица. Константата зависи от температурата, естеството на реагентите, но не и от тяхната концентрация.
Периодичен закон: формулировка, роля
Признава се, че този закон е най-важното постижение в химията, може да се каже, основата на съвременната химия. След откриването му, тя престана да бъде изключително описателна наука, така стана възможно така нареченото научно предвиждане.
Периодичният закон (химия) е открит от известния руски учен Дмитрий Иванович Менделеев през 1869 година. Официалната формулировка: “Свойствата на простите тела, както и формите и свойствата на съединенията на елементите са в периодична зависимост от размера на атомните тегла на елементите”.
Това са основните закони на химията (физически).
Химия като система от знания за веществата и техните трансформации
Знанието се извлича от надеждна обширна информация за съединенията и елементите (химическите), техните реакции, поведението в рамките на естествената и изкуствената среда. Съществуващите критерии за надеждност на изследваните факти, както и начините за тяхното организиране непрекъснато се развиват. Основните обобщения се прехвърлят към научните закони, формулирането на които позволява да се отворят нови етапи на химията (например, основните закони на химията: закон на Далтон, периодичния закон на Менделеев и др.). Теоретичните аспекти, в които се прилагат специфични понятия, дават възможност да се обяснят и прогнозират фактите на по-тясна предметна област. Следователно, може да се каже, че знанието, подкрепено от опита, става факт само след неговата теоретична интерпретация.
Така първата химическа теория е теорията за „флогистон” (призната за неправилна), тя насърчава формирането на съвременната химия, предвид факта, че тя съчетава разпръснатите факти в единна система, позволявайки му да формулира редица нови въпроси. Но структурната теория (F. Kekule, A. M. Butlerov) помогна да се рационализира и обясни обширния материал на органичната химия и да се определи ускореното развитие на химичния синтез, както и изучаването на структурата на органичните съединения.
Въпросната наука като знание е много динамична система. Еволюционният характер на процеса на натрупване на знания периодично се прекъсва от революции - радикално преструктуриране на системата от теории, методи и факти с появата на нов набор от понятия или дори фундаментално нов стил на мироглед и мислене. Така произведенията на Антоан Лоран Лавуазие (въвеждането на количествени методи на експеримента, материалистичната теория на окислението, развитието на химическата номенклатура), периодичният закон на Менделеев, разработването на нови аналитични методи (хроматография, микроанализ), появата на нови области, които формират новия предмет на химията и засягат всички нейни области (например физическа химия, базирана на химическа кинетика и термодинамика).
Също така трябва да се отбележи, че химическото познание е снабдено с развита структура, чиято химическа рамка е основната химична дисциплина, формирана през 19 век (органична, аналитична, неорганична и физична химия). Впоследствие в процеса на нейната еволюция се появиха много нови дисциплини (био- и кристална химия и др.) И инженерната индустрия - химическа технология.
Статията разглежда основните понятия и закони на химията.