Алуминиев сулфат и други алуминиеви съединения в природата и човешкия живот
Във всекидневния живот всеки от нас постоянно се сблъсква с невероятно количество химикали, както естествени, така и създадени от човека. Нека се спрем на две химични съединения: алуминиев сулфат, алуминиев хидроксид. Какво е това и защо трябва да обръщате внимание на тях?
За да се срещнете, трябва да заземите
Алуминиевият сулфат (двуалуминиев триоксид), заедно с алумосиликати и различни видове глина, съставлява основната част от земната кора. Това позволява на алуминия да заеме първо място сред металите по отношение на разпространението на Земята. В природата алуминиевият сулфат, формулата на която Al2 (SO4) * 18H20 е кристален хидрат и е бял разтворим водоразтворим кристал със сив, син или розов оттенък.

За разлика от алуминиевия сулфат, неговият хидроксид е бяло твърдо вещество, неразтворимо във вода. Широко се разпространяват алуминиев сулфат, алуминиев хидроксид, каолинит. Те се добиват в Сибир, Крим, Китай, Япония, както и в страните от Централна и Южна Америка.
Зри в епруветка
За да знаем истината, ние ще определим какви химически свойства имат сулфатът и хидроксидът А1. Нека преформулираме уловката на Кома Прутков „Погледни към корена!” В по-прагматичен: „Погледни в епруветката!”
 Нека започнем с Ал хидроксид, представяйки това вещество в образа Джанус с две лица. Много малко химични съединения могат да реагират едновременно с киселини и основи. Такава „двойственост“ в химията се нарича амфотерна. Така в реакциите на алуминиевия хидроксид с киселина се получават средни соли.
Нека започнем с Ал хидроксид, представяйки това вещество в образа Джанус с две лица. Много малко химични съединения могат да реагират едновременно с киселини и основи. Такава „двойственост“ в химията се нарича амфотерна. Така в реакциите на алуминиевия хидроксид с киселина се получават средни соли.

Като се има предвид взаимодействието на алуминиев хидроксид Al (OH) 3 с алкали, ние ще бъдем внимателни и ще вземем предвид условията, при които протича реакцията. Крайните продукти ще зависят от тях:

Самият Al (OH) 3 хидроксид се получава в лабораторията по непряк начин, т.е. не от оксид и вода, което в този случай е невъзможно, а от алуминиева сол. За да направите това, вземете разтвор на алуминиев сулфат и действайте върху него с алкали, като сода каустик, внимателно го изливайте на капки.
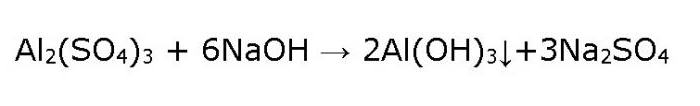
В резултат се образува бяла желатинова утайка, А1 (ОН) 3 в епруветката.

Обобщавайки всички горепосочени реакции, доказвайки амфотерния алуминиев хидроксид, можем да заключим: в кисела среда химическо равновесие се премества към образуването на Al соли, а в алкална - към образуването на металуминати или хидроксиалуминати.
Подкрепяща традиция
Нека да се откъснем от трудностите на „двойствеността“ на амфотерния алуминиев хидроксид и да се обърнем към традиционната средна сол - алуминиев сулфат. Няма отклонения от правилата. Разтвори на средни соли реагират с алкали, с киселини, с други соли, с метали, стоящи в серията Бекетов (серия от метални напрежения) към метал, чийто йон се съдържа в молекулата на солта. Например, алуминиевият сулфат в разтвор ще реагира с литий, калий, калций, натрий и магнезий. Потвърдете това с уравненията на реакцията.
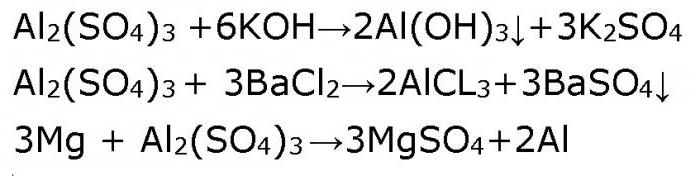
Алуминиевият сулфат, чиято формула е Al2 (SO4) 3, е продукт на взаимодействието на слаба алуминиева хидроксидна основа на Al (OH) 3 и силна сулфатна киселина H2SO4. Следователно, той лесно хидролизира във воден разтвор. Открива се излишък от водородни йони Н + , използвайки лакмусов индикатор, който променя синия му цвят в разтвор на алуминиев сулфат до червено. Така се установява, че разтворът на алуминиевия сулфат е кисел.

Възможно е да продължим да се вникваме в детайлите на тази тема, които бяха приятни и вълнуващи за химик-естет, ако подозрително скептично настроени с въпроса: „И така, какво ще имам?“
Те ще дойдат на помощ
За да разсеем всички съмнения, нека кажем, че вече имате много полезни и дори жизненоважни неща, благодарение на такива съединения като алуминиев сулфат, алуминиев хидроксид и други алуминиеви реагенти. На първо място, Al (OH) 3 се използва за почистване на твърда вода. След този процес водата става по-прозрачна и по-лека и се освобождава от солите, които я правят трудно.
Лосиони, гелове, тоници ни помагат да бъдем винаги красиви и добре поддържани. Но те също така съдържат алуминиев сулфат. Широко рекламираната иновация в дезодорантната антиперспирантна индустрия, наречена „кристали за свежест“, не е нищо повече от алуминиево-калиеви стипца, от която алуминиев сулфат е компонент. Алуминиевите съединения притежават способност за обгръщане и поради това се използват и при производството на многоцветни памучни тъкани и във фармакологията.