Какво представляват халогените в химията?
Нека поговорим за халогените. Те са в седмата група (основна подгрупа) на периодичната таблица. Преведено от гръцки, "халоген" означава "раждане на сол". Статията ще говори за това какво представлява химически халоген, кои вещества са комбинирани в този термин, какви са техните свойства и особености на производството.

Специални функции
Обмисляйки какви са халогените, отбелязваме спецификата на структурата на техните атоми. Всички елементи на външното енергийно ниво имат седем електрона, а един от тях е несдвоен (свободен). Следователно, окислителните свойства на халогените се изразяват, т.е. добавянето на един електрон при взаимодействие с различни вещества, което води до пълното завършване на външното енергийно ниво, образуването на стабилни конфигурации на халиди. При металите те образуват твърдо вещество йонна връзка характер.

Представители на халогени
Те включват следните елементи: флуор, хлор, бром, йод. Astatis и tennesin имат формална връзка с тях. За да се разбере какво представляват халогените, трябва да се отбележи, че хлорът, бромът и йодът имат свободна орбитала. Тя обяснява различните окислителни състояния за тези елементи. Например, хлорът има следните стойности: -1, + 1, + 3, +5, +7. Когато на хлорния атом е дадена допълнителна енергия, има постепенно преминаване на електроните, което обяснява промените в степените на окисление. Сред най-стабилните конфигурации на хлора са неговите съединения, в които степента на окисление е -1, както и +7.

Да бъдеш в природата
Характеристиките на структурата обясняват тяхното разпространение в природата. Халогенните съединения в природата са представени като халиди, силно разтворими във вода. С увеличаване на халогенния атомния радиус, тяхното количествено съдържание в земната кора намалява. Например, някои съединения на бром, хлор, флуор се използват в промишлени обеми.
Калциев флуорид (флуорит) може да бъде споменат като основно флуорно съединение, присъстващо в природата.
Характеристики на получаването
За да се разбере какво са халогени, е необходимо да се разбере как да ги получим. Основният вариант за изолиране на чисти халогени от соли е електролизата на стопените соли. Например, когато са изложени на натриев хлорид пряк електрически ток, тъй като реакционните продукти могат да се считат не само за газообразен хлор, но и за метален натрий. Металът се редуцира при катода, а на анода се образува халоген. За получаване на бром с морска вода, провеждане на електролиза на този разтвор.
Физични свойства
Нека се спрем на физическите свойства на представителите на седмата група от основната подгрупа. Флуорът при нормални условия е газообразно вещество, което има светложълт цвят, остра и дразнеща миризма. Газов и жълто-зелен хлор, с остър задушаващ кехлибар. Бромът е кафява тежка течност. От всички халогени само йодът е виолетово кристално вещество.
Флуорът е най-силният окислител. В групата способността да се прикрепи електрон по време на химическа реакция постепенно намалява от флуор до астатин. Причината за отслабване на това свойство е да се увеличи атомният радиус.
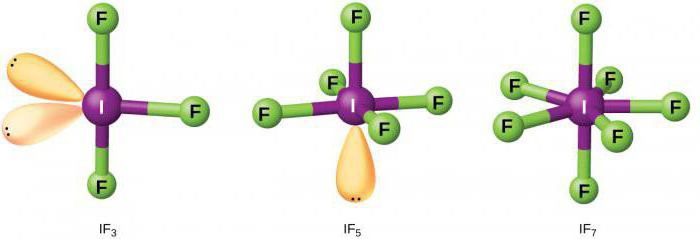
Характеристики на химичните свойства
Флуорът, който е най-силният окислител, може да реагира без допълнително загряване с почти всички неметали. Процесът е придружен от отделянето на голямо количество топлина. При металите процесът се характеризира със самозапалване на флуор.
Тъй като този халоген се характеризира с висока химическа активност, той може да взаимодейства при излагане на благородни газове.
Флуорът взаимодейства със сложни вещества. Активността на брома е значително по-ниска. Той се използва главно в органичната химия за провеждане на качествени реакции към ненаситени съединения.
Йодът взаимодейства с метали само при нагряване и процесът се характеризира с абсорбция на енергия (екзотермична реакция).
Характеристики на употреба
Каква е стойността на халогените? За да отговорите на този въпрос, разгледайте основните области на тяхното прилагане. Например, естественият минерал криолит, който е съединение на алуминий, флуор, натрий, се използва като добавка в паста за зъби, за да се предотврати кариесът на зъбите.
Хлор в големи количества, използвани в производството на солна киселина. В допълнение, този халоген се търси в производството на пластмаси, разтворители, багрила, каучуци, синтетични влакна. Голямо количество съдържащи хлор съединения се използва за ефективно борба с различни вредители на земеделски култури. Хлорът, както и неговите съединения, също са необходими за избелване на памучни и лен ленти, хартия и дезинфекция на питейна вода. Бром и йод се използват в химическата и фармацевтичната промишленост.
Напоследък озонът се използва вместо хлор за чиста питейна вода.
Биологично действие
Високата реактивност на халогените обяснява факта, че всички тези съединения са отрови, които имат задушаващ ефект и могат да увредят органичните тъкани. Въпреки тези характеристики, тези елементи са необходими за жизнените процеси на човешкото тяло.
Например, флуорът участва в метаболитни процеси в нервните клетки, мускулите, жлезите. В ежедневието тефлоновите ястия са все по-чести, флуорът е един от неговите компоненти.
Хлорът стимулира растежа на косата, стимулира обменните процеси, придава на тялото сила и жизненост. Максималното му количество под формата на натриев хлорид е част от кръвната плазма. Сред съединенията на този елемент от особен интерес от биологична гледна точка е солна киселина.
Това, че е в основата на стомашния сок, участва в процесите на разделяне на храната. За да функционира нормално тялото, човек трябва да консумира най-малко двадесет грама на ден. сол.
Всички халогени са необходими на лицето за жизнена дейност, а също така се използват от него в различни области на дейност.