Химичният елемент е ... Периодична система от химични елементи
Един химичен елемент е колективен термин, описващ набор от атоми на проста субстанция, т.е., която не може да бъде разделена на по-прости (в структурата на техните молекули) компоненти. Представете си, че получавате парче чисто желязо с искане да го разделяте на хипотетични компоненти, използвайки всяко устройство или метод, изобретен от химиците. Въпреки това, не можете да направите нищо, никога желязо не се разделя на нещо по-просто. Едно просто вещество - желязо - съответства на химичния елемент Fe. 
Теоретично определение
Посоченият по-горе експериментален факт може да бъде обяснен с помощта на тази дефиниция: химически елемент е абстрактно множество от атоми (не молекули!) От съответното просто вещество, т.е. атоми от същия вид. Ако имаше начин да се разгледа всеки от отделните атоми в парче от чистото желязо, споменато по-горе, тогава всички те ще бъдат едни и същи - железни атоми. Обратно, химическо съединение, като железен оксид, винаги съдържа поне два различни типа атоми: железни атоми и кислородни атоми.
Ad
Условия, които трябва да знаете
Атомна маса : масата на протоните, неутроните и електроните, които съставляват атом от химически елемент.
Атомно число : броят на протоните в ядрото на атома на елемент.
Химически символ : буква или двойка латински букви, представляващи обозначението на този елемент.
Химично съединение : Вещество, което се състои от два или повече химически елемента, които са свързани помежду си в определено съотношение.
Метал : елемент, който губи електрони химични реакции с други елементи.
Металоид : елемент, който понякога реагира като метал, а понякога и като неметален.
Неметални : елемент, който се стреми да произвежда електрони в химични реакции с други елементи.
Периодична система от химични елементи : системата за класификация на химичните елементи в съответствие с техните атомни номера.
Синтетичен елемент : такъв, който е изкуствено получен в лабораторията и по правило не се среща в природата. 
Естествени и синтетични елементи
Деветдесет и два химически елемента се намират в природата на Земята. Останалите са получени изкуствено в лаборатории. Синтетичен химичен елемент обикновено е продукт на ядрени реакции в ускорителите на частици (устройства, използвани за увеличаване на скоростта на субатомни частици, като електрони и протони) или ядрени реактори (устройства, използвани за контрол на енергията, отделена при ядрените реакции). Първият синтетичен елемент, получен с атомно число 43, е технеций, открит през 1937 г. от италианските физици C. Perrier и E. Segre. Освен технеций и прометий всички синтетични елементи имат ядра по-големи от тези на урана. Последното, което е получило името си, е синтетичен химичен елемент - черния дроб (116), а преди това е бил фламерий (114). 
Две дузини общи и важни елементи
| име | символ | Процент от всички атоми * | Свойства на химичните елементи (при нормални условия) | |||
| Във Вселената | В земната кора | В морска вода | В човешкото тяло | |||
| алуминий | Al | - | 6.3 | - | - | Лек сребърен метал |
| калций | Ca | - | 2.1 | - | 0.02 | Включени в състава на естествените минерали, черупки, кости |
| въглероден | C | - | - | - | 10.7 | Основата на всички живи организми |
| хлор | Cl | - | - | 0.3 | - | Отровни газове |
| мед | Cu | - | - | - | - | Само червен метал |
| злато | Au | - | - | - | - | Само жълт метал |
| хелий | той | 7.1 | - | - | - | Много лек газ |
| водород | Н | 92.8 | 2.9 | 66.2 | 60.6 | Най-лесният от всички елементи; газ |
| йод | аз | - | - | - | - | неметали; използван като антисептик |
| желязо | Fe | - | 2.1 | - | - | Магнитни метали; използвани производство на чугун и стана |
| водя | Pb | - | - | - | - | Мек тежък метал |
| магнезиев | Mg | - | 2.0 | - | - | Много лек метал |
| живак | Hg | - | - | - | - | Течен метал; един от два течни елемента |
| никел | Ni | - | - | - | - | Устойчив на корозия метал; използвани в монети |
| азот | N | - | - | - | 2.4 | Газ, основният компонент на въздуха |
| кислород | ох | - | 60.1 | 33.1 | 25.7 | Газ, вторият важен въздушен компонент |
| фосфор | P | - | - | - | 0.1 | неметали; важни за растенията |
| калий | K | - | 1.1 | - | - | метал; важно за растенията; често наричан "поташ" |
* Ако стойността не е посочена, тогава елементът е по-малък от 0,1 процента.
Големият взрив като основна причина за образуването на материята
Кой е първият химически елемент във Вселената? Учените смятат, че отговорът на този въпрос е в звездите и в процесите, чрез които се формират звездите. Смята се, че Вселената е възникнала в някакъв момент от 12 до 15 милиарда години. До този момент не се мисли за нищо друго освен за енергия. Но се случи нещо, което превърна тази енергия в огромна експлозия (т.нар. Голям взрив). В следващите секунди, след Големия взрив, материята започна да се оформя.
Ad
Първите протозойни форми на материята са протоните и електроните. Някои от тях са обединени в водородни атоми. Последният се състои от един протон и един електрон; това е най-простият атом, който може да съществува.  Бавно, в продължение на дълги периоди от време, водородните атоми започнаха да се събират в определени области на пространството, образувайки гъсти облаци. Водородът в тези облаци беше компактен. гравитационни сили. В крайна сметка, тези облаци от водород станаха достатъчно плътни, за да образуват звезди.
Бавно, в продължение на дълги периоди от време, водородните атоми започнаха да се събират в определени области на пространството, образувайки гъсти облаци. Водородът в тези облаци беше компактен. гравитационни сили. В крайна сметка, тези облаци от водород станаха достатъчно плътни, за да образуват звезди.
Звезди като химически реактори на нови елементи
Една звезда е просто маса от материя, която генерира енергията на ядрените реакции. Най-често срещаните от тези реакции са комбинация от четири водородни атома, образуващи един хелиев атом. Веднага след като звездите започнаха да се образуват, хелий станал вторият елемент, който се появил във Вселената.
Ad
Когато звездите станат по-стари, те се преместват от ядрени реакции на водород-хелий към другите им видове. В тях атомите на хелия образуват въглеродни атоми. По-късно въглеродните атоми образуват кислород, неон, натрий и магнезий. По-късно неонът и кислородът се комбинират помежду си, за да образуват магнезий. Тъй като тези реакции продължават, се образуват все повече химически елементи.
Първите системи от химични елементи
Преди повече от 200 години химиците започнаха да търсят начини да ги класифицират. В средата на XIX век са известни около 50 химически елемента. Един от въпросите, които химиците се опитват да решат. беше това: химичният елемент е съвсем различно вещество от всеки друг елемент? Или някои елементи, свързани с други по някакъв начин? Има ли общ закон, който да ги обединява?
Ad
Химиците са предложили различни системи от химични елементи. Така например, английският химик Уилям Праут през 1815 г. предполага, че атомните маси на всички елементи са кратни на масата на водородния атом, ако приемем, че е едно, т.е. трябва да са цели числа. По това време атомните маси на много елементи вече са изчислени от J. Dalton по отношение на масата на водорода. Обаче, ако това е приблизително случаят с въглерод, азот, кислород, тогава хлорът с маса 35,5 не се вписва в тази схема.
Немският химик Йохан Волфганг Доберинер (1780 - 1849) показа през 1829 г., че три елемента от така наречената халогенна група (хлор, бром и йод) могат да бъдат класифицирани по техните относителни атомни маси. Атомното тегло на бром (79.9) е почти точно средното атомно тегло на хлора (35.5) и йода (127), а именно 35.5 + 127 = 2 = 81.25 (близо до 79.9). Това е първият подход към изграждането на една от групите химически елементи. Добрейнер откри още две такива триади от елементи, но не успя да формулира общ периодичен закон.
Ad
Как се извършва периодичната система от химични елементи
Повечето от ранните класификационни схеми не бяха много успешни. След това около 1869 г. двама химици са направили почти едно откритие и почти едновременно. Руският химик Дмитрий Менделеев (1834-1907) и германският химик Юлий Лотар Мейер (1830–1895) предлагат организиране на елементи, които имат сходни физични и химични свойства в подредена система от групи, редове и периоди. В същото време Менделеев и Майер посочват, че свойствата на химичните елементи периодично се повтарят в зависимост от техните атомни тегла.
Днес Менделеев се смята за откривателя на периодичния закон, защото направи една стъпка, която Майер не е взел. Когато всички елементи се намират в периодичната таблица, в нея се появяват някои пропуски. Менделеев прогнозира, че това са места за елементи, които все още не са открити.
Въпреки това, той отиде още по-далеч. Менделеев предсказва свойствата на тези, които все още не са отворени елементи. Знаеше къде се намират в периодичната таблица, за да може да предскаже техните свойства. Трябва да се отбележи, че всеки предвиден химичен елемент на Менделеев, бъдещите галий, скандий и германий бяха открити по-малко от десет години след публикуването на периодичния закон.
Кратката форма на периодичната таблица
Имаше опити да се изчисли колко варианта на графичното изображение на периодичната система са предложени от различни учени. Оказа се, че е повече от 500. Освен това, 80% от общия брой варианти са таблици, а останалите са геометрични фигури, математически криви и т.н. В резултат на това, четири вида таблици са намерили практическо приложение: къси, полу-дълги, дълги и стълби (пирамидални). Последното е предложено от великия физик Н. Бор.
Фигурата по-долу показва кратката форма. 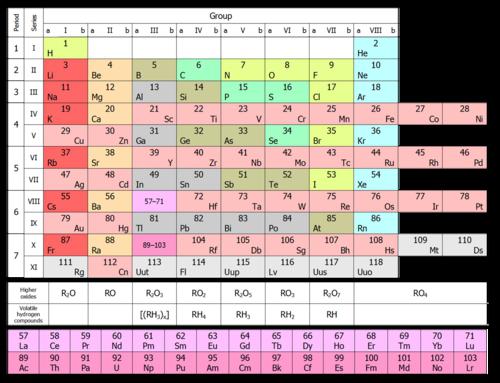 В него химичните елементи са подредени във възходящ ред на техните атомни номера отляво надясно и отгоре надолу. Така първият химически елемент на периодичната таблица водород има атомно число 1, тъй като ядрото на водородните атоми съдържа един и само един протон. По същия начин, кислородът има атомно число 8, тъй като ядрата на всички кислородни атоми съдържат 8 протони (виж фигурата по-долу).
В него химичните елементи са подредени във възходящ ред на техните атомни номера отляво надясно и отгоре надолу. Така първият химически елемент на периодичната таблица водород има атомно число 1, тъй като ядрото на водородните атоми съдържа един и само един протон. По същия начин, кислородът има атомно число 8, тъй като ядрата на всички кислородни атоми съдържат 8 протони (виж фигурата по-долу). 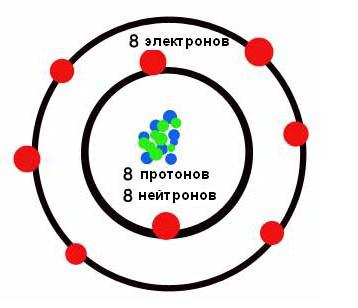
Основните структурни фрагменти на периодичната система са периоди и групи от елементи. В шест периода всички клетки са запълнени, седмият все още не е завършен (елементи 113, 115, 117 и 118, въпреки че са синтезирани в лаборатории, все още не са официално регистрирани и нямат имена).
Групите са разделени на основни (А) и вторични (В) подгрупи. Елементите на първите три периода, съдържащи по един ред, се включват изключително в A-подгрупи. Останалите четири периода включват два реда редове.
Химичните елементи в една група, като правило, имат сходни химически свойства. Така че, първата група е алкални метали вторият е алкалоземна. Елементите в същия период имат свойства, които бавно варират от алкален метал до благороден газ. Фигурата по-долу показва как една от свойствата - атомният радиус - варира за отделните елементи в таблицата.
Дългопериодна форма на периодичната таблица
Тя е показана на фигурата по-долу и е разделена в две посоки, в редове и колони. Има седем редови периода, както в кратка форма, и 18 колони, наречени групи или семейства. Всъщност, увеличаването на броя на групите от 8 в кратка форма до 18 години се получава чрез поставяне на всички елементи в периодите, започващи от 4-ти, а не в две, а в един ред.
За групите се използват две различни системи за номериране, както е показано в горната част на таблицата. Системата, базирана на римски цифри (IA, IIA, IIB, IVB и др.), Традиционно е популярна в САЩ. Другата система (1, 2, 3, 4 и т.н.) традиционно се използва в Европа и се препоръчва за употреба в Съединените щати преди няколко години.

Появата на периодичните таблици в горните цифри е малко подвеждаща, както във всяка публикувана таблица. Причината за това е, че двете групи елементи, показани в долната част на таблиците, всъщност трябва да бъдат разположени вътре в тях. Лантанидите, например, принадлежат към период 6 между барий (56) и хафний (72). В допълнение, актинидите принадлежат към период 7 между радий (88) и рутерфорд (104). Ако те бяха вмъкнати в масата, то щеше да стане твърде широко, за да се побере на лист хартия или на стена. Затова е обичайно тези елементи да се поставят в долната част на таблицата.