Физични и химични свойства на йода
Йодът е добре известен химичен елемент. Но повечето хора са запознати само с неговия алкохолен разтвор, който се използва в медицината. Напоследък те често говорят за неговия дефицит в организма при заболяване на щитовидната жлеза. Рядко известни физични и химични свойства на йода. А това е доста странен елемент, който е широко разпространен в природата и важен за човешкия живот.
Дори в ежедневието можете да използвате химичните свойства на йода, например, за да определите присъствието на нишесте в храните. Освен това в последно време се рекламираха много популярни методи за използване на този микроелемент за лечение на много заболявания. Ето защо всеки трябва да знае какви свойства има.
Обща характеристика на йода
Това е доста активен микроелемент, свързан с неметалите. В периодичната таблица тя е в групата на халогените с хлор, бром и флуор. Йодът е обозначен със символа I и има сериен номер 53. Този микроелемент е получил името си през 19-ти век поради виолетовия цвят на изпаренията. В крайна сметка, в гръцки йод се превежда като "виолетов, виолетов".
Така бе открит йод. Химикът Бернар Куртуа, работещ във фабрика за производство на нитрати, открива това вещество случайно. Котката обърна епруветката със сярна киселина и се качи на пепелта от водорасли, от която получи селитра. В същото време освобождава газ с пурпурен цвят. Това интересуваше Бернар Куртуа и той започна да изучава нов елемент. Така в началото на 19 век стана известно за йод. В средата на 20-ти век химиците започнали да наричат този елемент „йод“, въпреки че старото наименование е все по-често срещано.

Химични свойства на йода
Уравненията, показващи активността на химичните реакции на този елемент, не казват нищо на обикновен човек. Само тези, които са запознати с химията, разбират, че техните химически свойства са описани с тяхна помощ. Това е най-активният елемент от всички неметали. Йодът може да реагира с много други вещества, образувайки киселини, течни и летливи съединения. Въпреки, че сред халогените е най-малко активен.
Накратко, химическите свойства на йода могат да бъдат разгледани на примера на неговите реакции. При различни метали йодът реагира дори и при леко нагряване с образуването на йодиди. Най-известни са калиевите и натриевите йодиди. Той само частично реагира с водород и не се комбинира с някои други елементи. Той е несъвместим с азот, кислород, амоняк или етерични масла. Но най-известното химическо свойство на йода е неговата реакция с нишесте. Когато се добавят към вещества, съдържащи скорбяла, те стават сини.

Физични свойства
От всички микроелементи йодът се счита за най-спорен. Повечето хора не знаят за характеристиките му. Физико-химичните свойства на йода се изучават за кратко в училище. Този елемент се разпространява главно под формата на изотоп с маса 127. Той е най-тежкият от всички халогени. Има и радиоактивен йод 125, който се получава при разпадането на уран. В медицината често се използват изкуствени изотопи на този елемент с маса 131 и 133.
От всички халогени, йодът е единственият, който е твърд в естественото си състояние. Тя може да бъде представена от тъмнолилави или черни кристали или плочи с метален блясък. Те имат слаб мирис, работят добре и са като графит. В това състояние, този микроелемент е слабо разтворим във вода, но много лесно преминава в газообразно състояние. Той може да се превърне в пурпурен пара вече при стайна температура. Тези физикохимични свойства на йода се използват за получаването му. Нагряването на микроелемента под налягане, а след това охлаждане, се почиства от примеси. Йод се разтваря в алкохол, глицерин, бензол, хлороформ или въглероден дисулфид, за да се получат кафяви или пурпурни течности.

Източници на йод
Въпреки важността на този микроелемент за живота на много организми, йодът е доста труден за откриване. Кората му съдържа по-малко от най-редките елементи. Но все още се смята, че йодът е широко разпространен в природата, тъй като той присъства в малки количества почти навсякъде. Тя е концентрирана главно в морска вода, водорасли, почва, някои растителни и животински организми.
Химичните свойства на йода обясняват, че той не се среща в чист вид, само под формата на съединения. Най-често се извлича от пепел от морски водорасли или от отпадъци от производството на натриев нитрат. Така че, йодът се добива в Чили и Япония, които са лидери в извличането на този елемент. Освен това може да се получи от водите на някои солени езера или нефтени води.
В човешкото тяло йодът идва от храната. Намира се в почви и растения. Но у нас почвите са бедни на йод. Затова най-често се използват йодни торове. За предотвратяване на заболявания, свързани с дефицит на йод, елементът се добавя към сол и някои общи храни.

Неговата роля в живота на тялото
Йодът е един от онези микроелементи, които участват в много биологични процеси. В малки количества, той присъства в много растения. Но в живите организми е много важно. Йодът се използва при производството на тиреоидни хормони на щитовидната жлеза. Те регулират процесите на жизнената дейност на организма. При липса на йод при хората, щитовидната жлеза се увеличава, възникват различни патологии. Те се характеризират с намалена работоспособност, слабост, главоболие, намалена памет и настроение.
Медицински приложения
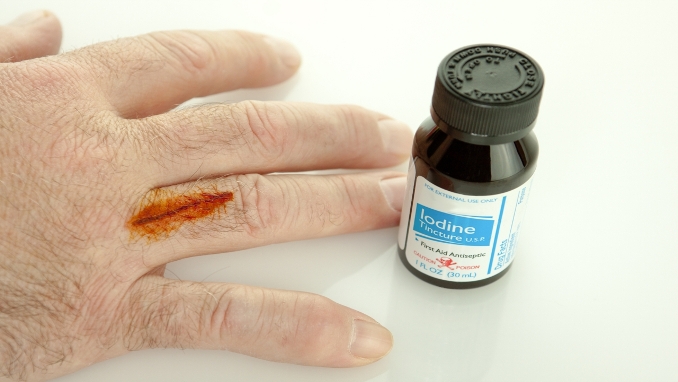
Най-честият 5% алкохолен разтвор на йод. Използва се за дезинфекция на кожата около лезиите. Но това е доста агресивен антисептик, така че напоследък са използвани по-меки разтвори на йод със скорбяла, например Betadine, Yoks или Yodinol. Отоплителните свойства на йода често се използват за премахване на болките в мускулите или патологиите на ставите, а след инжектиране се прави йодна мрежа.
Йодните препарати се използват и при радиографски и томографски методи за изследване. А някои изотопи на йода са ефективни при лечение на заболявания на щитовидната жлеза. Напоследък се появиха и мултивитаминни препарати, съдържащи йод. Те се предписват, когато се открие дефицит на този микроелемент.
Промишлени приложения
Този микроелемент също е от голямо значение в промишлеността. Специалните химични свойства на йода позволяват използването му в различни индустрии. Например, в съдебната медицина се използва за идентифициране на пръстови отпечатъци върху хартиени повърхности. Йодът се използва широко като източник на светлина в халогенните лампи. Използва се във фотографията, киното, металообработването. И наскоро, този микроелемент е бил използван в дисплеи с течни кристали, когато се създават стъкла с димиране, както и в областта на лазерния синтез.

Опасност за хората
Въпреки важността на йода в процесите на жизнената дейност, в големи количества той е токсичен за хората. Само 3 g от това вещество води до сериозно увреждане на бъбреците и сърдечно-съдовата система. Първо, човек се чувства слабост, главоболие, появява се диария и сърцето му се ускорява. Ако вдишвате йодни пари, има дразнене на лигавиците, очни изгаряния, белодробен оток. Без лечение, отравяне с йод е фатално.