Пептидното свързване е в основата на първичната структура на протеина. Характеризиране и образуване на пептидна връзка
Пептидната връзка е силна връзка между фрагментите от две аминокиселини, които са в основата на образуването на линейни протеинови структури и пептиди. В такива молекули всяка аминокиселина (с изключение на крайните) се комбинира с предишната и следващата.
В зависимост от броя на връзките, пептидните връзки могат да създават дипептиди (състоящи се от две аминокиселини), трипептиди (от три), тетрапептиди, пентапептиди и др. Кратки вериги (от 10 до 50 мономери) се наричат олигопептиди, а дългите - полипептиди и протеини ( тегл. повече от 10 000. Да).
Характеристики на пептидната връзка
Пептидна връзка е ковалентно химично съединение между първия въглероден атом на една аминокиселина и азотния атом на другото, получено от взаимодействието на алфа-карбоксилна група (СООН) с алфа-амино група (NH2). Когато това се случи, нуклеофилното заместване на ОН-хидроксила върху аминогрупата, от която се отделя водород. В резултат на това се образуват една CN връзка и водната молекула.
Ad
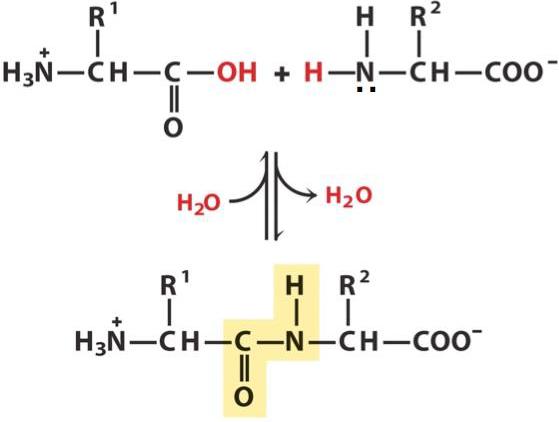
Тъй като по време на реакцията се губят някои компоненти (ОН групи и водороден атом), пептидните единици вече не се наричат аминокиселини, а аминокиселинни остатъци. Поради факта, че последните съдържат по 2 въглеродни атома, в пептидната верига се извършва редуване на С-С и CN връзки, които образуват пептидния скелет. От двете му страни са аминокиселинни радикали. Разстоянието между въглеродните и азотните атоми варира от 0.132 до 0.127 nm, което показва неопределена връзка.
Пептидната връзка е много силна форма на химично взаимодействие. При стандартните биохимични условия, съответстващи на клетъчната среда, тя не подлежи на самоунищожение.
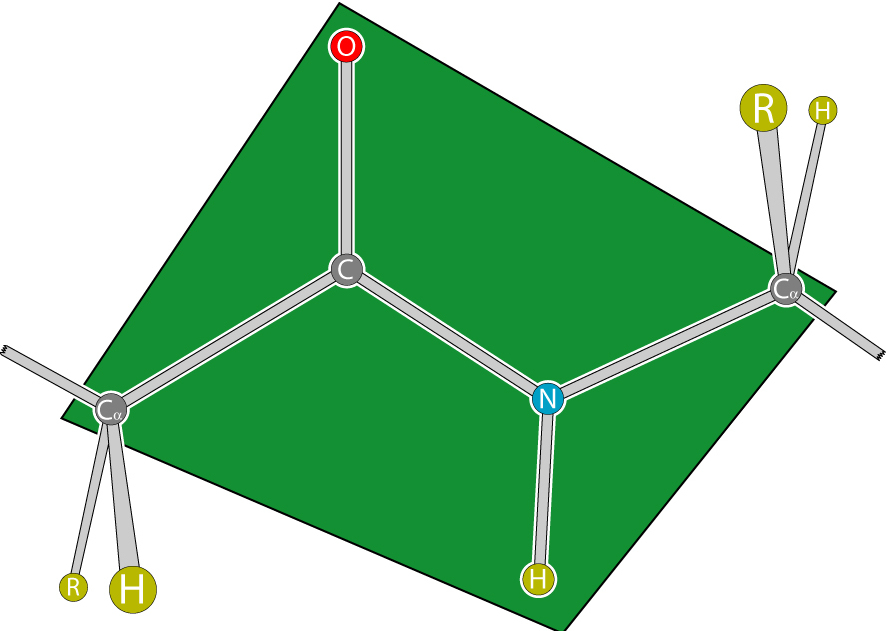
Пептидната връзка на протеини и пептиди се характеризира с свойството на копланарност, тъй като всички атоми, включени в неговото образуване (С, N, О и Н) са разположени в една и съща равнина. Това явление се обяснява с твърдостта (т.е. невъзможността за въртене на елементите около връзката) в резултат на резонансна стабилизация. В аминокиселинната верига между равнините на пептидните групи са а-въглеродни атоми, свързани с радикали.
Ad
Видове конфигурация
В зависимост от позицията на алфа-въглеродните атоми по отношение на пептидната връзка, последните могат да имат 2 конфигурации:
- "cis" (разположен от едната страна);
- "транс" (от различни страни).
Трансформата е по-устойчива. Понякога конфигурациите се характеризират с местоположението на радикалите, което не променя същността, тъй като те са свързани с алфа-въглеродни атоми.
Явление на резонанса
Особеността на пептидната връзка е, че тя е 40% двойна и може да бъде в три форми:
- Кетол (0.132 nm) - CN-връзка се стабилизира и е напълно единичен.
- Преходна или мезомерна - междинна форма, има частично неопределена.
- Enol (0.127 nm) - пептидната връзка става напълно двойна, а C - O съединението е напълно единично. В този случай кислородът придобива частично отрицателен заряд, а водороден атом - частично положителен.
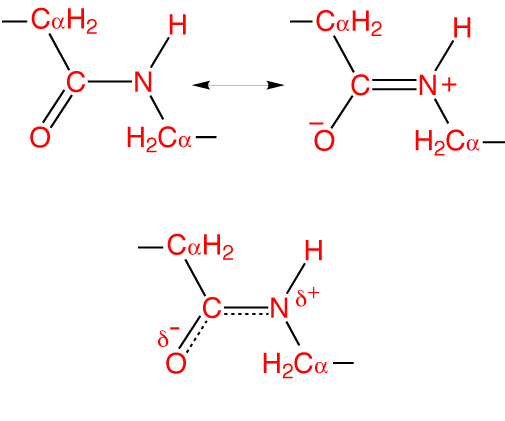
Тази характеристика се нарича резонансен ефект и се обяснява с делокализацията на ковалентната връзка между въглеродните и азотните атоми. В този случай, хибридните sp 2 орбитали образуват електронен облак, който се разпространява до кислороден атом.
Образуване на пептидна връзка
Образуването на пептидна връзка е типична реакция на поликондензация, която е термодинамично неблагоприятна. При естествени условия равновесието се измества към свободни аминокиселини, следователно, за да се осъществи синтеза, е необходим катализатор, който активира или модифицира карбоксилната група за по-лесно поддържане на хидроксил.
В една жива клетка се образува пептидна връзка в центъра на протеиновия синтез, където специфични ензими, работещи с енергията на макроергичните връзки действат като катализатор.