Дали методът за титриметричен анализ е това?
Титриметричният метод за анализ (титруване) позволява да се извърши обемно количествен анализ и се използва широко в химията. Основното му предимство е разнообразието от методи и методи, поради което може да се използва за решаване на различни аналитични задачи.
Принцип на анализ
Титриметричният метод за анализ се основава на измерване на обема на разтвор с известна концентрация (титрант), който реагира с изпитваното вещество.
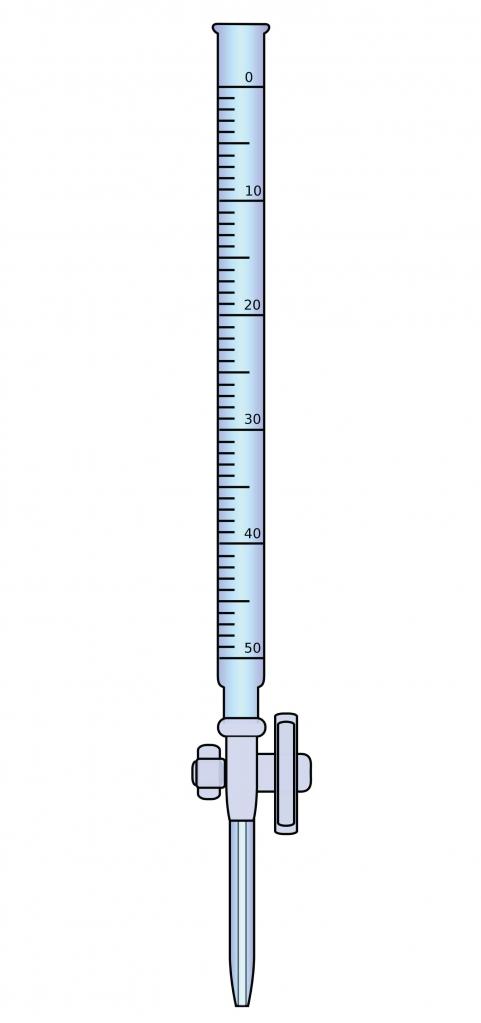
За анализа ще ви е необходимо специално оборудване, а именно бюрета - тънка стъклена тръба с приложено градуиране. Горният край на тази тръба е отворен, а отдолу има спирателен кран. Калибрираната бюрета с помощта на фуния запълва титранта до нула. Анализът се извършва до крайната точка на титруването (СТТ), като се добавя малко количество разтвор от бюретата към изпитваното вещество. Крайната точка на титруването се идентифицира чрез промяна в цвета на индикатора или някакво физикохимично свойство.
Крайният резултат се изчислява чрез изразходвания обем на титранта и се изразява в титър (T) - масата на веществото на 1 ml разтвор (g / ml).
Процес на обосновка
Титриметричният метод за количествен анализ дава точни резултати, тъй като веществата реагират една с друга в еквивалентни количества. Това означава, че произведението на техния обем и количество е идентично помежду си: C 1 V 1 = C 2 V 2 . От това уравнение е лесно да се намери неизвестната стойност на C 2 , ако останалите параметри са зададени независимо (C 1 , V 2 ) и са установени по време на анализа (V 1 ).
Детекция на крайната точка на титруване
Тъй като навременното записване на края на титруването е най-важната част от анализа, трябва да изберете правилните методи. Използването на цветни или флуоресцентни индикатори се счита за най-удобното, но могат да се използват и инструментални методи като потенциометрия, амперометрия и фотометрия.

Окончателният избор на метода за откриване на СТТ зависи от изискваната точност и селективност на определянето, както и от неговата скорост и възможности за автоматизация. Това е особено вярно за мътни и оцветени решения, както и за агресивни среди.
Изисквания за реакция на титруване
За да може титриметричният метод на анализ да даде правилния резултат, трябва да избереш правилната реакция, която ще я подкрепи. Изискванията към него са следните:
- стехиометрия;
- висок дебит;
- висока равновесна константа;
- наличие на надежден метод за фиксиране на експерименталния край на титруването.
Подходящите реакции могат да бъдат от всякакъв тип.
Видове анализи
Класификацията на методите за титриметричен анализ се основава на типа реакция. На тази основа се разграничават следните методи за титруване: t
- киселина-основа;
- редокс;
- комплексометричното;
- А гарафа.
Всеки тип се основава на собствен тип реакция, се избират специфични титранти, в зависимост от това кои подгрупи от методи са идентифицирани в анализа.
Титруване на киселинна основа
Титриметричният метод за анализ, използващ реакцията на взаимодействието на хидроксин с хидроксиден йон (Н3О + + ОН - = Н 2 О), се нарича киселинно-основа. Ако известно вещество образува протон в разтвора, което е типично за киселини, методът принадлежи към ацидиметричната подгрупа. Тук обикновено се използва стабилна солна киселина HCl като титрант.
Ако титрантът образува хидроксиден йон, методът се нарича алкалиметрия. Използваните вещества са алкални, например NaOH, или соли, получени чрез взаимодействие на силна основа със слаба киселина, като Na2C03.
Използвани са индикатори в този цвят. Те са слаби органични съединения - киселини и основи, в които се различават структурата и цвета на протонираните и непротонираните форми. Най-често монохроматичният индикатор фенолфталеин (бистър разтвор в алкална среда става малина) и двуцветният метил оранжев (червеното вещество пожълтява в кисела среда) се използват при киселинно-алкално титруване.

Широко разпространената им употреба е свързана с висока абсорбция на светлина, поради което техният цвят е ясно видим за невъоръженото око, както и контрастната и тясна преходна област на цвета.
Редокс титруване
Редокс-титриметричният анализ е метод за количествен анализ, основан на промяната в съотношението на концентрациите на окислените и редуцираните форми: aOx 1 + bRed 2 = aRed 1 + bOx 2 .
Методът е разделен на следните подгрупи:
- перманганатометрия (титрант - KMnO4);
- йодометрия (I2);
- дихроматометрия (K2Cr207);
- броматометрия (KBr03);
- йодометрия (KIO 3 );
- кериметрия (Ce (SO4) 2 );
- ванадометрия (NH4VO3);
- титанометрия (TiCl3);
- хромометрия (CrCl2);
- аскорбометрия (С6Н8ОН).
В някои случаи ролята на индикатора може да се играе от реагент, който участва в реакцията и променя цвета си с придобиването на окислена или редуцирана форма. Но те също използват специфични показатели, например:
- При определяне на йод се използва нишесте, което образува тъмно синьо съединение с I3-йони;
- при титруването на железното желязо се използват тиоцинатни йони, образуващи комплекси с метала, боядисани в яркочервен цвят.

В допълнение, има специални окислително-редукционни индикатори - органични съединения с различни цветове на окислените и редуцираните форми.
Комплексометрично титруване
Накратко, титриметричният метод на анализ, наречен комплексометричен, се основава на взаимодействието на две вещества с образуването на комплекс: M + L = ML. Ако се използват живачни соли, например, Hg (NO 3 ) 2 , методът се нарича меркуриметрия, ако етилендиаминтетраоцетната киселина (EDTA) е комплексно. По-специално, като се използва последният метод, за анализ на водата се използва титриметричен метод, а именно неговата твърдост.
При комплексонометрията се използват прозрачни метални индикатори, които придобиват цвят при образуването на комплекси с метални йони. Например, когато се титруват соли на железното желязо с EDTA, като индикатор се използва прозрачна сулфосалицилова киселина. Той оцветява разтвора в червено, когато е комплексно с желязо.

Въпреки това металните индикатори често имат собствен цвят, който варира в зависимост от концентрацията на металния йон. Като такива се използват многоосновни киселини, които образуват сравнително стабилни комплекси с метали, които в същото време бързо се влошават, когато са изложени на EDTA с контрастиращо обезцветяване.
Титруване на утаяване
Преципитира се титриметричният метод за анализ, който се основава на реакцията на взаимодействието на две вещества с образуването на твърдо съединение, което се утаява (M + X = MX ↓). Тя има ограничена стойност, тъй като обикновено процесите на отлагане протичат неквантизирани и нестехиометрични. Но понякога той все още се използва и има две подгрупи. Ако в метода се използват сребърни соли, например AgNO 3 , то се нарича аргентометрия, ако са живачни соли, Hg 2 (NO 3 ) 2 , а след това - меркурометрия.
За откриване на крайната точка на титруването се използват следните методи:
- Методът на Мора, в който индикаторът е хроматен йон, образуващ седимент от червени тухли със сребро;
- метода на Фолгард, основан на титруването на разтвор на сребърни йони с калиев тиоцианат в присъствието на железно желязо, което образува червен комплекс с титранта в кисела среда;
- Фаянсов метод, включващ титруване с адсорбционни индикатори;
- Gay-Lussac метод, при който CTT се определя чрез просветление или замъгляване на разтвора.

Последният метод на практика не е използван наскоро.
Методи за титруване
Титруването се класифицира не само чрез основната реакция, но и чрез метода на прилагане. На тази основа се различават следните видове: t
- директно;
- обратното;
- титруване на заместителя.
Първият случай се използва само в условия на идеална реакция. Титрантът се добавя директно към веществото, което трябва да се открие. Така с помощта на EDTA се определят магнезий, калций, мед, желязо и около 25 метала. Но в други случаи по-често се използват по-сложни методи.
Обратно титриране
Идеалната реакция не винаги е възможно да се избере. Най-често той протича бавно или е трудно да избере метод за фиксиране на крайната точка на титруване, или между продуктите се образуват летливи съединения, поради което веществото, което трябва да се определи, е частично загубено. За да се преодолеят тези недостатъци, можете да използвате метода на обратното титруване. За да се направи това, голямо количество титрант се излива в веществото, което трябва да се открие, така че реакцията да приключи, и след това се определя колко остава нереагирал разтвор. За целта остатъците от титранта от първата реакция (Т1) се титруват с друг разтвор (Т2), а количеството му се определя от разликата на продуктите от обемите и концентрациите в две реакции: С T1 V T 1 -C T 2 V T 2 .
Използването на титриметричния метод за анализ по обратния начин е в основата на определянето на манганов диоксид. Неговото взаимодействие с железен сулфат е много бавно, така че солта се взема в излишък и реакцията се ускорява чрез нагряване. Нереагиралото количество железен йон се титрува с калиев дихромат.

Титруване заместник
Титруването на заместителя се използва в случай на нестехиометрични или бавни реакции. Неговата същност е, че за аналита се избира стехиометрична реакция с помощно съединение, след което продуктът за взаимодействие се подлага на титруване.
Това е, което правят при определянето на дихромата. Към него се добавя калиев йодид, което води до освобождаване на йоден еквивалент, еквивалентен на веществото, което трябва да се открие, което след това се титрува с натриев тиосулфат.
Така титриметричният анализ позволява да се определи количественото съдържание на широк спектър от вещества. Познавайки техните свойства и особености на реакциите, може да се избере оптималният метод и метод на титруване, който ще даде резултат с висока степен на точност.