Особености на структурата на водородния атом
Най-често срещаният елемент в пространството, състоящ се от най-леките атоми, е водород. Открит е през 14 век от великия алхимик Парацелз. Учените с право се считат за основатели не само на медицината, но и на химията. Структурата на водородния атом беше допълнително подробно разгледана от Niels Bohr. Тогава елементът е открит от астрономите като част от Слънцето и други планети, както и от газовите звездни мъглявини. В тях се осъществява процесът на превръщане на водородните атоми в хелиеви атоми, с други думи се наблюдава ядрена реакция. В нашата статия ще изследваме не само структурата на водородния атом, но и ще разгледаме характерните особености на свойствата на този химичен елемент.
Мястото на елемента в периодичната система
Водородът е единственият химичен елемент, който се намира в две групи на периодичната система едновременно: 1 и 7. Може да се обясни следният факт: той има двойни химични свойства. Специалната структура на водородния атом му позволява да дари единствения си електрон на атомите, например, на активните елементи - неметали. Това са предимно халогени: агресивни по своите свойства флуор, хлор, бром и йод. Н 2 лесно взаимодейства с халкогени: сяра, кислород, селен. В този случай водородните атоми се превръщат в катиони - положително заредени частици.
Поради тази функция елементът заема своето място в първата група на периодичната система. Механизмът на реакцията между метали и водород изглежда различен. Според теорията за структурата на водородния атом според Н. Бор, елементът има един несдвоен електрон. Атом H приема електрони от активни атоми на алкални или алкалоземни метали. Така неговата електронна конфигурация става подобна на частица от инертен газ от хелий. Единственият енергиен слой вече е напълно завършен. При тези процеси структурата на водородния атом се променя и тя се променя в анионната форма. Поради тази причина елементът е разположен едновременно в периодичната таблица и в неговата 7-ма група.

Всичко в сравнение
Продължавайки да изучаваме структурните характеристики на водородните частици, нека да видим как тяхната вътрешна структура влияе на поведението на даден елемент в реакциите. За да направите това, обърнете внимание на най-близките й съседи в периодичната система и определете структурата на атомите на водорода, хелия и лития. С частици от инертен газ, водородът съчетава същото количество енергийни нива, с литий, подобна структура на външния енергиен слой, на който се намира един електрон. Въпреки това, свойствата на водорода са много различни както от инертен газ, така и от алкален метал. Този факт доказва, че всички характеристики на химичния елемент се определят от структурата на кухината на атома и молекулата на водорода, т.е. броя на енергийните нива и разпределението на електроните върху тях.
Раждане на вода
Името на елемента показва, че комбинацията от атоми с кислородни частици води до появата на такова уникално и важно вещество за Земята като водата. При нормални условия тази реакция не настъпва, температурата на горене на газовата смес достига 2800 ° С. В лабораторията взаимодействието между Н 2 и О 2 в съотношение 2: 1 води до експлозия. Самата смес се нарича детониращ газ и процесът, който се провежда в него, преминава през механизъм на свободните радикали. Ако не се контролира, реакцията завършва със сериозен проблем - мощна експлозия. Поради тази причина, въпреки изключителната си лекота, водородът е бил изоставен като пълнител за самолети във въздуха. Тъжната причина беше катастрофата на дирижабъла на Хинденбург, водещ към Америка през 1937 година. Нека сега да видим как структурата на водородния атом засяга физическите характеристики на газа.

Водород, деутерий, тритий
Не се изненадвайте от горния списък с термини. Всичко е за един и същ химичен елемент водород, а ядреният заряд на атом е +1. Второто и третото имена са имената на изотопите. Причината за техните разлики е в броя на неутроните в ядрото, докато протонният брой на трите вида частици е един и същ. Деутерият има два неутрона, тритий има 3, а самият водород има 1 неутрон в ядрото си. Водата, съдържаща деутерий в молекулите си, се нарича тежка. Той може да се намери в охлаждащите езера на атомните електроцентрали, както и в цитоплазмата на клетките, които имат нарушен нормален метаболизъм.
Електронна структура на водородния атом
Схемата по-долу ще ни помогне да разберем специфичното поведение на проста субстанция Н 2 в различни химични взаимодействия.
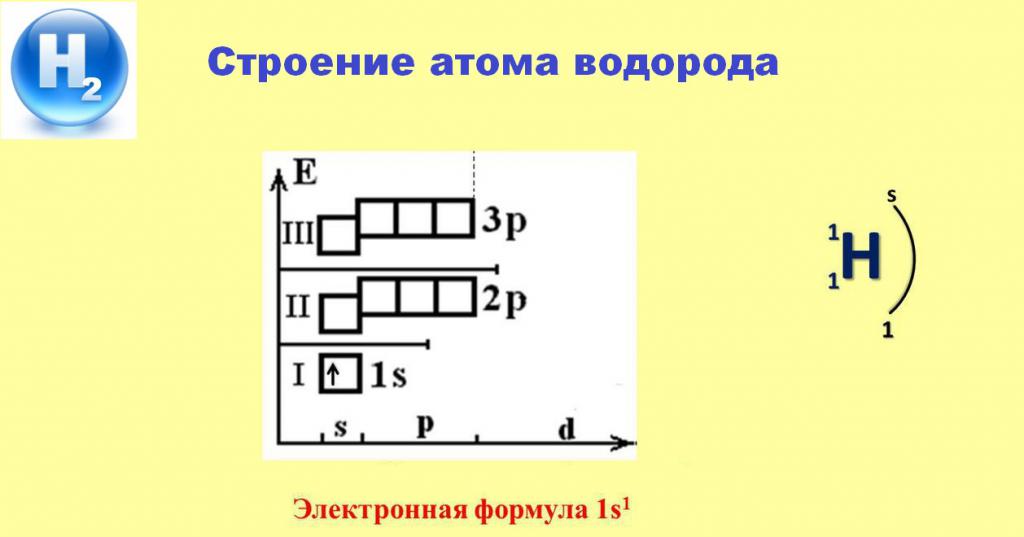
Наличието на един-единствен електрон, заемащ s-орбитата на първото енергийно ниво, осигурява постоянната валентност на водорода, равна на 1. В повечето случаи този електрон напуска пространството на атома и поема повече електроотрицателни елементи. Само реакциите с метали позволяват водородът да изтегли електрона от атомите на активните алкални или алкалоземни елементи в сферата на влияние на собственото си ядро, образувайки бели кристални съединения - техните хидриди.
Активни и агресивни
Атомният водород, така да се каже, е лесен за повдигане. Други редуциращи агенти като въглерод или неговите оксиди могат да завиждат на неговата скорост при намаляване на металите от техните оксиди. Атомите на Н са активно съчетани с частици сяра, кислород и фосфор. Пламъчната горелка с атомен водород дава затопляне над 4000 ° C. Поради тази причина такива устройства са лесни за обработка на метални повърхности: изрязани или заварени.

Атомният водород е добре установен като редуциращ агент на чистите метали - волфрам, молибден - от техните руди, представени основно от оксиди. Когато се срещат със същите атоми като него, водородът образува стабилна и пасивна структура - молекула. И двата атома Н се държат заедно от обща електронна двойка, като модел на стабилна ковалентна неполярна връзка. Той е издръжлив и осигурява стабилността на молекулите Н 2 както при земни условия, така и в пространството. Хранително-вкусовата промишленост, в която се използва за хидриране на масла и производството на нискокалорични спредове, които са модерни в съвременната диетология, не е без водород.

В нашата статия изследвахме структурата на водородния атом и открихме как тя влияе върху свойствата на едно просто вещество.