Електрохимична корозия и защита срещу нея
Корозията се отнася до процеса на спонтанно разрушаване на повърхността на материалите поради взаимодействието с околната среда. Неговата причина е термодинамичната нестабилност на химичните елементи към определени вещества. Формално, полимери, дърво, керамика, каучук са подложени на корозия, но терминът „стареене“ се прилага по-често. Най-сериозните щети са причинени от ръждясването на метали, за чиято защита се разработват високотехнологични контрамерки. Но ние ще говорим за това по-късно. Учените се различават по химична и електрохимична корозия на метали.

Химическа корозия
Обикновено се появява, когато е изложена на метална структура на сухи газове, течности или разтвори, които не извършват електрически ток. Същността на този тип корозия е прякото взаимодействие на метала с агресивна среда. Елементите се разяждат химически по време на топлинна обработка или в резултат на продължителна работа при достатъчно високи температури. Това се отнася за остриетата. газови турбини, пещи за топене на фитинги, части от двигатели с вътрешно горене и т.н. В резултат на това на повърхността се образуват определени съединения: оксиди, нитриди, сулфиди.
Ad
Електрохимична корозия
Това е резултат от метален контакт с течна среда, способна да провежда електрически ток. Поради окисляването материалът претърпява структурни промени, водещи до образуване на ръжда (неразтворим продукт), или метални частици се прехвърлят в разтвор на йони.
Електрохимична корозия: Примери
Той се разделя на:
- Атмосферно, което възниква, когато върху металната повърхност има течен филм, в който газовете, съдържащи се в атмосферата (например, O 2 , CO 2 , SO 2 ), могат да се разтварят с образуването на електролитни системи.
- Течност, която тече в проводима течна среда.
- Почва, която тече под влиянието на подпочвените води.
причини
Тъй като обикновено всеки метал, който се използва за промишлени нужди, не е напълно чист и съдържа включвания от различни видове, електрохимичната корозия на металите възниква в резултат на образуването на голям брой късо свързани локални галванични клетки върху повърхността на желязото.
Ad
Външният им вид може да бъде свързан не само с наличието на различни (особено метални) примеси (контактна корозия), но и с повърхностна хетерогенност, дефекти. кристална решетка механични повреди и други подобни.
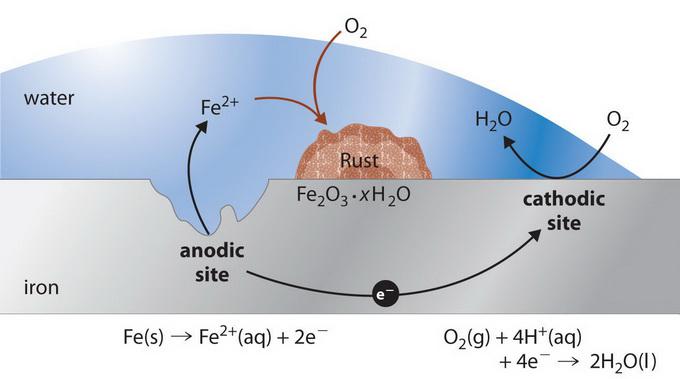
Механизъм на взаимодействие
Процесът на електрохимична корозия зависи от химичния състав на материалите и екологичните характеристики. Ако така нареченият технически метал е покрит с мокър филм, тогава във всеки от тези галванични микроелементи, които се образуват на повърхността, се осъществяват две независими реакции. По-активният компонент на корозионната двойка дарява електрони (например цинк в двойка Zn-Fe) и преминава в течната среда като хидратирани йони (т.е. корозира) чрез следната реакция (аноден процес):
M + nH2O = Mz + * nH2O + ze.
Тази част от повърхността е отрицателният полюс на локалния микроелемент, където металът се разтваря електрохимично.
В по-малко активната част на повърхността, която е положителният полюс на микроелемента (желязо в двойката Zn-Fe), електроните са обвързани поради редукционната реакция (катоден процес) по схемата:
Ad
Ox + ze = Червено.
По този начин, присъствието на окислителни агенти във воден филм, които са способни да свързват електрони, прави възможно да се продължи анодният процес. Съответно, електрохимичната корозия може да се развие, само ако се случват едновременно анодни и катодни процеси. Поради инхибирането на една от тях скоростта на окисление намалява.

Поляризационен процес
И двата гореспоменати процеса предизвикват поляризация на съответните полюси (електроди) на микроелемента. Какви са характеристиките тук? Обикновено електрохимичната корозия на металите се забавя значително от катодната поляризация. Следователно, той ще бъде усилван под влияние на фактори, които предотвратяват тази реакция и са придружени от така наречената деполяризация на положителния електрод.
В много корозионни процеси катодната деполяризация се извършва чрез изпускане на водородни йони или чрез редукция на водни молекули и съответства на формулите:
- В кисела среда: 2Н + + 2е = Н2.
- В алкална: 2Н2О + 2е = Н2 + 2ОН - .
Потенциален обхват
Потенциалът, който съответства на тези процеси, в зависимост от естеството на агресивната среда, може да варира от -0.83 до 0 V. За неутрален воден разтвор при температури близки до стандартните, той е приблизително -0.41 V. Следователно, водородните йони, съдържащи се във вода и в неутрални водни системи, могат да окисляват само метали с потенциал по-малък от -0.41 V (разположени в серия от напрежения към кадмий). Предвид факта, че някои от елементите са защитени с оксиден филм, броят на металите, чувствителни към окисление в неутрални среди от водородни йони, е незначителен.
Ако влажен филм съдържа разтворен кислород на въздуха, то той може, в зависимост от естеството на средата, да свързва електрони чрез ефекта на кислородна деполяризация. В този случай схемата на електрохимичната корозия е както следва:
Ad
- О2 + 4е + 2Н20 = 4OH - или
- О2 + 4е + 4Н + = 2Н20.
Потенциалите на тези електродни реакции при температури близки до стандартните варират от 0,4 V (алкална среда) до 1,23 V (кисела среда). В неутрални среди потенциалът на процеса на редукция на кислород при тези условия съответства на стойност от 0,8 V. Следователно, разтворен кислород е способен да окислява метали с потенциал по-малък от 0,8 V (разположен в серия от напрежения за сребро).

Основни оксиданти
Видовете електрохимична корозия се характеризират с окислителни елементи, най-важните от които са водородните йони и кислорода. В същото време, филм, съдържащ разтворен кислород, е много по-опасен от корозия, отколкото от влага, където няма кислород, и който е способен да окислява металите само с водородни йони, тъй като в последния случай броят на видовете материали, които могат да корозират, е много по-малък.
Ad
Например в стоманата и в желязото въглеродните примеси присъстват главно под формата на железен карбид Fe 3 C. В този случай механизмът на електрохимичната корозия с деполяризация на водород за тези метали е следният:
- (-) Fe - 2e + nH 2 O = Fe 2+ nH 2 O (може да се образува ръжда);
- (+) 2Н + + 2е = Н2 (в подкислена среда);
- (+) 2Н2О + 2е = Н2 + 2ОН - (в неутрална и алкална среда).
Механизмът на корозия на желязото, който съдържа примеси от мед, в случая на кислородна деполяризация на катода се описва с уравнения:
- (-) Fe-2e + nH2O = Fe2 + nH2O;
- (+) 0.502 + Н20 + 2е = 2OH - (в подкислена среда);
- (+) 0.5O2 + 2H + + 2e = Н20 (в неутрална и алкална среда).
Електрохимичната корозия протича с различни скорости. Този индикатор зависи от:
- потенциални разлики между полюсите на микропластичния елемент;
- състав и свойства на електролитната среда (рН, наличие на инхибитори на корозията и стимуланти);
- концентрация (скорост на потока) на окислителя;
- температура.
Методи за защита
Електрохимичната защита на метали от корозия се постига по следните начини:
- Създаване на антикорозионни сплави (легиране).
- Увеличете чистотата на отделния метал.
- Чрез нанасяне на повърхността на различни защитни покрития.
Тези покрития на свой ред са:
- Неметални (бои, лакове, смазочни материали, емайл).
- Метални (анодни и катодни покрития).
- Образува се чрез специална повърхностна обработка (пасивиране на желязо в концентрирана сярна киселина или. T азотна киселина; желязо, никел, кобалт, магнезий в алкални разтвори; образуването на оксиден филм, например, на алуминий).
Метални листове
Най-интересно и обещаващо е електрохимичната защита от корозия на друг вид метал. По естеството на защитния ефект метализираните покрития се разделят на анодни и катодни. Нека се спрем на този въпрос по-подробно.
Анодното покритие е покритие, образувано от по-активен (по-малко благороден) метал от този, който е защитен. Това означава, че защитата се извършва от елемент, който е в обхвата на напреженията на основния материал (например покритието от желязо с цинк или кадмий). В случай на локално разрушаване на защитния слой, по-малко благородното покритие на метала ще корозира. В зоната на драскотини и пукнатини се образува местна галванична клетка, като катодът е металът, който трябва да се огради, а анодът е окислено покритие. Целостта на такъв защитен филм не е от значение. Но колкото по-дебел е, толкова по-бавно ще се развие електрохимичната корозия, полезният ефект ще продължи по-дълго.
Катодът се нарича покритие с метал с висок потенциал, който в поредица от напрежения стои след защитения материал (например разпрашване на нисколегирани стомани с мед, калай, никел, сребро). Покритието трябва да бъде непрекъснато, тъй като при повреда се образуват местни галванични клетки, в които основният метал е анод, а защитният слой е катод.

Как да защитим метала от окисление
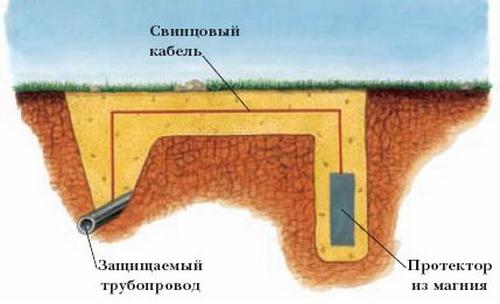
Електрохимичната защита от корозия е разделена на два типа: протектора и катода. Протектора, подобна на анодното покритие. По-голяма плоча от по-активна сплав е прикрепена към материала, който трябва да бъде защитен. Образува се галванична клетка, като основният метал служи като катод, а протекторът е анод (разяжда). Обикновено за този вид защита се използват цинкови, алуминиеви или магнезиеви сплави. Покровителят постепенно се разтваря, така че трябва периодично да се сменя.
Много проблеми в сектора на комуналните услуги и в индустрията като цяло са причинени от електрохимичната корозия на тръбопроводите. В борбата с него най-подходящ е методът на катодна поляризация. За тази цел металната конструкция, която е защитена от деструктивни окислителни процеси, е свързана с отрицателния полюс на някакъв външен източник на постоянен ток (след това става катод, това увеличава скоростта на еволюция на водорода, а скоростта на корозия намалява), а ниския метал се прикрепя към положителния полюс. ,
Методите за електрохимична защита са ефективни в проводяща среда (морската вода е отличен пример). Следователно, протектори често се използват за защита на подводните части на корабите.
Агресивно боравене
Този метод е ефективен, когато електрохимичната корозия на желязото протича в малък обем от проводима течност. Да се справят с разрушителните процеси в този случай по два начина:
- Отстраняване на кислород от течността (деаерация) в резултат на продухване с инертен газ.
- Въвеждането на инхибитори в околната среда - така наречените инхибитори на корозията. Например, ако повърхността е разрушена чрез окисляване с кислород, добавете органична материя молекули, които съдържат определени аминокиселини (имино, тио- и други групи). Те са добре адсорбирани върху металната повърхност и значително намаляват скоростта на електрохимичните реакции, водещи до разрушаване на повърхностния контакт.
заключение
Разбира се, химическата и електрохимичната корозия причиняват значителни щети както в промишлеността, така и в ежедневието. Ако металът не корозира, експлоатационният живот на много елементи, части, сглобки, механизми ще се увеличи значително. Сега учените активно разработват алтернативни материали, които могат да заменят метала, а не по-лоши в изпълнението, но вероятно е невъзможно напълно да се откаже от използването му в краткосрочен план. В този случай на преден план излизат усъвършенствани методи за защита на металните повърхности от корозия.