Кристални и аморфни тела: структура и свойства
Съществуват няколко агрегативни състояния, в които се намират всички органи и вещества. Това е:
- газ;
- течност;
- плазма;
- солидна.
Ако вземем предвид общата популация на планетата и пространството, тогава повечето вещества и тела са все още в състояние на газ и плазма. На самата Земя обаче съдържанието на твърди частици също е значително. Тук ще говорим за тях, за да разберем какви са кристалните и аморфни твърди вещества.
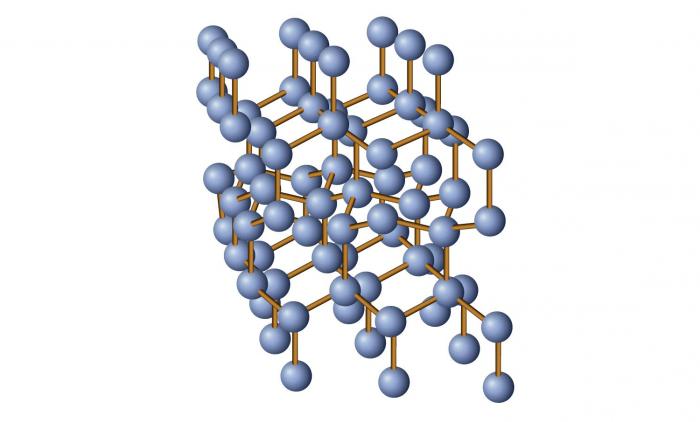
Кристални и аморфни тела: обща концепция
Всички твърди тела, тела, обекти са условно разделени на:
- кристал;
- аморфна.
Разликата между тях е огромна, защото основата на единицата са признаците на структурата и проявените свойства. Накратко, твърдите кристали са онези вещества и тела, които имат определен тип пространствени кристална решетка те имат способността да се променят в определена посока, но не във всички (анизотропия).
Ако обаче се характеризират аморфни съединения, тогава техният първи признак е способността да се променят физическите характеристики във всички посоки едновременно. Това се нарича изотропия.
Структурата, свойствата на кристалните и аморфните тела са напълно различни. Ако първата има ясно ограничена структура, състояща се от подредени частици в пространството, то последната няма ред.

Свойства на твърдите вещества
Кристалните и аморфни тела все пак принадлежат към една група твърди вещества и следователно имат всички характеристики на това агрегатно състояние. Това означава, че общите свойства за тях ще бъдат следните:
- Механично - еластичност, твърдост, способност за деформиране.
- Топлинно кипене и точки на топене, коефициент на топлинно разширение.
- Електрическа и магнитно - топлинна и електрическа проводимост.
Следователно, разглежданите държави притежават всички тези характеристики. Появяват се само в аморфни тела, те ще бъдат малко по-различни от тези в кристалните.
Важни свойства за промишлени цели са механични и електрически. Важна характеристика е способността да се възстанови от деформация или, напротив, да се разпадне и смила. Също така голяма роля играе фактът, че дадено вещество може да проведе електрически ток или да не може да го направи.

Кристална структура
Ако опишем структурата на кристалните и аморфните тела, тогава най-напред трябва да посочим вида на частиците, които ги съставят. В случай на кристали може да има йони атоми, атоми, йони (в метали) молекули (рядко).
Като цяло тези структури се характеризират с наличието на строго подредена пространствена решетка, която се формира в резултат на подреждането на частиците, образуващи веществото. Ако си представите структурата на кристал в преносен смисъл, вие получавате нещо подобно: атомите (или други частици) са раздалечени една от друга на определени разстояния, така че се получава идеалната клетка на бъдещата кристална решетка. След това тази клетка се повтаря многократно и така се формира цялостната структура.
Главната особеност е, че физическите свойства в такива структури варират паралелно, но не във всички посоки. Това явление се нарича анизотропия. Това означава, че ако действате върху една част от кристала, втората страна може да не реагира на нея. Така че можете да мелите половин парче сол, но второто ще остане непокътнато.
Кристални типове
Обичайно е да се обозначават два варианта на кристали. Първата е монокристална структура, т.е. когато самата решетка е 1. Кристалните и аморфните тела в този случай са доста различни по свойства. В крайна сметка, един кристал се характеризира с анизотропия в чиста форма. Това е най-малката елементарна структура.
Ако единичните кристали се повтарят многократно и се комбинират в едно, тогава става въпрос за поликристал. Тогава не се говори за анизотропия, тъй като ориентацията на елементарните клетки нарушава общата подредена структура. В това отношение, поликристалите и аморфните тела са близо един до друг по отношение на техните физични свойства.

Метали и сплави
Кристалните и аморфни тела са много близки една до друга. Лесно е да се убедите в това, като вземете за пример метали и техните сплави. Сами по себе си те са в нормални условия на твърди вещества. Обаче, при определена температура, те започват да се топят и докато настъпи пълна кристализация, те ще останат в състояние на разтягане, гъста, вискозна маса. И това вече е аморфното състояние на тялото.
Следователно, строго погледнато, почти всяко кристално вещество може при определени условия да стане аморфно. Точно както при второто втвърдяване, то става твърдо вещество с подредена пространствена структура.
Металите могат да имат различни типове пространствени структури, като най-известните и изучавани са следните:
- Обикновено кубичен.
- Лице центрирано.
- Obemotsentrirovannaya.
Структурата на кристала може да се основава на призма или пирамида, а основната му част е представена от:
- триъгълник;
- успоредник;
- по квадрат;
- шестоъгълник.
Вещество, което има проста нормална кубична решетка, има идеални изотропни свойства.

Концепцията за аморфен
Кристалните и аморфни тела отвън са достатъчно прости за разграничаване. В крайна сметка, последните често могат да бъдат объркани с вискозни течности. Структурата на аморфна субстанция също се основава на йони, атоми, молекули. Те обаче не образуват подредена строга структура и следователно техните свойства се променят във всички посоки. Това означава, че те са изотропни.
Частиците са подредени произволно, случайно. Само понякога те могат да образуват малки локуси, които все още не влияят на показаните общи свойства.
Свойства на подобни тела
Те са идентични с тези на кристалите. Разликите са само по показатели за всеки отделен орган. Така например можем да разграничим такива характерни параметри на аморфните тела:
- твърдост;
- плътност;
- вискозитет;
- пластичност;
- проводимост и полупроводник.
Често можете да отговорите на граничните условия на съединенията. Кристалните и аморфни тела могат да станат полуаморфни.
Също така интересна е характеристиката на въпросната държава, която се проявява с остро външно влияние. Така че, ако аморфното тяло е подложено на силен удар или деформация, то тогава е способно да се държи като поликристал и да се разделя на малки парчета. Обаче, ако времето е дадено на тези части, те скоро ще се съберат отново и ще се превърнат в вискозно течно състояние.

Това състояние на съединенията няма специфична температура, при която настъпва фазов преход. Този процес се разширява значително, понякога дори десетилетия (например разлагане на полиетилен с ниско налягане).
Примери за аморфни вещества
Има много примери за такива вещества. Нека определим някои от най-очевидните и често срещани.
- Шоколадът е типично аморфно вещество.
- Смоли, включително фенол-формалдехид, всички пластмаси.
- Амбър.
- Стъкло от всякакъв състав.
- Битум.
- Tar.
- Восък и др.
Аморфно тяло се образува в резултат на много бавна кристализация, т.е. увеличаване на вискозитета на разтвора при понижаване на температурата. Често е трудно да се нарекат такива вещества твърди, по-скоро те се отнасят до вискозни дебели течности.
Съединения, които изобщо не кристализират по време на втвърдяването, имат специално състояние. Те се наричат очила, а държавата - стъклени.
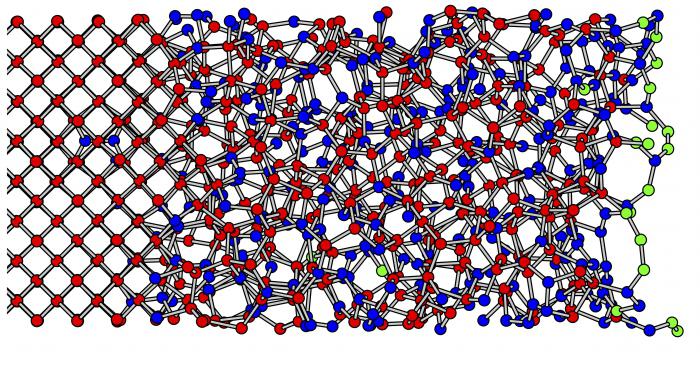
Стъклени вещества
Свойствата на кристалните и аморфните тела са сходни, както установихме, поради техния общ произход и единна вътрешна природа. Но понякога те се разглеждат отделно като специално състояние на веществата, наречени стъкловидното тяло. Това е хомогенен минерален разтвор, който кристализира и втвърдява без образуването на пространствени решетки. Това означава, че тя остава изотропна по отношение на променящите се свойства винаги.
Например, конвенционалното прозоречно стъкло няма точната стойност на точката на топене. То само с увеличаване на този индикатор бавно се топи, омекотява и се превръща в течно състояние. Ако ефектът бъде спрян, тогава ще се осъществи обратния процес и ще започне втвърдяването, но без кристализация.
Такива вещества са високо ценени, стъкло днес е един от най-често срещаните и търсени строителни материали в света.